Patientenzentrierte Wahl des prandialen Insulins
Verschiedene prandiale Insuline, einschließlich reguläres Humaninsulin, Aspart, Glulisin, Lispro und schnell wirkendes Insulin Aspart (FIAsp), werden als Teil von Basal plus, Basal Bolus oder Prandial allein verwendet. Einige prandiale Insuline, auch kurzwirksame Insuline genannt, können auch intravenös oder in Insulininfusionspumpen verwendet werden. Der Fokus dieses Leitartikels liegt darauf, prandiale Insuline zu klassifizieren, ihre pharmakologischen Eigenschaften zu verstehen und ihre Verwendung in der aktuellen klinischen Praxis zu untersuchen. Es werden auch die einzigartigen Eigenschaften hervorgehoben, die eine bevorzugte Verwendung dieser Insuline in bestimmten klinischen Situationen ermöglichen.
Insulin ist ein wesentlicher Bestandteil der glukosesenkenden Therapie. Die meisten Empfehlungen zur glukosesenkenden Therapie konzentrieren sich auf die Insulinregime, die für die Einleitung und Intensivierung ausgewählt werden sollen.1,2 Debatte und Kontroverse dreht sich in der Regel um die Wahl der basalen im Vergleich zu einem vorgemischten Regime als anfängliche Insulintherapie.3 In einem solchen Szenario wird die Bedeutung prandialer Insuline und spezifischer prandialer Insulinpräparate häufig ignoriert. Diese Übersicht untersucht die Ähnlichkeiten und Unterschiede verschiedener prandialer Insulinpräparate und gibt Einblicke in ihren unterschiedlichen Nutzen in der Diabetesversorgung.
Einstufung
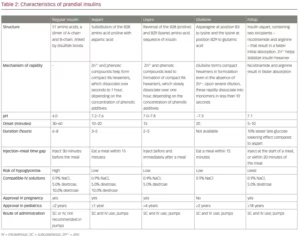
Die verschiedenen Arten von Prandialinsulinen, die weltweit erhältlich sind, können als schnell wirkendes Humaninsulin, schnell wirkende Insulinanaloga und ultraschnell wirkende Analoga klassifiziert werden (Tabelle 1). Diese Klassifizierung basiert auf dem Ursprung des Insulins und seinen pharmakokinetischen Eigenschaften, insbesondere dem Wirkungseintritt. Obwohl diese taxonomische Struktur pharmakologischer Natur ist, hat sie auch klinischen Nutzen. Es informiert den Zeitpunkt der Injektion in Bezug auf Mahlzeiten und ermöglicht Flexibilität bei der Verabreichung von ultraschnell wirkendem Insulin. Die Ähnlichkeiten und Unterschiede zwischen den verschiedenen Prandialinsulinen sind in Tabelle 2 aufgeführt. Viele dieser Insuline sind auch als Biosimilars wie reguläres Insulin und Lispro erhältlich.
Es sind auch hochkonzentrierte Versionen von Prandialinsulinen erhältlich, zum Beispiel: U500 Regular Insulin, U200 lispro und U200 regular Insulin. U200 lispro hat ähnliche pharmakokinetische und pharmakodynamische Eigenschaften wie U100 lispro. Im Vergleich zu U100-Normalinsulin hat U500-Normalinsulin eine längere Zeit bis zur maximalen Wirkung (5 Stunden gegenüber 6 Stunden) und eine längere Wirkdauer (18 Stunden gegenüber 24 Stunden). Verringertes Volumen, weniger Injektionen und weniger Schmerzen während der Verabreichung sind einige Vorteile dieser konzentrierten Insuline.4,5
Intravenöse Anwendung
Prandialinsulin kann intravenös oder subkutan und selten intramuskulär verabreicht werden.6-8 Es kann auch mit Total parenteral Nutrition Bags zur zentralen intravenösen Verabreichung gemischt werden. Die strukturellen Unterschiede zwischen verschiedenen Analoga beeinflussen ihre Kompatibilität mit verschiedenen intravenösen Flüssigkeiten. Während Insulinglulisin mit normaler Kochsalzlösung und Ringer-Laktat kompatibel ist, kann es daher nicht in dextrosehaltigen Lösungen verwendet werden. Die anderen Prandialinsuline können mit allen gängigen intravenösen Infusionsflüssigkeiten verdünnt werden. Dies ermöglicht die uneingeschränkte Verwendung von normalem Humaninsulin, Aspart, Lispro und FIAsp im Krankenhaus. Insulin-Stewardship-Programme auf Intensivstationen und Krankenstationen sollten die Zubereitung und Konzentration der verwendeten Prandialinsuline sowie deren Verabreichungsart widerspiegeln.Eine Verringerung der Morbidität und Mortalität wurde mit Insulinaspart in Krankenhäusern in Verbindung gebracht.10 Insulin Aspart mit einem besseren Wirksamkeits- und Sicherheitsprofil als kurzwirksames Humaninsulin scheint eine gute Alternative zu kurzwirksamem Humaninsulin zu sein.10

In einigen Ländern erhöht die Verfügbarkeit von U40-, U100- und U500-Insulinfläschchen und -spritzen die Wahrscheinlichkeit von Dosierungsfehlern, es sei denn, die Patienten sind zum Zeitpunkt der Einleitung der Insulintherapie über verschiedene Arten von Fläschchen und Spritzen informiert und mit ihnen vertraut. Die Patienten sollten darüber informiert werden, dass U100-Durchstechflaschen nur mit U100-Spritzen und U40-Durchstechflaschen nur mit U40-Insulinspritzen verwendet werden dürfen.11
Inhalierte prandiale Insuline
Die ersten beiden schnell wirkenden inhalativen Insuline Exubera® (Pfizer, New York City, New York, USA) und Afrezza® (MannKind Corporation, Westlake Village, Kalifornien, USA) beseitigten hypothetisch die mit der subkutanen Insulinabgabe verbundenen psychologischen Barrieren wie Nadelphobie und falsche Injektionstechnik.12 Diese inhalativen Insulinpräparate entsprachen jedoch nicht ihren Erwartungen.
Weniger als 2 Jahre nach seiner Zulassung wurde Exubera aufgrund mehrerer produktbezogener Nachteile vom Markt genommen und hatte „keine Akzeptanz bei Patienten und Ärzten gefunden“, was zu einem schlechten Verkaufsvolumen führte.13 Hypoglykämie war nachweislich die häufigste Nebenwirkung von Exubera. Es wurden viele Nebenwirkungen auf die Atemwege berichtet, darunter ein erhöhtes Risiko für Atemwegsinfektionen, Husten, Pharyngitis und Rhinitis. In Bezug auf Lungenkrebs wurde eine Änderung des Sicherheitsetiketts vorgenommen, als bei Patienten, die Exubera einnahmen, sechs neu diagnostizierte Fälle von malignen Lungenerkrankungen festgestellt wurden.14
Afrezza scheint entscheidende Vorteile gegenüber Exubera zu haben. Das Verabreichungssystem ist klein, schlank und in Einheiten dosiert und bietet eine einfache Dosisumrechnungstabelle, während das Verabreichungssystem von Exubera groß, umständlich und in Milligramm dosiert war.12 Das Sicherheitsprofil von Afrezza ähnelt dem von Exubera, mit einer Abnahme der Lungenfunktion und einer leicht erhöhten Inzidenz von Lungenkrebs. Nach der Zulassung von Afrezza wurden neue Bedenken vorgebracht, die die US-amerikanische Food and Drug Administration (FDA) dazu veranlassten, eine Risikobewertungs- und Minderungsstrategie sowie eine Black-Box-Warnung zu verlangen, die den Patienten über ein erhöhtes Risiko für akute Bronchospasmen bei Patienten mit chronischer Lungenerkrankung informiert.15 Diabetische Ketoazidose wurde auch häufiger bei Patienten in der Afrezza-Kohorte gefunden.15
Übergangspflege
Beim Übergang von einer Intensivstation in eine unkritische Krankenhausumgebung oder von einem Krankenhaus in eine OPD-Pflegeumgebung treten andere Überlegungen in den Vordergrund. Ein schneller Wirkungseintritt ermöglicht einen einfachen Übergang von intravenösen zu subkutanen Injektionen mit minimalem Risiko einer Hyperglykämie und ohne Absetzen von intravenösem Insulin. Ein ordnungsgemäß geplanter Übergang erfordert, dass die erste Dosis subkutanes Insulin mindestens 1 Stunde (bei kurzwirksamen subkutanen Insulinen; idealerweise 2-3 Stunden bei langwirksamen subkutanen Insulinen) vor Absetzen der Infusion verabreicht wird.16 Die Verwendung ultraschnell wirkender Analoga wie FIAsp bietet in diesem Zusammenhang praktische und pragmatische Vorteile.17
Subkutane Anwendung
Wenn Prandialinsulin subkutan angewendet wird, kann es als Teil eines Basal Plus-, Basal Bolus- oder Prandial-only-Regimes verwendet werden.18 In allen diesen Regimen wird das Insulin vor der Mahlzeit verabreicht. Die ideale Zeitspanne zwischen Injektion und Mahlzeit variiert je nach prandialer Zubereitung. Während alle prandialen Insuline in dieser Umgebung wirksam sind, sind Sicherheitstoleranz und Bequemlichkeit die entscheidenden Faktoren für eine patientenzentrierte Insulinauswahl. Humanes reguläres Insulin ist nach wie vor das wirtschaftlichste Insulin weltweit, ist jedoch in bestimmten Ländern möglicherweise nicht verfügbar. Normales Humaninsulin sollte 30 Minuten vor einer Mahlzeit injiziert werden, was jedoch seine Flexibilität einschränkt.19 Die schnell wirkenden Analoga bieten eine größere Flexibilität und werden in dieser Hinsicht von ultraschnell wirkenden Analoga übertroffen. Während Aspart, Lispro und Glulisin unmittelbar vor einer Mahlzeit injiziert werden können, kann FIAsp bis zu 20 Minuten nach einer Mahlzeit verabreicht werden20 Die Verfügbarkeit kann jedoch von Land zu Land variieren.
Ein weiterer Vorteil des ultraschnell wirkenden FIAsp ist sein schnellerer Wirkungseintritt und -peak, was zu einer besseren Auflösung der 1-stündigen postprandialen Glykämie führt.21 Dies ist hilfreich in klinischen Situationen wie Schwangerschaftsdiabetes und Kortikosteroid-induziertem Diabetes sowie bei Menschen mit Ernährungsvorlieben für Mahlzeiten mit hohem Kohlenhydrat- und glykämischen Index. Die relativ schnellere Verringerung der Insulinwirkung führt zu einem geringeren Risiko einer Hypoglykämie vor den Mahlzeiten mit FIAsp (da die Gesamtwirkungsdauer dieses Insulins etwas geringer ist als die von Insulinaspart). Im gleichen Zusammenhang gibt es Daten, die darauf hindeuten, dass bei der Anwendung von FIAsp zum Abendessen ein geringeres Risiko für nächtliche Hypoglykämie besteht, da die Wirkdauer im Vergleich zu schnell wirkenden Insulinanaloga (Aspart, Lispro oder Glulisin), deren Wirkdauer länger dauern kann, verringert ist in die Nacht.21 Dies verringert den Grad der Unannehmlichkeiten im Lebensstil des Patienten im Zusammenhang mit der Verwendung von Prandialinsulin und ermöglicht eine größere Freiheit bei der Planung von körperlicher Aktivität, Bewegung oder Freizeitaktivitäten wie dem Essen in einem Restaurant, in dem die Menge an Kohlenhydraten / Kalorien unvorhersehbar sein kann (und wo FIAsp nach Abschluss der Mahlzeit eingenommen werden kann). Es beseitigt auch die Notwendigkeit eines 3 + 3-Mahlzeitmusters, das herkömmlicherweise in Basalbolusregimen vorgeschrieben ist.
Die Möglichkeit, schnell und ultraschnell wirkende Insuline unmittelbar vor oder sogar nach einer Mahlzeit zu injizieren, ermöglicht es, die Insulindosis je nach Appetit oder Kohlenhydratzählung anzupassen. Diese Flexibilität ist besonders bei sehr jungen und älteren Menschen sowie bei Menschen mit Appetitlosigkeit, Übelkeit oder Erbrechensrisiko von Vorteil, z. B. bei Patienten mit Nieren-, Leber- oder Magen-Darm-Erkrankungen. In In-vivo-Studien wurde berichtet, dass FIAsp eine schnellere Kinetik aufweist, wenn es intradermal injiziert wird.22

Insulinpumpen
Die Insulinpumpentherapie basiert auf der Verwendung von kurzwirksamem oder prandialem Insulin als kontinuierliche subkutane Infusion, um den Basalinsulinspiegel aufrechtzuerhalten. Die prandiale Dosierung erfolgt durch Drücken der Pumpentasten zu den Mahlzeiten basierend auf vorgegebenen Kohlenhydratverhältnissen von Insulin zu den Mahlzeiten. Dieses Insulinabgabevehikel passt die Basalinsulinraten und Bolusinsulinraten genauer an, insbesondere bei Typ-1-Diabetikern und spröden Diabetikern. Neuere Technologien, wie kontinuierliche Glukoseüberwachungssysteme, werden mit neueren Pumpen (z. B. MiniMed ™ 670G, Medtronic, Dublin, Irland) kombiniert und können die Basalraten in diesen Pumpen automatisch basierend auf dem Blutzuckerspiegel des Patienten mithilfe selbstlernender Cloud-verknüpfter Algorithmen anpassen (IBM Watson Cloud wird vom Medtronic 670G Closed Loop Hybrid System verwendet).
Die physikalisch-chemischen Unterschiede zwischen verschiedenen Insulinen führen zu Unterschieden in Stabilität, Verträglichkeit und Nützlichkeit in Insulinpumpen- oder Infusionssystemen. In Studien wurde festgestellt, dass Insulinaspart während einer kontinuierlichen subkutanen Insulininfusion hinsichtlich der physikalischen Stabilität gegen die Bildung unlöslicher Insulinfibrillen sowie der chemischen Stabilität hinsichtlich der Bildung löslicher Proteine mit hohem Molekulargewicht stabiler ist als Insulinglulisin.23,24
Flexibilität und Prandialinsulin
Bei der patientenzentrierten Behandlung von Diabetes sollte versucht werden, eine wirksame, sichere Blutzuckerkontrolle mit minimalem Eingriff in den Lebensstil des Patienten zu gewährleisten. Die pharmakodynamischen und pharmakokinetischen Eigenschaften eines Prandialinsulins sollten es ermöglichen, Flexibilität in Bezug auf Verabreichungsweg und -zeitpunkt, Dosierung, Wahl des Mahlzeitenmusters und die Fähigkeit zur Planung von körperlicher Aktivität, Bewegung oder Freizeitaktivität zu bieten. Diese zusätzliche Funktion kann auch die Einhaltung der Insulintherapie durch den Patienten verbessern.20 Moderne ultraschnell wirkende Prandialinsuline können diese Flexibilität bieten. Wenn Verfügbarkeit, Zugang und Erschwinglichkeit kein Problem darstellen, sollten solche Insulinpräparate für die Behandlung von Diabetes bevorzugt werden. Klinische Situationen, die bevorzugte Indikationen für FIAsp sind, sind in Tabelle 3 aufgeführt.
Wir wiederholen, dass unabhängig von der verwendeten Insulinzubereitung die korrekte Injektionstechnik befolgt werden muss. Es gibt keinen Ersatz für die richtige Insulintechnik, die sicherstellt, dass die richtige Insulindosis zum richtigen Zeitpunkt auf bequeme Weise in gesundes Unterhautgewebe verabreicht wird.25
Zusammenfassung
Dieser kurze Überblick bietet einen patientenzentrierten Ansatz und klinisch orientierte Einblicke in die Verwendung verschiedener prandialer Insuline. Es klassifiziert und beschreibt diese Präparate und teilt Vorschläge bezüglich ihrer rationellen Verwendung als intravenöses und vorübergehendes subkutanes Insulin. Dieser Artikel unterstreicht die Flexibilität, die ultraschnell wirkendes Insulin heute in der Diabetesversorgung ermöglicht.