Fisiopatología / Fundación Internacional de Osteoporosis
Las hormonas son posiblemente los moduladores más importantes de la formación ósea. Está bien establecido que el estrógeno Lindsay, R., Prevención y tratamiento de la osteoporosis. Lancet, 1993. 341( 8848): p. 801-5.
. labios de hormona paratiroidea, P., Fisiología de vitamina D. Prog Biophys Mol Biol, 2006. 92 (1): p. 4-8
. y, en menor medida, testosterona directa o indirectamente a través de la conversión en estrógeno Seeman, E., La base estructural de la fragilidad ósea en los hombres. Bone, 1999. 25 (1): p. 143-7.
Van Pottelbergh, I., et al., Estado perturbado de esteroides sexuales en hombres con osteoporosis idiopática y sus hijos. J Clin Endocrinol Metab, 2004. 89( 10): p. 4949-53.
. son esenciales para el desarrollo y mantenimiento óptimo de los huesos. De estos, ahora se cree que los estrógenos tienen el efecto más directo sobre las células óseas, interactuando con proteínas específicas, o receptores, en la superficie de los osteoblastos y osteoclastos Zallone, A., Acciones directas e indirectas de los estrógenos sobre los osteoblastos y osteoclastos. Ann N Y Acad Sci, 2006. 1068: p. 173-9.
Esta interacción desencadena una compleja cadena de eventos dentro de las células, aumentando la actividad de los osteoblastos al mismo tiempo que interfiere con la comunicación osteoblasto-osteoclasto – una de las ironías del remodelado óseo es que los factores de liberación de osteoblastos que estimulan los osteoclastos e impulsan la reabsorción ósea, como veremos a continuación.
Los efectos de los estrógenos están mediados por un tipo específico de receptor de superficie celular llamado receptor alfa de estrógenos (ERa), que se une y transporta la hormona al núcleo de la célula, donde el complejo receptor-hormona actúa como un interruptor para activar genes específicos. Los receptores ERa se encuentran en la superficie de los osteoblastos, al igual que el receptor alfa relacionado con el receptor de estrógeno (ERRa), que puede desempeñar un papel auxiliar en la regulación de las células óseas Bonnelye, E. y J. E. Aubin, receptor alfa relacionado con el receptor de estrógeno: un mediador de la respuesta del estrógeno en el hueso. J Clin Endocrinol Metab, 2005. 90 (5): p. 3115-21.
. Estudios recientes también sugieren que la globulina fijadora de hormonas sexuales (SHBG), que facilita la entrada de estrógenos en las células, también puede desempeñar un papel de apoyo Goderie-Plomp, H. W., et al., Endogenous sex hormones, sex hormone-binding globulin, and the risk of incident vertebral fractures in elderly men and women: the Rotterdam Study. J Clin Endocrinol Metab, 2004. 89 (7): p. 3261-9.
.
El estrógeno, por supuesto, se produce y secreta en el torrente sanguíneo a cierta distancia del hueso y también tiene efectos profundos en otros tejidos, como el útero y la mama. Pero hay otras moléculas de señalización producidas localmente que tienen profundos efectos en la fisiología ósea.

Figure taken from Ferrari & Roux, 2019 Pocket Reference to Osteoporosis, S. Ferrari, Roux, C., Editor 2019, Springer International Publishing.
.
Prostaglandins, particularly prostaglandin E2 (PGE2), stimulate both resorption and formation of bone Pilbeam, C.C., J.R. Harrison, and L.G. Raisz, Chapter 54 – Prostaglandins and Bone Metabolism, in Principles of Bone Biology (Second Edition), J.P. Bilezikian, L.G. Raisz, and G.A. Rodan, Editors. 2002, Academic Press: San Diego. p. 979-994
. PGE2 es un lípido que se forma en varias células óseas a partir de un precursor llamado ácido araquidónico. El primer paso en la síntesis de PGE2 se lleva a cabo por una enzima llamada ciclooxigenasa 2 (COX2) e inhibidores de esta enzima pueden prevenir la formación ósea en respuesta al estrés mecánico en animales Forwood, R. M., la ciclooxigenasa inducible (COX-2) media la inducción de la formación ósea por carga mecánica in vivo. J Bone Miner Res, 1996. 11( 11): p. 1688-93.
. La PGE2 puede ser necesaria para la formación ósea inducida por el ejercicio.
Existe evidencia de que el riesgo de fractura aumenta en personas que toman antiinflamatorios no esteroideos que inhiben la COX-2 Carbone, L. D., et al., Asociación entre la densidad mineral ósea y el uso de antiinflamatorios no esteroideos y aspirina: impacto de la selectividad de la ciclooxigenasa. J Bone Miner Res, 2003. 18( 10): p. 1795-802 también puede aumentar. Otro conjunto de moléculas lipídicas que parecen regular el remodelado óseo son los leucotrienos. También derivados del ácido araquidónico, se ha encontrado que reducen la densidad ósea en ratones Traianedes, K., et al., Los metabolitos de la 5-lipoxigenasa inhiben la formación ósea in vitro. Endocrinología, 1998. 139 (7): p. 3178-84.
.
El impacto de cualquiera de estas hormonas en el remodelado óseo depende de cómo alteran la actividad de los osteoclastos y/o osteoblastos. Receptores específicos de la superficie celular ayudan a transmitir señales de las células óseas externas al núcleo celular, donde se pueden activar o desactivar diferentes genes que regulan la actividad celular. Estos incluyen receptores para proteínas morfogenéticas óseas (BMP), una familia de proteínas que son potentes inductores de la formación ósea.
Se han encontrado receptores BMP en la superficie de células precursoras de osteoblastos Mbalaviele, G., et al., Beta-catenina y BMP-2 se sinergizan para promover la diferenciación osteoblástica y la formación de hueso nuevo. Bioquímica de células J, 2005. 94 (2): p. 403-18.
. Otro receptor de superficie celular llamado receptor de proteína 5 relacionada con lipoproteínas de baja densidad (LDL) (LRP5), un receptor Wnt, también puede ser importante para la formación ósea porque la pérdida de LRP5 en animales conduce a osteoporosis severa Gong, Y., et al., La proteína 5 relacionada con el receptor de LDL (LRP5) afecta la acumulación ósea y el desarrollo ocular. Cell, 2001. 107 (4): págs. 513-23.
. Los receptores BMP y LRP5 pueden cooperar para estimular la acción de los osteoblastos, aunque no se ha aclarado exactamente cómo podría ocurrir esto.
La esclerostina, producto del gen SOST y expresada por los osteocitos, se une al receptor LRP5/6 en los osteoblastos e inhibe la señalización Wnt, lo que lleva a una disminución en la formación ósea Bonewald, L. F., El sorprendente osteocito. J Bone Miner Res, 2011. 26 (2): p. 229-38. Li, X., et al., La esclerostina se une a LRP5 / 6 y antagoniza la señalización canónica de Wnt. J Biol Chem, 2005. 280( 20): p. 19883-7.
. La hormona paratiroidea (PTH) y la carga mecánica disminuyen la secreción de esclerostina por los esteocitos Bellido, T., et al., La elevación crónica de la hormona paratiroidea en ratones reduce la expresión de esclerostina por los osteocitos: un nuevo mecanismo para el control hormonal de la osteoblastogénesis.Endocrinología, 2005. 146( 11): p. 4577-83. Robling, A. G., et al., La estimulación mecánica del hueso in vivo reduce la expresión de Sost/esclerostina en los osteocitos. J Biol Chem, 2008. 283 (9): p. 5866-75.
. Se ha desarrollado un anticuerpo contra la esclerostina como un fármaco potencial con potentes propiedades sobre la resistencia ósea. Read more on anabolics as treatments.

Figure taken from Ferrari & Roux, 2019 Pocket Reference to Osteoporosis, S. Ferrari, Roux, C., Editor 2019, Springer International Publishing.
.
Un receptor de superficie celular llamado RANK (para activador del receptor de NFkB) produce células precursoras de osteoclastos para convertirse en osteoclastos completamente diferenciados cuando RANK es activado por su ligando RANK asociado (RANKL) Yasuda, H., et al., El factor de diferenciación de osteoclastos es un ligando para el factor inhibidor de osteoprotegerina / osteoclastogénesis y es idéntico al TRANCE / RANKL. Proc Natl Acad Sci U S A, 1998. 95 (7): p. 3597-602. Lacey, D. L., et al., El ligando de osteoprotegerina es una citocina que regula la diferenciación y activación de los osteoclastos. Cell, 1998. 93 (2): p. 165-76.
.
RANKL, de hecho, es producido por osteoblastos y es una de las muchas moléculas de señalización que facilitan la conversación cruzada entre los osteoblastos y los osteoclastos y ayudan a coordinar el remodelado óseo Theill, L. E., W. J. Boyle y J. M. Penninger, RANK-L y RANK: células T, pérdida ósea y evolución de los mamíferos. Annu Rev Immunol, 2002. 20: p. 795-823.
. Osteoprotegerina, otra proteína liberada por los osteoblastos Suda, T., et al., Modulación de la diferenciación y función de los osteoclastos por los nuevos miembros de las familias de receptores y ligandos del factor de necrosis tumoral. Endocr Rev, 1999. 20 (3): p. 345-57.
, también puede unirse a RANKL, actuando como señuelo para evitar que RANK y RANKL entren en contacto. El equilibrio de RANKL / osteoprotegerina puede ser crucial en la osteoporosis. De hecho, estudios en animales mostraron que el aumento de la producción de osteoprotegerina conduce a un aumento de la masa ósea, mientras que la pérdida de la proteína conduce a osteoporosis y un aumento de fracturas Bucay, N., et al., ratones con deficiencia de osteoprotegerina desarrollan osteoporosis de inicio temprano y calcificación arterial. Genes Dev, 1998. 12 (9): p. 1260-8.
. Los inhibidores de RANKL también han demostrado ser prometedores como tratamiento potencial para la osteoporosis en humanos.
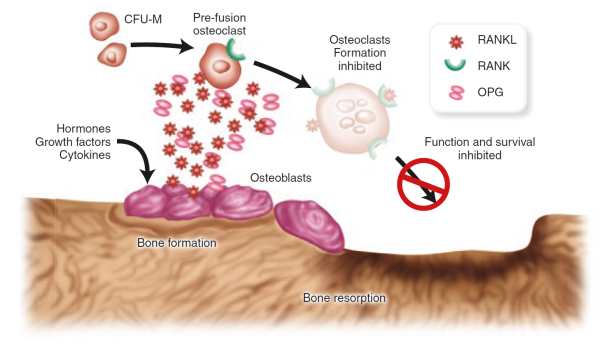
Figure taken from Ferrari & Roux, 2019 Pocket Reference to Osteoporosis, S. Ferrari, Roux, C., Editor 2019, Springer International Publishing.
.
En los últimos años también se descubrió un segundo sistema de señalización celular complementario que ayuda a impulsar la formación y activación de osteoclastos. En ausencia de la proteína 12 activadora de DNAX (DAP12) y de la cadena γ común del Receptor Fc (FcRy), dos receptores de la superficie celular, los ratones desarrollan osteoporosis severa, exactamente lo contrario de la osteoporosis, caracterizada por un aumento dramático de la densidad ósea Mocsai, A., et al., Las proteínas adaptadoras inmunomoduladoras DAP12 y la cadena gamma del receptor Fc (FcRgamma) regulan el desarrollo de osteoclastos funcionales a través de la tirosina quinasa Syk. Proc Natl Acad Sci U S A, 2004. 101( 16): p. 6158-63. Koga, T., et al., Las señales costimulatorias mediadas por el motivo ITAM cooperan con RANKL para la homeostasis ósea. Nature, 2004. 428( 6984): p. 758-63.
. Estos dos receptores de la superficie celular interactúan con un grupo de proteínas en la célula llamadas proteínas adaptadoras ITAM (motivo de activación basado en tirosina de inmunorreceptores) para causar un aumento en el calcio intracelular.
Los estudios sugieren que el RANK/RANKL y las vías mediadas por ITAM cooperaron para inducir la actividad total de los osteoclastos. Estas dos vías pueden converger para activar una proteína llamada factor nuclear de células T activadas (NFAT) c1. NFATc1 sirve como un interruptor maestro para la reabsorción ósea porque activa los genes que las células precursoras de los osteoclastos necesitan para convertirse en osteoclastos completamente activos Takayanagi, H., Conocimiento mecanicista de la diferenciación de los osteoclastos en osteoinmunología. J Mol Med (Berl), 2005. 83 (3): p. 170-9.
.