fenantreen
- fenantreen chemische eigenschappen,Gebruik,productie
- niet-lineaire polycyclische aromatische koolwaterstoffen
- moleculaire structuur
- chemische eigenschappen
- gebruikt
- preparaat
- chemische eigenschappen
- chemische eigenschappen
- fysische eigenschappen
- gebruikt
- gebruikt
- definitie
- productiemethoden
- Synthesis Reference(s)
- General Description
- lucht & Waterreacties
- Reactiviteitsprofiel
- gezondheidsrisico
- brandgevaar
- veiligheidsprofiel
- potentiële blootstelling
- carcinogeniteit
- bron
- lot in het milieu
- scheepvaart
- zuiveringsmethoden
- afvalverwijdering
fenantreen chemische eigenschappen,Gebruik,productie
niet-lineaire polycyclische aromatische koolwaterstoffen
fenantreen is de eenvoudigste niet-lineaire polycyclische aromatische koolwaterstoffen met drie benzeenringstructuur, zijnde de isomeer van het antraceen. In 1872 heeft E. Ostermayer et al het fenantreen in de antraceenoliefractie in koolteerdestillaat geïdentificeerd, zijnde een van koolteerverwerkende producten. In de hogetemperatuurkoolteer is het fenantreengehalte slechts secundair aan naftaleen en bedraagt het ongeveer 4 ~ 6%, voornamelijk geconcentreerd in de antraceenoliefracties. De chemische activiteit van fenantreen is sterker dan die van naftaleen, maar zwakker dan die van antraceen, en de oxidatie-en additie-reacties kunnen ook optreden op 9 en 10 posities. het fenantreen is een kleurloos kristal met glans, en het uit ethanol neergeslagen fenantreen is een kleurloos monoclinisch kristal. Het fenantreen is een bladachtig kristal met een relatieve dichtheid van 1.179 (25/4℃) en een brekingsindex van 1,6450, smeltpunt van 101 °C en kookpunt van 340 °C. Het kan worden gesublimeerd, onoplosbaar in water, slecht oplosbaar in ethanol, oplosbaar in ether, benzeen, azijnzuur, chloroform, tetrachloorkoolstof en koolstofdisulfide. De oplossing vertoont blauwe fluorescentie. De 1, 4, 5, 8-posities zijn hetzelfde, bekend als α-positie; de 2, 3, 6, 7-Positie zijn ook hetzelfde, bekend als β-positie; de 9, 10-posities zijn hetzelfde, bekend als de ?-positie. De chemische eigenschap ligt tussen naftaleen en antraceen. Het kan ook optiereactie hebben in de 9, 10-positie, maar niet zo eenvoudig als antraceen. Oxidatie vindt ook plaats op de 9, 10-positie met oxidatie die fenantrenequinon geeft. Er kunnen ook substitutiereacties optreden. Het kan ook worden verkregen door afscheiding uit de antraceenoliefractie van koolteerolie. Fenantreen kan worden gebruikt bij de vervaardiging van pesticiden en kleurstoffen, maar kan ook worden gebruikt als stabilisator van de hoogrenderende & bestrijdingsmiddelen met lage toxiciteit en rookloze poeder explosieven.
fenantreen kan worden gebruikt om kleurstoffen, geneesmiddelen en harsen te produceren na conversie verwerking. De oxidatieproducten phenanthrenequinone kan als kleurstoffen, fungiciden en polymerisatieinhibitors worden gebruikt; 9, 10-bifenyl dicarbonzuur wordt gebruikt om polyester en alkydhars te vervaardigen; 9, 10-dihydro-9-fenathroic zuur is een plantengroei-stimulerend hormoon; Perhydrophenantreen gemaakt door hydrogenering van fenantreen kan worden gebruikt in de productie van vliegtuigbrandstof; zijn gesulfoneerd product, fenanthrene sulfonzuur kan worden gebruikt als bindmiddel en looien.
De fenantreenhoudende moedervloeistof tijdens de productie van geraffineerd antraceen met behulp van oplosmiddelmethode, na terugwinning van oplosmiddel en verdere kristallisatiefiltratie, kan ruw fenantreen opleveren dat 40% fenantreen bevat.
Het ruwe fenantreen wordt, na verwijdering van residuoplosmiddelen in de smeltketel en vervolgens met 20 theoretische platen in de rectificatietoren gerectificeerd, de fracties van 335 tot 340 °C uitgesneden, gevolgd door afkoeling, kristallisatie en filtering om het industriële fenantreen met een fenantreengehalte van meer dan 70% te verkrijgen. .de bovenstaande informatie is samengesteld door Tongtong uit Chemicalbook.
moleculaire structuur
de moleculaire structuur van fenantreen en antraceen is vergelijkbaar met elkaar, waarbij alle atomen zich in hetzelfde vlak, maar niet in dezelfde lijn bevinden, aangezien het een gesloten conjugaatsysteem met aromatische eigenschap is. De 1, 2, 3, 4, 10 standen en de 5, 6, 7, 8, 9 posities binnen de moleculen elkaar, respectievelijk, maar er waren verschillen in activiteit op de 5 posities, waaronder 9 en 10 waren de hogere activiteit met substitutie, oxidatie en toevoeging plaatsvindt op 9 en 10 posities: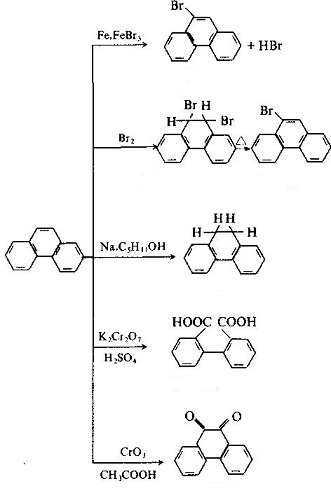
Phenanthrenequinone is een pesticide gebruikt als germicide zaad dressing, in staat om te voorkomen dat tarwe schurft, harde vuiligheid en zoete aardappel zwarte vlek.Industrieel fenantreen wordt verkregen door destillatie van antraceenolie verkregen uit koolteerdestillaat. Veel soorten natuurlijke producten (zoals sterolen) bevatten dit ringsysteem. Phenantreen wordt voornamelijk gebruikt bij de vervaardiging van kleurstoffen, geneesmiddelen, hoge efficiëntie en lage toxiciteit van pesticiden, en kan worden gebruikt als scintillants, rookloze poederstabilisator. Veel van de fenantreen derivaten hebben carcinogene fysiologische effecten. Zoals: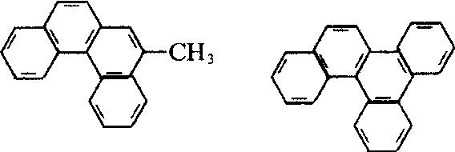
De moleculaire structuur van 2-methyl-3-benzofenantreen en 1, 2, 3, 4-dibenzofeen
chemische eigenschappen
het verschijnt als witte glans en fluorescerende vlokkristallen. Het is niet oplosbaar in water, lichtjes oplosbaar in ethanol, oplosbaar in ether, azijnzuur, benzeen, tetrachloorkoolstof en koolstofdisulfide.
gebruikt
het kan worden gebruikt voor de vervaardiging van fenantreenquinon, kunsthars, pesticiden en conserveermiddelen, enzovoort.
fenantreen kan door oxidatie fenantrenequinon geven, dat gebruikt wordt ter vervanging van de organische kwikhoudende bestrijdingsmiddelen ceresine en gallotox. Het uit de oxidatie verkregen bifenylzuur kan worden gebruikt voor de bereiding van alkydhars. Fenantreen oxidatie kan ook anhydride, cyclohexanon en fenol geven. De chloorproducten van fenantreen kunnen worden gebruikt om niet-ontvlambare elektrische isolatoren en impregneermiddelen te maken. Het gesulfoneerde fenantreen sulfonzuur kan worden gemaakt van bindmiddel, looien en ga zo maar door. Maar in feite zijn de meeste van deze toepassingen nog niet ontwikkeld. In de papierindustrie kan het fenantreen worden gebruikt als pulp antifogging agent; kan ook worden gebruikt voor nitroglycerine explosieven en nitrocellulose stabilisator en voor de vervaardiging van rookbom; het vaste oxide van fenantreen kan worden gemaakt van uitstekende vlambestendige elektrische isolerende materialen en vulstoffen. In de geneeskunde kan fenantreen worden gebruikt voor het synthetiseren van alkaloïden-morfine en cafeïne, dimethyl morfine en geneesmiddelen met speciale fysiologische effecten op veel voortplantingsorganen. In de kleurstofindustrie kan het fenantreen worden gemaakt van 2-aminophenantreen quinone, benzantrone, sulfide reduction dye (blauwe BO, zwarte BB en bruin) enzovoort. Bovendien kunnen de kunststofindustrie, synthetische looistoffen en fenantreen, onder hoge temperatuur en hoge druk, hydrogenering ondergaan om hydrofenantreen te krijgen, zijnde de brandstof van senior straalvliegtuigen.voor de bepaling van het molecuulgewicht en de synthese van organische verbindingen.
preparaat
fenantreen is een relatief hoog gehalte aan koolteer, goed voor 5% koolteer, na het naftaleengehalte. De antraceenolie in de 300-360 ℃ fractie van koolteer heeft het hoogste gehalte aan fenantreen, gevolgd door antraceen en carbazool enzovoort. De fenantreen-extractiemethode is meestal antraceenolie verzenden voor koeling, kristallisatie en vervolgens vacuümfiltratie of centrifugale scheiding voor oliescheiding. De relatief hoge hoeveelheid oplosbare fenolen in oliën kan worden teruggewonnen met behulp van een precisiedestillatiemethode. Het verkregen kristal wordt ruw antraceen genoemd, dat 25-30% antraceen, 22-25% carbazool en 30% fenantreen bevat. Ruwe antraceen kan worden onderworpen aan zware benzeen extractie, koeling, filtratie met het filtraat gestoomd uit oplosmiddel voor herkristallisatie en filtratie. Neem filtraat voor destillatie zodat we industriële fenantreen met sulfonatie kunnen krijgen om fijne fenantreen te krijgen.
chemische eigenschappen
witte kristallen
chemische eigenschappen
fenantreen is een witte kristallijne stof. Zwakke Aromatische geur. Polycyclische aromatische koolwaterstoffen (PAK ‘ s) zijn verbindingen die meerdere benzeenringen bevatten en worden ook polynucleaire aromatische koolwaterstoffen genoemd.
fysische eigenschappen
kleurloze monoclinische kristallen met een zwakke Aromatische geur
gebruikt
fenantreen is een polycyclische aromatische koolwaterstoffen, een milieuverontreinigende stof.
gebruikt
gelabelde polycyclische aromatische koolwaterstoffen als microverontreinigingen.
definitie
ChEBI: Een polycyclische aromatische koolwaterstof bestaande uit drie gefuseerde benzeenringen, die zijn naam ontleent aan de twee termen “fenyl” en “antraceen”.”
productiemethoden
fenantreen komt voor in koolteer en kan worden geïsoleerd uit verschillende soorten ruwe aardolie.
Synthesis Reference(s)
Journal of Heterocyclic Chemistry, 30, p. 291, 1993 DOI: 10.1002/jhet.5570300151
The Journal of Organic Chemistry, 18, p. 801, 1953 DOI: 10.1021 / jo50013a004
Tetrahedron Letters, 15, p. 495, 1974
General Description
Colorless monoclinic crystals with a faint aromatic geur. Oplossingen vertonen een blauwe fluorescentie.
lucht & Waterreacties
onoplosbaar in water.
Reactiviteitsprofiel
fenantreen kan reageren met oxiderende materialen .
gezondheidsrisico
de acute orale toxiciteit van fenantreen is low.It is giftiger dan antraceen. Een orale LD50-waarde bij muizen wordt gemeld bij 700 mg / kg. Het kan een tumor in de huid veroorzaken op de plaats van toediening.Er zijn echter onvoldoende aanwijzingen voor carcinogeniteit bij dieren.
brandgevaar
fenantreen is brandbaar.
veiligheidsprofiel
Gif via intraveneuze route. Matig giftig bij inname. Mutatiegegevens gerapporteerd. Een menselijke huid fotosensitizer. Twijfelachtig carcinogeen met experimentele neoplastigeen en tumorigenische gegevens door huidcontact. Brandbaar wanneer blootgesteld aan hitte of vlam; kan krachtig reageren met oxiderende materialen. Om brand te bestrijden, gebruik water, schuim, CO2, droge chemische stof. Bij verhitting om te ontbinden stoot het scherpe rook uit en irriterende dampen
potentiële blootstelling
stof kan een explosief mengsel met lucht vormen. Onverenigbaar met oxidatiemiddelen (chloraten, nitraten, peroxiden, permanganaten, perchloraten, chloor, broom, fluor, enz.); contact kan branden of explosies veroorzaken. Blijf weg van alkalische materialen, Sterke basen, sterke zuren, oxozuren, epoxiden.
carcinogeniteit
fenantreen is niet effectief als initiator. Het is Niet classificeerbaar voor carcinogeniteit bij de mens—klasse 3 volgens IARC en klasse D volgens IRIS, gebaseerd op geen gegevens bij de mens en onvoldoende gegevens uit één enkele studie bij ratten en huidverf-en injectiestudies inmice.
bron
aangetroffen in grondwater onder een voormalige vergassingsinstallatie in Seattle, WA bij een concentratie van 130 µg / L (ASTR, 1995). Gedetecteerd in 8 dieselbrandstoffen bij concentraties variërend van 0,17-110 mg / L met een gemiddelde waarde van 41,43 mg/L (Westerholm en Li, 1994) en in in gedestilleerd water oplosbare fracties van nieuwe en gebruikte motorolie bij concentraties van respectievelijk 1,9-2,1 en 2,1–2,2 µg / L (Chen et al., 1994). Lee et al. (1992) rapporteerde concentratiebereiken van respectievelijk 100 tot 300 mg/L en 15 tot 25 µg/L in dieselbrandstof en de overeenkomstige waterfase (gedestilleerd water). Schauer et al. (1999) melding gemaakt van fenantreen in dieselbrandstof met een concentratie van 57µg/g en in uitlaat van een dieselmotor voor middelzware vrachtwagens met een emissie van 93,1 µg/km.Vastgesteld in ruwe olie uit Koeweit en Zuid-Louisiana in concentraties van respectievelijk 26 en 70 ppm (Pancirov en Brown, 1975). Dieselbrandstof uit een tankstation in Schlieren, Zwitserland, bevat fenantreen in een geschatte concentratie van 327 mg / L (Schluep et al.,2001).in asfaltdampen werd fenantreen aangetroffen bij een gemiddelde concentratie van 57,73 ng / m3 (Wanget al., 2001).Thomas and Delfino (1991) equilibrated contaminant-free groundwater collected fromGainesville, FL with individual fractions of three individual petroleum products at 24-25 °C for24 h. The watery phase were analysed for organic compounds Through US EPA approved test method625. Fenantreen werd alleen gedetecteerd in de in water oplosbare fractie van dieselbrandstof bij een gemiddelde concentratie van 17 µg/L. op basis van laboratoriumanalyse van 7 koolteermonsters varieerden de fenantreen-concentraties van3.100 tot 35.000 ppm (EPRI, 1990). Gedetecteerd in 1 jaar oude koolteerfilm en bulkkoolteer bij een identieke concentratie van 10.000 mg/kg (Nelson et al., 1996). Een hogetemperatuurkoolteer bevatte fenantreen met een gemiddelde concentratie van 2,66 gew. % (McNeil, 1983). Ook in hogetemperatuurkoolteerputten bij concentraties variërend van 7.500 tot 40.300 mg/kg worden geïdentificeerd (Arrendale en Rogers, 1981). Lee et al. (1992a) acht koolteer in evenwicht gebracht met gedestilleerd water bij 25 °C. De maximale concentratie fenantreen in de waterfase is 0,4 mg/l.negen in de handel verkrijgbare creosootmonsters bevatten fenantreen bij concentraties van 48.000 tot 120.000 mg / kg (Kohler et al., 2000).de typische concentratie van fenantreen in een zware pyrolyseolie is 2,5 wt % (Chevron Phillips, mei 2003).
lot in het milieu
biologisch. Catechol is de centrale metaboliet in de bacteriële afbraak van fenantreen.Tussenproducten zijn onder meer 1-hydroxy-2-naftoëzuur, 1,2-dihydroxynaftaleen en salicylzuur (Chapman, 1972; Hou, 1982). Er werd gemeld dat Beijerinckia, onder aerobicomstandigheden, fenantreen afbrak tot cis-3,4-dihydroxy-3,4-dihydrofenantraceen (Kobayashiand Rittman, 1982).
bodem. De gerapporteerde halfwaardetijden voor fenantreen in een Kidman sandy leem en McLaurin sandyloam zijn respectievelijk 16 en 35 d (Park et al., 1990). Manilal en Alexander (1991) rapporteerden eenhalf-leven van 11 d in een Kendaia bodem.
oppervlaktewater. In een 5 m diep oppervlaktewaterlichaam waren de berekende halfwaardetijden voor directe fotochemische omzetting op 40 °noorderbreedte in de midzomer gedurende de middag respectievelijk 59 en 69 d met en zonder sediment-waterpartitionering (Zepp en Schlotzhauer, 1979).
Fotolytisch. Een kooldioxideopbrengst van 24,2% werd bereikt wanneer het geadsorbeerde fenantreen onsilica gel gedurende 17 uur met licht (λ >290 nm) werd bestraald (Freitag et al., 1985). In een 2-WK-experiment gaf fenantreen toegepast op bodem-water suspensies onder aërobe en anaerobische omstandigheden 14CO2 opbrengsten van 7,2 en 6.3%, respectievelijk (Scheunert et al ., 1987). Matsuzawa etal. (2001) onderzocht de fotochemische degradatie van vijf polycyclische aromatische koolwaterstoffen indiesel fijn stof afgezet op de grond en in verschillende bodemcomponenten. De fotochemische degradatie door kunstmatig zonlicht werd bereikt met behulp van een 900-W xenonlamp.Het licht van deze lamp werd door een glasfilter geleid om licht van kortere golflengten (λ2) te elimineren. Bovendien werd een zonnesimulator met een 300W xenonlamp gebruikt om de maximale zonlicht-intensiteit te leveren die in Tokio wordt waargenomen (35,5 °noorderbreedte). De halfwaardetijden van fenantreen in dieseldeeltjes met 900-en 300-W-bronnen waren respectievelijk 4,29 en 60,63 uur. De volgende halfwaardetijden werden vastgesteld voor fenantreen dat aan verschillende bodemcomponenten werd geadsorbeerd met behulp van apparatuur van 900 W: 3,04 uur voor kwarts,2,90 uur voor veldspaat, 1,15 uur voor kaoliniet, 4,97 uur voor montmorilloniet, 3,26 uur voor silicagel en 1,17 uur voor aluminiumoxide.
chemisch / fysisch. De waterige chlorering van fenantreen bij pH 8,8), fenantreen-9,10-oxide, fenantreen-9,10-Dion en 9,10-dihydrofenantrenediol werden geïdentificeerd als belangrijke producten (Oyler et al.,1983). Er werd gesuggereerd dat de chlorering van fenantreen in leidingwater verantwoordelijk was voor de aanwezigheid van chloor – en dichloorfenantreen (Shiraishi et al., 1985).
scheepvaart
UN3077 milieugevaarlijke stoffen, vast, N.O.s., gevarenklasse: 9; etiketten: 9-diverse gevaarlijke stoffen, technische naam vereist.
zuiveringsmethoden
mogelijke contaminanten zijn antraceen, carbazool, fluoreen en andere polycyclische koolwaterstoffen. Zuiver het door destillatie uit natrium onder vacuüm, kokend met maleïnezuuranhydride in xyleen, kristallisatie uit azijnzuur, sublimatie en zonesmelting. Het is ook herhaaldelijk opnieuw gekristalliseerd uit EtOH, * benzeen of pet-ether (B 60-70o), waarna het onder vacuüm boven P2O5 in een abderhalden-pistool is gedroogd. Feldman, Pantages en Orchin scheidden het grootste deel van de antraceenonzuiverheid door fenantreen (671g) met maleïnezuuranhydride (194g) in xyleen (1,25 L) gedurende 22 uur onder stikstof terug te voeren en vervolgens te filteren. Het filtraat werd geëxtraheerd met 10% NaOH in water, de organische fase werd gescheiden en het oplosmiddel werd verdampt. Het residu werd na 2 uur roeren met 7 g natrium in een vacuüm gedestilleerd en vervolgens tweemaal geherkristalliseerd uit 30% * benzeen in EtOH. Vervolgens werd het opgelost in heet azijnzuur (2,2 mL / g) en werd er langzaam een waterige oplossing van CrO3 (60 g in 72 ml H2O plus 2,2 L azijnzuur) aan toegevoegd, gevolgd door langzame toevoeging van conc H2SO4 (30 ml). Het mengsel werd 15 minuten lang teruggespoeld, verdund met een gelijk volume water en afgekoeld. Het neerslag werd afgefilterd, met water gewassen, gedroogd en gedestilleerd en vervolgens tweemaal opnieuw gekristalliseerd uit EtOH. Verdere zuivering is mogelijk door chromatografie van een CHCl3-oplossing op geactiveerde aluminiumoxide, met *benzeen als eluent, en door zoneraffinage. De picraat (1:1) vormt goudgele naalden met m 146o, en de styphnaat (1:1) heeft m 138-139o (platen of naalden van EtOH of EtOH/H2o respectievelijk).
afvalverwijdering
Raadpleeg de regelgevende instanties voor het milieu voor richtsnoeren over aanvaardbare verwijderingspraktijken. Producenten van afval dat deze verontreinigende stof bevat (≥100 kg/mnd) moeten voldoen aan de EPA-voorschriften voor opslag, transport, verwerking en afvalverwerking.