Patofysiologia / International Osteoporosis Foundation
hormonit ovat mahdollisesti ratkaisevimpia luunmuodostuksen modulaattoreita. On hyvin todettu, että estrogeeni Lindsay, R., ehkäisy ja osteoporoosin hoito. Lancet, 1993. 341 (8848): s. 801-5.
. lisäkilpirauhashormoni huulet, P., D-Vitamiinifysiologia. Prog Biophys Mol Biol, 2006. 92 (1): S. 4-8
. ja vähäisemmässä määrin testosteroni suoraan tai epäsuorasti estrogeeniseeman, E., rakenteellisen perustan luun hauraus miehillä. Bone, 1999. 25(1): s. 143-7.
Van Pottelbergh, I., et al., Häiriintynyt sukupuoli steroidi asema miehillä, joilla on idiopaattinen osteoporoosi ja heidän poikansa. J Clin Endocrinol Metab, 2004. 89(10): s. 4949-53.
. ovat välttämättömiä optimaaliselle luun kehitykselle ja ylläpidolle. Näistä estrogeenin uskotaan nyt olevan suorin vaikutus luusoluihin, vuorovaikutuksessa spesifisten proteiinien tai reseptorien kanssa osteoblastien ja osteoklastien pinnalla Zallone, A., suorat ja epäsuorat estrogeenin vaikutukset osteoblasteihin ja osteoklasteihin. Ann N Y Acad Sci, 2006. 1068: s.173-9
.
tämä interaktio käynnistää monimutkaisen tapahtumaketjun soluissa, mikä lisää osteoblastin aktiivisuutta ja häiritsee samalla osteoblasti-osteoklasti – viestintää-yksi luun uudelleenmuodostuksen ironioista on se, että osteoblastit vapauttavat osteoklasteja stimuloivia ja luun resorptiota edistäviä tekijöitä, kuten jäljempänä nähdään.
Estrogeenivaikutukset välittyvät yhden tietyntyyppisen solun pintareseptorin eli estrogeenireseptorin alfan (ERa) kautta, joka sitoo ja kuljettaa hormonin solun tumaan, jossa reseptorihormonikompleksi toimii kytkimenä tiettyjen geenien päälle. Era-reseptoreita löytyy osteoblastien pinnalta, samoin estrogeenireseptoreihin liittyvää reseptorialfaa (ERRa), jolla voi olla avustava rooli luusolujen säätelyssä Bonnelye, E. ja J. E. Aubin, estrogeenireseptoreihin liittyvä reseptorialfa: estrogeenivasteen välittäjäaine luussa. J Clin Endocrinol Metab, 2005. 90(5): s. 3115-21.
. Viimeaikaiset tutkimukset viittaavat myös siihen, että sukupuolihormoneja sitova globuliini (SHBG), joka helpottaa estrogeenin pääsyä soluihin, voi myös olla tukiroolissa Goderie-Plomp, H. W., et al., Endogeeniset sukupuolihormonit, sukupuolihormoneja sitova globuliini ja nikamamurtumien riski iäkkäillä miehillä ja naisilla: Rotterdam-tutkimus. J Clin Endocrinol Metab, 2004. 89(7): s. 3261-9.
.
estrogeenia tietenkin valmistetaan ja erittyy verenkiertoon jonkin matkan päässä luusta, ja sillä on myös syvällisiä vaikutuksia muihin kudoksiin, kuten kohtuun ja rintaan. Mutta on muitakin paikallisesti tuotettuja merkinantomolekyylejä, joilla on syvällinen vaikutus luuston fysiologiaan.

Sytokiinituotanto estrogeenin kontrollissa luun ja luun uudistamisessa.
Figure taken from Ferrari & Roux, 2019 Pocket Reference to Osteoporosis, S. Ferrari, Roux, C., Editor 2019, Springer International Publishing.
.
Prostaglandins, particularly prostaglandin E2 (PGE2), stimulate both resorption and formation of bone Pilbeam, C.C., J.R. Harrison, and L.G. Raisz, Chapter 54 – Prostaglandins and Bone Metabolism, in Principles of Bone Biology (Second Edition), J.P. Bilezikian, L.G. Raisz, and G.A. Rodan, Editors. 2002, Academic Press: San Diego. p. 979-994
. PGE2 on lipidi, jota muodostuu eri luusoluissa esiasteesta nimeltä arakidonihappo. PGE2-synteesin ensimmäisen vaiheen suorittaa syklo-oksigenaasi 2 (COX2)-niminen entsyymi, ja tämän entsyymin inhibiittorit voivat estää luun muodostumista vasteena eläinten mekaaniselle rasitukselle Forwood, M. R., indusoituva syklo-oksigenaasi (COX-2) välittää luun muodostumisen induktiota mekaanisella kuormituksella in vivo. J Bone Miner Res, 1996. 11(11): s. 1688-93.
. PGE2 voi olla tarpeen liikunnan aiheuttaman luunmuodostuksen vuoksi.
on näyttöä siitä, että murtumariski on suurentunut potilailla, jotka käyttävät ei-steroidisia tulehduskipulääkkeitä, jotka inhiboivat COX-2 Carbone, L. D., et al., Luun mineraalitiheyden ja ei-steroidisten tulehduskipulääkkeiden ja aspiriinin käytön välinen yhteys: syklo-oksigenaasin selektiivisyyden vaikutus. J Bone Miner Res, 2003. 18(10): s. 1795-802
saattaa myös kasvaa. Toinen joukko lipidimolekyylejä, jotka näyttävät säätelevän luun remodelling ovat leukotrieenit. Myös arakidonihaposta johdettujen näiden on todettu vähentävän luun tiheyttä hiirillä Traianedes, K., et al., 5-Lipoksigenaasin metaboliitit estävät luun muodostumista in vitro. Endokrinologia, 1998. 139 (7): s. 3178-84.
.
näiden hormonien vaikutus luun uudelleenmuodostukseen riippuu siitä, miten ne muuttavat osteoklastien ja / tai osteoblastien aktiivisuutta. Erityiset solun pintareseptorit auttavat siirtämään luusolujen ulkopuolelta tulevia signaaleja solun tumaan, jossa eri solujen toimintaa säätelevät geenit voidaan kytkeä päälle tai pois päältä. Näitä ovat reseptorit luun morfogeneettisten proteiinien (BMPs) perheen proteiineja, jotka ovat voimakkaita induktorit luun muodostumista.
BMP-reseptoreita on löydetty osteoblastien esiastesolujen Mbalaviele, G., ym.pinnalta., Beetakateniini ja BMP-2-synergia edistävät osteoblastien erilaistumista ja uuden luun muodostumista. J Cell Biochem, 2005. 94(2): s. 403-18.
. Toinen solun pinnan reseptori kutsutaan low-density lipoprotein (LDL) liittyvä proteiini 5 reseptori (LRP5), Wnt reseptori, voi myös olla tärkeä luun muodostumista, koska menetys lrp5 eläimillä johtaa vaikea osteoporoosi Gong, Y., et al., LDL-reseptoriin liittyvä proteiini 5 (LRP5) vaikuttaa luun kertymiseen ja silmien kehitykseen. Cell, 2001. 107(4): s. 513-23.
. BMP-reseptorit ja LRP5 voivat toimia yhdessä osteoblastien stimuloimiseksi, mutta sitä, miten tämä tarkalleen ottaen tapahtuu, ei ole selvitetty.
sklerostiini, joka on Sost-geenin tuote ja jota osteosyytit ilmentävät, sitoutuu osteoblastien lrp5 / 6-reseptoriin ja estää Wnt-signalointia, mikä johtaa luun muodostumisen vähenemiseen bonewald, L. F., hämmästyttävä osteosyytti. J Bone Miner Res, 2011. 26(2): s. 229-38.
Li, X., et al., Sklerostiini sitoutuu LRP5/6: een ja estää kanonisen Wnt-signaloinnin. J Biol Chem, 2005. 280(20): s. 19883-7.
. Lisäkilpirauhashormoni (PTH)ja mekaaninen kuormitus vähentävät sklerostiinin eritystä esteosyyteissä Bellido, T., et al., Lisäkilpirauhashormonin krooninen nousu hiirillä vähentää sklerostiinin ilmentymistä osteosyyteissä: Uusi mekanismi osteoblastogeneesin hormonaaliseen säätelyyn.Endokrinologia, 2005. 146(11): s. 4577-83.
Robling, A. G., et al., Luun mekaaninen stimulaatio in vivo vähentää sostin/sklerostiinin osteosyyttien ilmentymistä. J Biol Chem, 2008. 283 (9): s. 5866-75.
. Sklerostiinia vastaan on kehitetty vasta-aine potentiaalisena lääkkeenä, jolla on voimakkaita luun lujuuteen vaikuttavia ominaisuuksia. Read more on anabolics as treatments.

Figure taken from Ferrari & Roux, 2019 Pocket Reference to Osteoporosis, S. Ferrari, Roux, C., Editor 2019, Springer International Publishing.
.
solun pintareseptori nimeltä RANK (nfkb: n reseptorin aktivaattoriksi) tuottaa osteoklastien esiastesoluja kehittymään täysin erilaistuneiksi osteoklasteiksi, kun rank aktivoituu sen konjakkikumppanin RANK ligandin (RANKL) Yasuda, H., et al., Osteoklastien erilaistumistekijä on osteoprotegeriinin/osteoklastogeneesiä estävän tekijän ligandi ja on identtinen TRANCE / RANKL: n kanssa. Proc Natl Acad Sci U S A, 1998. 95(7): s. 3597-602.
Lacey, D. L., et al., Osteoprotegerin ligandi on sytokiini, joka säätelee osteoklastien erilaistumista ja aktivaatiota. Cell, 1998. 93(2): s. 165-76.
.
RANKL on itse asiassa osteoblastien tuottama ja yksi ehkä monista merkinantomolekyyleistä, jotka helpottavat ristikeskustelua osteoblastien ja osteoklastien välillä ja auttavat koordinoimaan luun remodelling Theill, L. E., W. J. Boyle, ja J. M. Penninger, RANK-L ja RANK: T-solut, luukato ja nisäkkäiden evoluutio. Annu Rev. Immunol, 2002. 20: s. 795-823.
. Osteoprotegeriini, toinen osteoblastien Suda, T., et al.vapauttama proteiini, Tuumorinekroositekijän reseptorin ja ligandiperheiden uusien jäsenten osteoklastien erilaistumisen ja toiminnan Mukauttaminen. Endocr Rev. 1999. 20(3): s. 345-57.
, voi myös sitoutua RANKLIIN, toimien houkutuslintuna estääkseen rankin ja RANKLIN yhteyden. RANKL/osteoprotegeriinin tasapaino voi olla ratkaiseva osteoporoosissa. Itse asiassa eläinkokeet osoittivat, että osteoprotegeriinin lisääntynyt tuotanto johtaa luumassan lisääntymiseen, kun taas proteiinin menetys johtaa osteoporoosiin ja lisääntyneisiin murtumiin Bucay, N., et al., osteoprotegeriinipuutteisille hiirille kehittyy varhain alkava osteoporoosi ja valtimoiden kalkkeutuminen. Genes Dev, 1998. 12(9): s. 1260-8.
. RANKL: n estäjät ovat myös osoittautuneet lupaaviksi mahdollisiksi osteoporoosin hoitomuodoiksi ihmisillä.
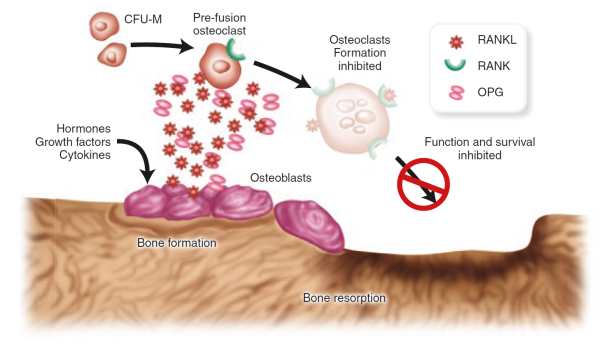
Figure taken from Ferrari & Roux, 2019 Pocket Reference to Osteoporosis, S. Ferrari, Roux, C., Editor 2019, Springer International Publishing.
.
viime vuosina löydettiin myös toinen, komplementaarinen solumerkkijärjestelmä, joka edistää osteoklastien muodostumista ja aktivoitumista. Dnax-aktivoivan proteiinin 12 (DAP12) ja Fc – reseptorin yhteisen γ – ketjun (fcry), kahden solun pintareseptorin puuttuessa hiirille kehittyy vaikea osteoporoosi-osteoporoosin täydellinen vastakohta-jolle on ominaista luun tiheyden dramaattinen kasvu Mocsai, A., et al., Immunomodulatoriset adapteriproteiinit DAP12 ja Fc-reseptorin gammaketju (FcRgamma) säätelevät funktionaalisten osteoklastien kehittymistä Syk-tyrosiinikinaasin kautta. Proc Natl Acad Sci U S A, 2004. 101(16): s. 6158-63.
Koga, T., et al., Itam-Motifin välittämät kustannussignaalit toimivat yhdessä RANKL: n kanssa luun homeostaasissa. Luonto, 2004. 428 (6984): s. 758-63.
. Nämä kaksi solun pintareseptoria vuorovaikuttavat solussa olevien proteiinien kanssa, joita kutsutaan nimellä ITAM (immunoreceptor tyrosiini-based activation motif) adapteriproteiinien kanssa aiheuttaen solunsisäisen kalsiumin lisääntymistä.
tutkimukset viittaavat siihen, että RANK / RANKL ja ITAM-välitteiset reitit indusoivat yhdessä täyden osteoklastien aktiivisuuden. Nämä kaksi reittiä voivat yhtyä aktivoidakseen proteiinin, jota kutsutaan aktivoitujen T-solujen ydintekijäksi (nfat) c1. NFATc1 toimii pääkytkimenä luun resorptiolle, koska se kytkee geenit, joita osteoklastien esiastesolut tarvitsevat tullakseen täysin aktiivisiksi osteoklasteiksi Takayanagi, H., mekanistinen näkemys osteoklastien erilaistumisesta osteoimmunologiassa. J Mol Med (Berlin), 2005. 83(3): s. 170-9.
.