rajat sydän-ja verisuonitaudeissa
Johdanto
tutkittaessa koordinaattijärjestelmiä, joita voitaisiin käyttää eri biologisille yksiköille, olisi otettava huomioon erityisominaisuudet. Esimerkiksi kromosomiluku ja emäsparin sijainti muodostavat lineaarisen koordinaatiston, joka riittää määrittämään sijainnin vertailugenomissa (1). Kuitenkin, koordinaattijärjestelmä koko ihmiskehon, joka voi palvella tarpeita HuBMAP, HCA, HPA, ja muut kartoitus ponnisteluja, on paljon monimutkaisempi useista syistä (2-5). Ensinnäkin solut elävät kolmessa ulottuvuudessa, ja lisätietoja tarvitaan kuvaamaan minkä tahansa kudosnäytteen kokoa ja rotaatiosuuntausta, jota käytetään tietojen tuottamiseen. Toiseksi, vaikka genomin emäsparin sijainti ei riipu siitä, miten DNA taittuu ja pakataan tumaan, yksittäisten alkuaineiden sijainnit (esim., solut, elimet) kehossa ovat dynaamisia, koska ne voivat muuttua luuston ja lihasten liikkeiden, painovoiman, hengityksen, sydämen sykkeen ja muiden kudosta vääristävien toimintojen ja voimien myötä. Kolmanneksi, vaikka DNA: n vaihtelu ihmisten välillä on <1%, ihmisen kehon geometria kattaa laajan valikoiman korkeuksia, painoja ja muotoja, jotka vaihtelevat sukupuolen ja rodun mukaan ja muuttuvat merkittävästi ihmisen eliniän aikana.
yksi vaihtoehto on käyttää 3D-Karteesista koordinaatistoa kuvaamaan sijaintia kappaleen sisällä. Karteesisten koordinaattijärjestelmien etuna on se, että ne ovat tuttuja ja helposti ymmärrettäviä. Ruumiin ollessa tavanomaisessa anatomisessa asennossa vasen-oikea, kaudaalinen-kallo ja posterior-anterior muodostavat kolme kohtisuoraa (x-y-z) akselia. Pienemmän mittakaavan analyyseissä alkuperän keskittäminen anatomiseen maamerkkiin voisi olla hyödyllisintä ja mahdollisesti vähemmän vaihteleva eri ihmisten välillä. Esimerkiksi kudosnäytteen etäisyys munuaisesta munuaisen ylempään napaan olisi helpompi mitata kuin ihmisen päälaelle. Karteesisten koordinaattien haittana on, että sen akselit eivät noudata kappaleen luonnollista muotoa. Tämän seurauksena vertailukehokartan luominen digitaalisesti ”ompelemalla” yhteen kudosnäytteitä, jotka on kerätty erikokoisilta ihmisiltä, vaatisi monimutkaisen prosessin, jossa tiedot vääristyvät, pyörivät ja kohdistetaan yhteen. Tämän tekeminen siten, että skaalautuu koko kehoon säilyttäen samalla solutason tarkkuuden, olisi erittäin haastavaa.
muita 3D-koordinaattijärjestelmiä on kehitetty eri sovelluksiin. Esimerkiksi pallokoordinaatit, joiden akselit edustavat leveyttä, pituutta ja korkeutta, kuvaavat sopivasti sijaintia maan pinnalla. Yksinkertainen polku pallomaisissa koordinaateissa, kuten ”1 km itään”, on paljon vaikeampi kommunikoida Karteesisilla koordinaateilla. Samoin ihmiskehon koordinaattijärjestelmissä olisi ihanteellisesti oltava akselit, jotka noudattavat anatomisia rakenteita, geneettisiä ilmentymäkuvioita, kemiallisia kaltevuuksia ja/tai muita biologisesti merkityksellisiä reittejä. On kehitetty useita elinkohtaisia koordinaattijärjestelmiä, kuten talairachin koordinaatit funktionaalista aivokuvausta varten, mutta nämä eivät ulotu koko kehoon (6).
Vascular Based Coordinate System
vuonna 2017 National Institutes of Health, Broad Institute, Sanger Institute ja Chan Zuckerberg Initiative järjestivät yhteisen Koordinaattikehyksen (CCF). Osallistujat, joihin kuului anatomeja, patologeja, kliinikoita ja tekniikan asiantuntijoita eri puolilta maailmaa, ehdottivat useita lähestymistapoja ihmisruumiin solujen kartoittamiseksi, mukaan lukien anatomiset koordinaattijärjestelmät (7). Yksi näistä, joka käyttää verisuonitus, keskusteltiin edelleen 2019 CCF Workshop, erityisesti paikallistamiseen munuaissolujen (8). Tässä käsikirjoituksessa esitämme käsitteellisen yleiskuvan tästä vaskulaarisesta koordinaatistosta ja kuvailemme sen hyötyjä ja rajoituksia (Kuva 1).
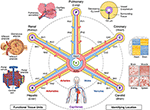
kuva 1. Verisuonikoordinaatiston napa-ja puolirakenne. Verisuonikoordinaatisto koostuu edustavista astiasilmukoista, jotka alkavat ja päättyvät sydämen kammioihin ja ulottuvat kunkin elimen toiminnallisiin yksiköihin (vastapäivään vasemmalta yläpuolelta: keuhkorakkulat, glomerulukset ja maksan lobulit). Solun ” osoite ”sisältää silmukan nimen (esim.” R ”munuaisten ja” H ”maksan osalta) ja lähimmän astian haaroittumistason (esim.” RA1 ” munuaispiirin afferenttien arteriolien osalta). Huomaa, että sydämen seinät ovat pitkin sepelvaltimon (”C”) verisuonisilmukkaa, ja joidenkin sydämen sisäisten rakenteiden solut ovat todellisuudessa sijoitettuna koordinaatiston kehälle, lähelle hiussuonia, joista ne saavat verta. On olemassa useita tapoja paikantaa vieläkin tarkempi ”GPS-kaltainen” sijainti, mukaan lukien, kulkee myötäpäivään yläoikealla, ”hypoksia sormenjälki”, joka johtuu laskemalla happipitoisuus kauempana aluksen, ainutlaatuinen” histologinen sormenjälki ”ja” geeniekspressio sormenjälki ”eri verisuonten endoteelisoluissa, ja erottuva” verisuonten arkkitehtuuri sormenjälki ” löytyy eri kudostyypeissä. Verisuonitus ulottuu kaikkiin kehon osiin (pohjaan) ja kehystää kaikkia elimiä kaikilla asteikoilla. lähdetiedosto: Kuvia maksalohkoista, glomeruleista, keuhkorakkuloista, geeniekspression lämpökartasta ja koko kehon verisuonistosta on muokattu Wikimedia Commonsista: https://commons.wikimedia.org/wiki/File:2423_Microscopic_Anatomy_of_Liver.jpg (Public Domain); https://commons.wikimedia.org/wiki/File:Juxtaglomerular_Apparatus_and_Glomerulus.jpg (CC BY 3.0 license); https://commons.wikimedia.org/wiki/File:Alveolus_diagram.svg (Public Domain); https://commons.wikimedia.org/wiki/File:Iris_dendrogram.png (CC BY-SA 4.0-lisenssi); ja, https://commons.wikimedia.org/wiki/File:Circulatory_System_en.svg (Public Domain). Gene expression heat map luotu Guo et al. (9) käyttämällä simuloitua dataa. Vascular architecture perustuu Bosetti et al. (10) (cc by 4.0-lisenssi).
verisuonikoordinaatiston tavoitteena ei ole rakentaa verisuonikarttaa. Sen sijaan ideana on käyttää kehon läpi kulkevia tunnettuja verisuonireittejä akselina koordinaatistossa, joka voi kuvata anatomisten elementtien, kuten solujen, sijaintia verisuonistoa ympäröivässä kudoksessa. Tässä ehdotetussa kehyksessä sydämen kammioita voidaan pitää koko kehon kartan alkuperänä. Verisuoniakseli sisältää verisuonten silmukoita (verrattavissa ”tiet” Google Map metafora), jotka ulottuvat läpi aortan tai keuhkovaltimon, vähitellen kartio pois yhden solun kokoon, kun ne lähestyvät joka toinen solu jokaisessa elimessä kehossa, ja palata sydämeen. Näitä reittejä pitkin verisuonitus seuraa eri elinten ja kudosten ainutlaatuista biologiaa; samoin kehon elimet ja kudokset eivät voisi olla olemassa ilman niiden tiiviisti integroituneen verisuonituksen ainutlaatuisia ominaisuuksia.
aivan kuten genomikartta avaa DNA: n lineaariseksi sekvenssiksi, voimme kuvitella avautuvamme vaskulatuuriakselin monimutkaiset 3D-käänteet yksinkertaisempaan 2D-muotoon, jossa sydämen kammiot ovat keskellä. Tämä verisuoniston kaavamainen esitys helpottaa (1) kehon sijainnin kuvaamista; (2) verisuonten reittien suuntaamista vaihtelevalla 3D-muodolla, mutta eri ihmisten vastaavilla toiminnoilla; (3)tunnistaa malleja, kuten solutyypin muutoksia ja geeniekspressiota, yhtenä siirtymänä suuremmista pienempiin verisuoniin elimen sisällä (pitkin Puolaa); ja (4) vertaa samalla tasolla olevia kudoksia (esim.kapillaareja) eri elimissä (pinnoissa).
elimellä, kuten munuaisella, on kymmeniä tuhansia verisuonireittejä, jos jokaista hiussuonta tarkastellaan selvästi. Jotta CCF: n rakentaminen olisi kuitenkin mahdollista, teemme vielä yksinkertaistavan olettamuksen, jonka mukaan monia näistä poluista ei voi erottaa toisistaan. Erityisesti pienimmät verisuonet (hiussuonet) ovat jokaisen elimen pienten erikoistuneiden toiminnallisten yksiköiden keskellä (esim., maksan lobules maksassa, glomerulukset munuaisissa ja keuhkorakkuloissa). Kokonainen elin vaatii monia näistä verisuonikeskeisistä toiminnallisista yksiköistä, jotka ovat anatomisesti ja fysiologisesti samanlaisia (11). Tämän samankaltaisuuden avulla voidaan romahduttaa lukuisia verisuonireittejä muutamaksi edustavaksi (kuva 2). Tulevaisuudessa, kun opimme lisää näiden reittien biomolekulaarisista profiileista, voimme jalostaa CCF: ää jakamalla reitit mihin tahansa löydettäviin alatyyppeihin.

kuva 2. Munuaisten verisuonireitin avautuminen alas yksisolutasolle. Edustava verisuonireitti tulee munuaiseen munuaisvaltimon kautta, kulkee glomeruluksen läpi ja palaa ulos munuaislaskimosta. Makroskooppisessa (vasemmalla) ja mesoskaalassa (keskellä) keltaisissa laatikoissa olevat etiketit ovat anatomisia rakenteita, jotka vastaavat tämän silmukan eri astioita. Mikroskoopissa (oikealla) keltaisten laatikoiden etiketit ovat erityyppisiä soluja, jotka ovat lyhyen matkan päässä läheisestä glomerulusastiasta. Yksittäisten solujen sijainti voidaan kuvata lähimmän aluksen osoitteen (esim., ”RA0 ”glomerulus-kapillaarille), etäisyys mikrometreinä tai solujen lukumääränä astian endoteelista ja kulma kohtisuorassa astian pituuteen nähden (esim.” RA0-10 µm-135° ”tai”RA0-1C-135°”). Äärioikealla jokainen astia ja sitä ympäröivä kudos on poimittu alkuperäisestä kuvasta ja kohdistettu pystysuoraan, jotta on helppo nähdä, miten solutyypit ja jakautuminen muuttuvat verisuonireittiä pitkin. Tässä esimerkissä myös linjakuvia on kierretty niin, että glomeruluksen keskusta on aina oikealla. lähdetiedosto: Kuvia munuaisesta ja glomeruluksesta on muokattu Wikimedia Commonsista: https://commons.wikimedia.org/wiki/File:KidneyStructures_PioM.svg (CC BY 3.0-lisenssi); ja, https://commons.wikimedia.org/wiki/File:Renal_corpuscle-en.svg (CC BY-SA 4.0-lisenssi).
yksittäisen solun ”osoitteessa” verisuonikoordinaatistossa on neljä komponenttia. (1) Ensimmäinen on lähin anatomisesti nimetty astia, joka tarkimmin tunnistaa verisuonisilmukan (verisuonialueen eli ”vedenjakajan”), kuten oikean munuaisvaltimon. (2) Seuraava komponentti edustaa aluksen haarautumistasoa. Munuaisissa, esimerkkejä proksimaalista distaaliseen ovat interlobar valtimot, aivokuoren säteisvaltimot, afferent arteriolit, ja glomerulus kapillaareja. Haarautumistaso voidaan määritellä myös numeerisesti, jolloin hiussuonet ovat nollatasolla ja korkeammat tasot suuremmilla luvuilla. (3) kolmas komponentti on kohtisuora etäisyys mikrometreinä tai solujen lukumääränä astian endoteelikerroksesta. (4) valinnainen neljäs komponentti voisi olla pyörimiskulma, joka on kohtisuorassa aluksen pituuteen nähden. Nolla astetta voidaan määritellä monin tavoin sovelluksesta riippuen. Se voi olla esimerkiksi suhteessa kudosnäytteen merkkiaineeseen tai se voi osoittaa kohti anatomista rakennetta, kuten munuaisen lähimmän glomeruluksen keskusta. Näiden komponenttien hyödyllisyys ja tarve olisi vahvistettava kokeellisella testauksella.
toinen lähestymistapa on käyttää endoteelisoluja ”ankkurointisoluina” muiden solujen suhteellisten sijaintien tunnistamiseen GPS: n kaltaisella tavalla. Endoteeli johtaa koko verisuonistoa. Verisuoniston eri osissa esiintyy erillisiä endoteelisolutyyppejä (EC), jotka voidaan havaita histologisesti solun yksilöllisten ominaisuuksien ja viereisten solujen avulla (”histologinen sormenjälki”) sekä analysoimalla niiden erityisiä geeniprofiileja (”geeniekspression sormenjälki”, kuva 1 lämpökartta) (9, 12, 13). Verisuonten organisaatiomalli, haaroittuva monimutkaisuus, halkaisija jne. tarjoa muita tunnistettavia ominaisuuksia, jotka muodostavat kullekin kudokselle” verisuoniarkkitehtuurin sormenjäljen ” (kuva 1 vääräväriset fluoresoivat verisuonikuvat) (10, 14). Jokaisella kudoksella on erityiset happigradientit, joiden avulla voidaan määrittää etäisyys astiasta. Kun PO2: ta ei voida mitata suoraan, voidaan päätellä solun etäisyys hypoksiaa indusoivien geenien induktio-/ekspressiogradienteistä erityyppisissä soluissa (”hypoksian sormenjälki”, kuva 1 aluksen poikittainen näkymä) (15-17).
verisuonten CCF: n edut
vaskulatuurikoordinaatisto on biologisesti järkevä. Jokaisen elävän solun on sijaittava pienellä säteellä lähimmästä verisuonesta (kudoksesta riippuen 100 µm-1 mm) saadakseen happea (18); ja jokaista alusta reunustaa sama jatkuva endoteelikerros (19). Siten, verisuonitus muodostaa katkeamaton reitti, joka saavuttaa kaikki kehon osat, saumattomasti kapeneva alas asteikot, makroskooppi (koko kehon/kliininen) mesoskale mikroskooppi (yhden solun kokoinen kapillaari alukset). Osana tätä, se käsittelee asteittaista siirtymistä suurista valtimoista ja laskimoista, jotka säilyvät useimmilla ihmisillä, alas miljoonia mikroskooppisia aluksia, jotka ovat tunnistettavissa luokan (esim., glomerulus kapillaari), mutta ei yksittäisiä nimiä. Verisuonisto mukautuu yksilöllisen kehon kokoon ja muotoon, mikä vastaa yksilöiden välisiä vaihteluita (20, 21). Se määrittelee toiminnallisten yksiköiden muodon eri elimissä, kuten maksalohkoissa, munuaiskeräsissä ja keuhkorakkuloissa. Uuden kudoksen normaali kehitys alkaa verisuonten muodostumisesta ennen kuin sen ympärille voi kasvaa uusia solutyyppejä (22).
verisuonisto tavoittaa myös kaikki elimet, kudokset ja solut yhtenäisesti. Muilla anatomisilla rakenteilla ei näytä olevan samanlaista monipuolisuutta. Esimerkiksi luusto ulottuu koko kehoon; kuitenkin, etäisyys solun sisällä elin voi olla useita senttimetrejä, ja että luu ei todennäköisesti ole osa elin, ja vielä vähemmän todennäköisesti osa kudosnäyte. Hermosto seuraa monia samoja reittejä kuin suuremmat alukset, joilla on supistumiskykyisiä ominaisuuksia, mutta ei tiedetä, ulottuvatko ne seuraamaan pienempiä aluksia, jotka saavuttavat kaikki kudossolut. Toisin kuin solujen happiriippuvuus, ei ole takeita siitä, että jokainen solu on lähellä hermoa. Elinkohtaiset vertailujärjestelmät perustuvat ainutlaatuisiin rakenteellisiin ominaisuuksiin, joita esiintyy vain kyseisessä yksittäisessä elimessä (esim.aivojen tietyillä alueilla) ja joista ei todennäköisesti ole hyötyä solujen sijaintien kuvaamisessa muualla kehossa.
verisuonikoordinaatistosta on monia käytännön etuja. Kaikkien elinten verisuonireittejä on tutkittu paljon ja ne on kuvattu kirjallisuudessa yksityiskohtaisesti. Ne ovat hyödyllisiä, tunnettuja ja niillä on standardoidut nimet monilla erikoisaloilla. Kudosten verisuonitus malleja käytetään kliinisesti diagnosoida tauti; ja, aluksia käytetään kirurgiassa ja biopsiat tärkeimmät anatomiset maamerkit ja määritellä ”verisuonten alueet” (23, 24). Vaikka tarkka sijainti 3D Karteesisessa tilassa voi olla vaikea määrittää resektoidulle kudosnäytteelle, kirurgi yleensä pystyy osoittamaan, mikä verisuonten vedenjakaja sisälsi näytteen.
verisuonten CCF: n rajoitukset
vain emäsparien tunteminen genomisekvenssissä ei anna riittävästi tietoa sen määrittämiseksi, miten DNA taittuu tietyssä solussa. Vastaavasti, vaikka avautumaton verisuonikoordinaatisto voi kuvata lähisolujen 3D-avaruussuhdetta mikroskoopilla, alusten viemät mutkitteluradat ja solujen suhteellinen etäisyys suuremmissa mittakaavoissa menetetään. Tietoa suuremman mittakaavan rakenteista voitaisiin saada yhdistämällä kliininen kuvantaminen sekä histologinen ja molekyylikuviointi.
joitakin muita sijaintitietoja menetetään verisuonireittien luhistuessa. Esimerkiksi verisuonten koordinaatisto saattaa aluksi käsitellä kaikkia munuaiskerästen hiussuonia samana rakenteena, mikä saattaa peittää erot munuaiskerästen ylä-ja ala-arvoisissa munuaispylväissä. Kun opimme lisää näiden reittien biomolekulaarisista profiileista, voimme iteratiivisesti jalostaa verisuonten CCF: ää ajan myötä jakamalla reitit mihin tahansa löydettyihin alatyyppeihin.
näistä rajoituksista huolimatta verisuonikoordinaatisto säilyttää riittävästi sijaintitietoa vastatakseen monenlaisiin tutkimuskysymyksiin siten, että tutkijat voivat tarkasti paikallistaa yksittäisiä soluja funktionaalisissa yksiköissä, kudoksissa ja elimissä tai vertailla kontekstin vaikutuksia eri solutyyppeihin koko kehossa makro – ja mesoasteikolla.
next Steps and Future Directions
kuvassa 1 esitetään hyvin yksinkertaistettu ja tyylitelty esitys vaskulaarisesta CCF: stä yleisen konseptin esittelemiseksi. Varsinaiset verisuoniradat ovat paljon monimutkaisempia, ja koko verisuonten CCF koostuu lopulta sadoista tai tuhansista rakenteista sekä haarautumiskuvioista, jotka eivät noudata tiukkaa napapohjaista asettelua. Esimerkiksi maksaportaalijärjestelmän laskimot, jotka kuljettavat verta useista elimistä maksaan, ja verenkierron anastomoosit, kuten Willisin ympyrä aivoissa, kulkisivat kohtisuoraan Kuvan 1 ”pinnoja” vastaan ja ylittäisivät ne.
vaskulaariseen CCF: ään on myös sisällytettävä verisuoniston normaaleja anatomisia variantteja, kuten thyroidea ima ja kaksoiskovidaalinen verisuonisto, samalla tavalla kuin yksittäiset nukleotidipolymorfismit (SNP) kuvaavat genomin normaalivaihteluita. Kun laajennamme ja täytämme verisuonten CCF: n yksityiskohdat, se saattaa saada enemmän lumihiutaleen tai web-kaltaisen ulkonäön, jossa todennäköisyydet on osoitettu eri osiin osoittamaan todennäköisyyttä löytää ne tietyssä henkilössä.
varsinainen verisuonten CCF vaatii kehittyneempää koodausjärjestelmää alusten nimeämiseksi kuin kuvassa 1 esitetään, jotta sen monimutkaisuus voidaan esittää tarkemmin ja jotta se voidaan ”laskea” ohjelmistoalgoritmien avulla. Yksi lähestymistapa on hyödyntää olemassa olevia anatomisia ontologioita, kuten UBERONIA, joka sisältää jo uniikkeja Uniform Resource Identifiers (Uri) – tunnisteita monille aluksille ja määrittelee erilaisia suhdetyyppejä, kuten ”branching_part_of”, kuvaamaan alusten yhteyttä (25).
solu voi olla useamman astian lähellä, jolloin sille on mahdollista antaa erillinen osoite suhteessa kuhunkin astiaan. Tulevaisuudessa tarvitaan tutkimusta sen määrittämiseksi, mikä sopiva ”cutoff” etäisyys pitäisi olla. Voisi olla toivottavaa tallentaa useita osoitteita solujen auttaa triangulation niiden sijainti 3D-avaruudessa.
vaikka alkumotivaatiomme verisuonten CCF: lle on määritellä koordinaattijärjestelmä solujen sijainnin määrittämistä varten, ihmisruumiin uudenlaisella säteittäisellä asettelulla verisuonten ympärillä, kuten kuvassa 1 esitetään, voisi olla muitakin tieteellisiä sovelluksia. Esimerkiksi sijaintitieto tässä kehyksessä on analogia embryologiseen kehitykseen ja saattaa antaa tietoa mekanismeista, jotka aiheuttavat sairauksia tai säätelyhäiriöitä, jotka johtuvat soluryhmästä. Esimerkiksi vaskulaarisessa CCF: ssä tyypin 2 diabetekseen liittyvät makrovaskulaariset sairaudet (esim.iskeeminen sydänsairaus, perifeerinen verisuonisairaus ja aivoverisuonisairaus) ryhmittyvät lähelle keskustaa, kun taas mikrovaskulaariset sairaudet (esim. retinopatia, nefropatia ja neuropatia) muodostavat renkaan ulkopuolelle (26).
Yhteenveto
verisuonistolla on useita ominaisuuksia, jotka vastaavat niitä ominaisuuksia, joita on aiemmin pidetty toivottavina CCF: lle, jotta ihmisruumiin kaikki solut voidaan kartoittaa (7). (1) Se toimii useilla asteikoilla. Jatkuvan endoteelin kautta se siirtyy saumattomasti suurista anatomisista rakenteista solutasolle. (2) Sitä sovelletaan kaikkiin kehon kudoksiin. Koska elimet kehittyvät alusten ympärille, verisuonitus kehystää urkujen arkkitehtuuria kaikissa mittakaavoissa. Verisuonikuviot ovat niin erottuvia, että pelkästään alusten kuvia, joissa kaikki muut solut on poistettu, voidaan helposti käyttää elimen tunnistamiseen. 3) Se selittää lahjoittajien väliset erot. Vaskularisaatio sopeutuu luonnollisesti yksilöllisiin muutoksiin kudoksessa, kehon koossa ja muodossa. Sen sijaan, että kunkin glomeruluksen 3D-koordinaatit olisi kartoitettava yhdessä ihmisessä oleviin glomeruluksiin, verisuonten CCF asettaisi jokaisen solun edustavaan glomerulus-kapillaariin jokaisesta ihmisestä. (4) verisuonitus on hyvin tunnettu monien eri kliinisten erikoisalojen harjoittajille, jotka auttavat sekä diagnosoimaan sairauksia että ohjaamaan leikkauksia, ja joita patologit, radiologit ja muut lääkärit käyttävät maamerkkeinä. Tämä helpottaisi kudosnäytteiden sijoittamista elimistöön ja yksittäisten solujen sijainnin kirjaamista. Vaikka mikään yksittäinen CCF ei ole ihanteellinen kaikkiin käyttötapauksiin, vaskulaarinen CCF määrittelee luonnollisen koordinaattijärjestelmän, jonka avulla on helppo yhdistää biomolekulaarisia tietoja useilta ihmisiltä ja kysyä biologisesti merkityksellisiä tutkimuskysymyksiä.
tiedon Saatavuuslausunto
julkisesti saatavilla olevat aineistot analysoitiin tässä tutkimuksessa. Tiedot löytyvät täältä: https://www.proteinatlas.org.
tekijän kannanotot
GW laati tämän tutkimuksen CCF-kokouksen ja 2019 CCF-Työpajan raporttien perusteella. Kb ja YJ antoivat kriittistä palautetta. GW kirjoitti alkuperäisen luonnoksen, jossa oli tekstiä puhtaaksi CCFWS – 01-diaesityksestä. Kaikki kirjoittajat osallistuivat käsikirjoituksen muokkaamiseen.
Rahoitus
tätä tutkimusta tuki National Institutes of Health (NIH) award OT2OD026671. Tämä työ ei edusta NIH: n tai National Heart, Lung, and Blood Instituten (NHLBI) mielipidettä.
eturistiriita
kirjoittajat toteavat, että tutkimus tehtiin ilman kaupallisia tai taloudellisia suhteita, jotka voitaisiin tulkita mahdollisiksi eturistiriidoiksi.
kiitokset
Kiitämme tohtori Zorina S. Galis National Institutes of Health auttaa kehittämään ajatusta verisuoniperäisestä koordinaatistosta 2017 CCF-kokouksessa ja 2019 CCF-työpajassa, joka tarjoaa meille esityksiä näistä tapahtumista ja osallistuu lukuisiin keskusteluihin, jotka muodostivat tämän käsikirjoituksen perustan. Arvostelijoiden asiantuntijakommentit auttoivat selventämään ja tarkentamaan ehdotettua vaskulaarista yhteistä koordinaatistoa.
3. Uhlén M, Björling E, Agaton C, Szigyarto CA, Amini B, Andersen E, et al. A human protein atlas for normal and cancer solutions based on vasta proteomics. Mol-Soluproteomiikka. (2005) 4:1920–32. doi: 10.1074 / mcp.M500279-MCP200
PubMed Abstract | CrossRef Full Text | Google Scholar
12. Vanlandewijck M, He L, Mäe MA, Andrae J, Ando K, Del Gaudio F, et al. Molekyyliatlaksen solutyypeistä ja zonaatiosta aivojen verisuonistossa. Luonto. (2018) 554:475–80. doi: 10.1038/nature25739
PubMed Abstract | CrossRef Full Text | Google Scholar
14. Johnson C, Sung HJ, Lessner SM, Fini ME, Galis ZS. Matrix metalloproteinase-9 is required for adequate angiogenic revascularization of ischemic tissues: potential role in capillary branching. Circ Res. (2004) 94:262–8. doi: 10.1161/01.RES.0000111527.42357.62
PubMed Abstract | CrossRef Full Text | Google Scholar
15. De Santis V, laulaja M. Tissue oxygen tension monitoring of organ perfusion: rationale, methodologies, and literature review. Br J Anaesth. (2015) 115:357–65. doi: 10.1093/bja/aev162
PubMed Abstract | CrossRef Full Text | Google Scholar
17. Koch CJ. Solujen ja kudosten absoluuttisten happipitoisuuksien mittaaminen happiantureilla ja 2-nitroimidatsolilla EF5. Menetelmät Entsymoli. (2002) 352:3–31. doi: 10.1016/S0076-6879(02)52003-6
PubMed Abstract | CrossRef Full Text | Google Scholar
20. Paruchuri V, Salhab KF, Kuzmik G, Gubernikoff G, Fang H, Rizzo JA, et al. Aortic size distribution in the general population: explaining the size paradox in aortic dissection. Cardiology. (2015) 131:265–72. doi: 10.1159/000381281
PubMed Abstract | CrossRef Full Text | Google Scholar
21. Abadi E, Segars WP, Sturgeon GM, Roos JE, Ravin CE, Samei E. Modeling lung architecture in the XCAT series of phantoms: physiologically based airways, valtimot ja laskimot. IEEE Trans Med Imaging. (2018) 37:693–702. doi: 10.1109 / TMI.2017.2769640
PubMed Abstract | CrossRef Full Text/Google Scholar
24. Majno P, Mentha G, Toso C, Morel P, Peitgen HO, Fasel JH. Maksan anatomia: ääriviivat kolmella monimutkaistasolla–uusi askel kohti räätälöityjä alueellisia maksan resektioita. J Hepatol. (2014) 60:654–62. doi: 10.1016/j.jhep.2013.10.026
PubMed Abstract | CrossRef Full Text | Google Scholar
26. Cade WT. Diabetes-related microvascular and macrovascular diseases in the physical therapy setting. Phys Ther. (2008) 88:1322–35. doi: 10.2522/ptj.20080008
PubMed Abstract | CrossRef Full Text | Google Scholar