Choix centré sur le patient de l’insuline prandiale
Diverses insulines prandiales, y compris l’insuline humaine régulière, l’asparte, la glulisine, le lispro et l’insuline asparte à action rapide (FIAsp), sont utilisées dans le cadre des régimes basal plus, basal bolus ou prandial seul. Certaines insulines prandiales, également appelées insulines à courte durée d’action, peuvent également être utilisées par voie intraveineuse ou dans des pompes à perfusion d’insuline. L’objectif de cet éditorial est de classer les insulines prandiales, de comprendre leurs propriétés pharmacologiques et d’explorer leur utilisation dans la pratique clinique actuelle. Il met également en évidence les caractéristiques uniques qui permettent une utilisation préférentielle de ces insulines dans des situations cliniques spécifiques.
L’insuline est un élément essentiel du traitement hypoglycémiant. La plupart des recommandations sur le traitement hypoglycémiant se concentrent sur les schémas insuliniques à choisir pour l’initiation et l’intensification.1,2 Le débat et la controverse portent généralement sur le choix d’un traitement basal par rapport à un traitement prémélangé en tant qu’insulinothérapie initiale.3 Dans un tel scénario, l’importance des insulines prandiales et des préparations spécifiques d’insuline prandiale est souvent ignorée. Cette revue explore les similitudes et les différences de diverses préparations d’insuline prandiales, et partage des informations sur leur utilité différentielle dans les soins du diabète.
Classification
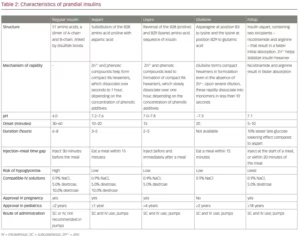
Les différents types d’insulines prandiales disponibles dans le monde peuvent être classés comme insuline humaine à action rapide, analogues de l’insuline à action rapide et analogues à action ultrarapide (tableau 1). Cette classification est basée sur l’origine de l’insuline et ses propriétés pharmacocinétiques, en particulier le début de l’action. Bien que de nature pharmacologique, cette structure taxonomique a également une utilité clinique. Il informe le moment de l’injection par rapport aux repas et permet une flexibilité dans l’administration d’insuline à action ultra-rapide. Les similitudes et les différences entre les différentes insulines prandiales sont énumérées dans le tableau 2. Beaucoup de ces insulines sont également disponibles sous forme de biosimilaires, tels que l’insuline régulière et lispro.
Des versions à haute concentration d’insulines prandiales sont également disponibles, par exemple: insuline régulière U500, insuline lispro U200 et insuline régulière U200. Le lispro U200 possède des propriétés pharmacocinétiques et pharmacodynamiques similaires à celles du lispro U100. Par rapport à l’insuline régulière U100, l’insuline régulière U500 a un délai d’effet maximal plus long (5 heures contre 6 heures, respectivement) et une durée d’action plus longue (18 heures contre 24 heures, respectivement). Diminution du volume, diminution du nombre d’injections et diminution de la douleur pendant l’administration sont quelques avantages de ces insulines concentrées.4,5
Voie intraveineuse
L’insuline prandiale peut être administrée par voie intraveineuse ou sous-cutanée, et rarement par injection intramusculaire.6-8 Il peut également être mélangé avec des sacs de nutrition parentérale totale pour l’administration intraveineuse centrale. Les différences structurelles entre les différents analogues ont un impact sur leur compatibilité avec différents fluides intraveineux. Ainsi, alors que l’insuline glulisine est compatible avec une solution saline normale et le lactate de Ringer, elle ne peut pas être utilisée dans des solutions contenant du dextrose. Les autres insulines prandiales peuvent être diluées avec tous les liquides cristallins intraveineux couramment utilisés. Cela permet l’utilisation sans restriction d’insuline humaine régulière, d’aspart, de lispro et de FIAsp en milieu hospitalier. Les programmes de gestion de l’insuline des unités de soins intensifs et des services hospitaliers doivent refléter la préparation et la concentration des insulines prandiales utilisées, ainsi que leur mode d’administration.9 La réduction de la morbidité et de la mortalité a été associée à l’insuline asparte en milieu hospitalier.10 L’insuline asparte présentant un meilleur profil d’efficacité et de sécurité que l’insuline humaine à courte durée d’action semble être une bonne alternative à l’insuline humaine à courte durée d’action.10

Dans certains pays, la disponibilité des flacons et seringues d’insuline U40, U100 et U500 augmente la probabilité d’erreur posologique à moins que les patients ne soient informés et familiarisés avec différents types de flacons et de seringues au moment de l’initiation de l’insulinothérapie. Les patients doivent être informés que les flacons U100 doivent être utilisés avec des seringues U100 et les flacons U40 avec des seringues d’insuline U40 uniquement.11
Insulines prandiales inhalées
Les deux premières insulines inhalées à action rapide, Exubera® (Pfizer, New York, New York, États-Unis) et Afrezza® (MannKind Corporation, Westlake Village, Californie, États-Unis), ont hypothétiquement éliminé les barrières psychologiques associées à l’administration d’insuline sous-cutanée, telles que la phobie des aiguilles et une technique d’injection incorrecte.12 Cependant, ces préparations d’insuline inhalées n’ont pas répondu à leurs attentes.
Moins de 2 ans après son approbation, Exubera a été retiré du marché en raison de plusieurs inconvénients liés au produit et n’avait « pas réussi à être accepté par les patients et les médecins », ce qui a entraîné un faible volume de ventes.13 Il a été démontré que l’hypoglycémie était l’effet indésirable le plus fréquent d’Exubera. De nombreux effets indésirables respiratoires ont été rapportés, notamment un risque accru d’infection respiratoire, de toux, de pharyngite et de rhinite. Un changement d’étiquette de sécurité a été émis concernant le cancer du poumon lorsque six nouveaux cas de tumeurs malignes du poumon ont été détectés chez des patients prenant Exubera.14
Afrezza semble avoir des avantages clés par rapport à Exubera. Son système d’administration est petit, élégant et dosé en unités et il fournit un tableau de conversion de dosage simple, alors que le système d’administration d’Exubera était grand, maladroit et dosé en milligrammes.12 Le profil d’innocuité d’Afrezza ressemble à celui d’Exubera, avec une diminution de la fonction pulmonaire et une légère augmentation de l’incidence du cancer du poumon. De nouvelles préoccupations ont été soulevées après l’approbation d’Afrezza, ce qui a incité la Food and Drug Administration (FDA) des États-Unis à exiger une stratégie d’évaluation et d’atténuation des risques et un avertissement de boîte noire informant le patient d’un risque accru de bronchospasme aigu chez les personnes atteintes d’une maladie pulmonaire chronique.15 L’acidocétose diabétique s’est également avérée plus fréquente chez les patients de la cohorte Afrezza.15
Soins de transition
Lors de la transition d’un établissement de soins intensifs à un établissement hospitalier non critique, ou d’un hôpital à un établissement de soins OPD, d’autres considérations viennent au premier plan. Un début d’action rapide permet une transition facile des injections intraveineuses aux injections sous-cutanées avec un risque minimal d’hyperglycémie et sans arrêt de l’insuline intraveineuse. Une transition correctement planifiée nécessite que la première dose d’insuline sous-cutanée soit administrée au moins 1 heure (pour les insulines sous-cutanées à courte durée d’action; idéalement 2 à 3 heures pour les insulines sous-cutanées à longue durée d’action) avant l’arrêt de la perfusion.16 L’utilisation d’analogues à action ultrarapide, tels que le FIAsp, offre des avantages pratiques et pragmatiques dans ce contexte.17
Voie sous-cutanée
Lorsque l’insuline prandiale est utilisée par voie sous-cutanée, elle peut être utilisée dans le cadre d’un régime basal plus, basal bolus ou prandial uniquement.18 Dans tous ces régimes, l’insuline est administrée avant le repas. L’intervalle idéal entre l’injection et le repas varie en fonction de la préparation prandiale. Bien que toutes les insulines prandiales soient efficaces dans ce cadre, la tolérance de sécurité et la commodité sont les facteurs décisifs pour faire un choix d’insuline centré sur le patient. L’insuline humaine régulière reste l’insuline la plus économique au monde, mais peut ne pas être disponible dans certains pays. L’insuline humaine régulière doit être injectée 30 minutes avant un repas, mais cela limite sa flexibilité.19 Les analogues à action rapide offrent une plus grande flexibilité et sont surpassés à cet égard par les analogues à action ultra-rapide. Alors que l’aspart, le lispro et la glulisine peuvent être injectés immédiatement avant un repas, FIAsp peut être administré jusqu’à 20 minutes après un repas.20 Cependant, la disponibilité peut varier d’un pays à l’autre.
Un autre avantage du FIAsp à action ultrarapide est son début et son pic d’action plus rapides, ce qui conduit à une meilleure résolution de la glycémie postprandiale de 1 heure.21 Ceci est utile dans des situations cliniques telles que le diabète gestationnel et le diabète induit par les corticostéroïdes, et chez les personnes ayant des préférences alimentaires pour des repas riches en glucides et à indice glycémique élevé. La réduction relativement plus rapide de l’action de l’insuline se traduit par un risque plus faible d’hypoglycémie avant les repas avec FIAsp (car la durée globale d’action de cette insuline est légèrement inférieure à celle de l’insuline asparte). Dans le même contexte, des données suggèrent qu’il existe un risque réduit d’hypoglycémie nocturne avec l’utilisation de FIAsp à l’heure du dîner, en raison de sa durée d’action réduite, par rapport aux analogues de l’insuline à action rapide (aspart, lispro ou glulisine) dont la durée d’action peut durer plus longtemps dans la nuit.21 Cela réduit le degré d’inconvénient dans le mode de vie du patient lié à l’utilisation de l’insuline prandiale et permet une plus grande liberté dans la planification d’activités physiques, d’exercices ou de loisirs, telles que manger dans un restaurant où la quantité de glucides / calories peut être imprévisible (et où FIAsp peut être pris après avoir terminé le repas). Il évite également la nécessité d’un schéma de repas 3 + 3 qui a été classiquement prescrit dans les régimes de bolus basaux.
La possibilité d’injecter des insulines à action rapide et ultrarapide immédiatement avant, voire après un repas, permet d’ajuster les doses d’insuline en fonction de l’appétit ou du comptage des glucides. Cette flexibilité est particulièrement avantageuse chez les très jeunes et les personnes âgées, ainsi que chez les personnes ayant une perte d’appétit, des nausées ou un risque de vomissements, telles que celles présentant une insuffisance rénale, hépatique ou gastro-intestinale supérieure. Il a été rapporté que le FIAsp avait une cinétique plus rapide s’il était injecté par voie intradermique dans des études in vivo.22

Pompes à insuline
Le traitement par pompe à insuline est basé sur l’utilisation d’insuline de courte durée d’action ou prandiale en perfusion sous-cutanée continue, pour maintenir les niveaux d’insuline basale. Le dosage prandial est assuré en appuyant sur les boutons de la pompe au moment des repas sur la base de rapports glucides insuline/repas prédéterminés. Ce véhicule d’administration d’insuline ajuste les taux d’insuline basale et les taux d’insuline en bolus de manière plus précise, en particulier chez les diabétiques de type 1 et les diabétiques fragiles. Les technologies plus récentes, telles que les systèmes de surveillance continue de la glycémie, sont associées à des pompes plus récentes (par exemple, MiniMed ™ 670G, Medtronic, Dublin, Irlande) et peuvent ajuster automatiquement les taux basaux de ces pompes en fonction des niveaux de glycémie du patient, à l’aide d’algorithmes liés au cloud auto-apprentissage (IBM Watson cloud utilisé par le système hybride en boucle fermée Medtronic 670G).
Les différences physico-chimiques entre les différentes insulines entraînent des différences de stabilité, de compatibilité et d’utilité dans les systèmes de pompe à insuline ou de perfusion. Dans des études, l’insuline asparte s’est avérée plus stable que l’insuline glulisine lors d’une perfusion sous-cutanée continue d’insuline en termes de stabilité physique contre la formation de fibrilles d’insuline insolubles, ainsi que de stabilité chimique en termes de formation de protéines solubles de haut poids moléculaire.23,24
Flexibilité et insuline prandiale
Dans la gestion du diabète centrée sur le patient, il faut essayer de fournir un contrôle glycémique efficace et sûr, avec une intrusion minimale dans le mode de vie du patient. Les propriétés pharmacodynamiques et pharmacocinétiques d’une insuline prandiale devraient lui permettre d’offrir une flexibilité dans la voie et le moment de l’administration, la posologie, le choix du modèle de repas et la capacité de planifier une activité physique, un exercice ou une activité de loisirs. Cette caractéristique supplémentaire peut également améliorer l’adhésion du patient à l’insulinothérapie.20 insulines prandiales modernes à action ultrarapide peuvent offrir cette flexibilité. Si la disponibilité, l’accès et l’abordabilité ne sont pas une préoccupation, de telles préparations d’insuline doivent être préférées pour une utilisation dans la prise en charge du diabète. Les situations cliniques qui sont des indications préférentielles pour FIAsp sont énumérées dans le tableau 3.
Nous réitérons que, quelle que soit la préparation d’insuline utilisée, la technique d’injection correcte doit être suivie. Il n’y a pas de substitut à une technique d’insuline appropriée, qui garantit que la dose correcte d’insuline est administrée, de manière confortable, dans un tissu sous-cutané sain, au moment approprié.25
Résumé
Cette brève revue offre une approche centrée sur le patient et un aperçu cliniquement orienté de l’utilisation de diverses insulines prandiales. Il classe et décrit ces préparations, et partage des suggestions concernant leur utilisation rationnelle en tant qu’insuline intraveineuse et sous-cutanée de transition. Cet article souligne la flexibilité que l’insuline à action ultrarapide permet aujourd’hui dans les soins du diabète.