Physiopathologie / Fondation internationale pour l’ostéoporose
Les hormones sont probablement les modulateurs les plus cruciaux de la formation osseuse. Il est bien établi que oestrogène Lindsay, R., Prévention et traitement de l’ostéoporose. Lancette, 1993. 341 (8848): p. 801-5.
. lèvres de l’hormone parathyroïdienne, P., physiologie de la vitamine D. Prog Biophys Mol Biol, 2006. 92(1): p. 4-8
. et dans une moindre mesure, la testostérone directement ou indirectement via la conversion en œstrogènes Seeman, E., La base structurelle de la fragilité osseuse chez les hommes. Bone, 1999. 25(1): p. 143-7.
Van Pottelbergh, I., et coll., Statut de stéroïde sexuel perturbé chez les hommes atteints d’ostéoporose idiopathique et leurs fils. J Clin Endocrinol Metab, 2004. 89(10): p. 4949-53.
. sont essentiels pour un développement et un entretien optimaux des os. Parmi ceux-ci, on pense maintenant que les œstrogènes ont l’effet le plus direct sur les cellules osseuses, interagissant avec des protéines spécifiques, ou récepteurs, à la surface des ostéoblastes et des ostéoclastes Zallone, A., Actions œstrogènes directes et indirectes sur les ostéoblastes et les ostéoclastes. Ann N Y Acad Sci, 2006. 1068: p. 173-9
.
Cette interaction déclenche une chaîne complexe d’événements au sein des cellules, augmentant l’activité des ostéoblastes tout en interférant avec la communication ostéoblaste-ostéoclaste – l’une des ironies du remodelage osseux est que les ostéoblastes libèrent des facteurs qui stimulent les ostéoclastes et stimulent la résorption osseuse, comme nous le verrons ci-dessous.
Les effets des œstrogènes sont médiés par un type spécifique de récepteur de surface cellulaire appelé récepteur alpha des œstrogènes (ERa), qui lie et transporte l’hormone dans le noyau de la cellule où le complexe récepteur-hormone agit comme un interrupteur pour activer des gènes spécifiques. Les récepteurs ERa se trouvent à la surface des ostéoblastes, tout comme le récepteur alpha lié au récepteur des œstrogènes (ERRa), qui peut jouer un rôle auxiliaire dans la régulation des cellules osseuses Bonnelye, E. et J.E. Aubin, récepteur alpha lié au récepteur des œstrogènes: un médiateur de la réponse des œstrogènes dans l’os. J Clin Endocrinol Metab, 2005. 90(5): p. 3115-21.
. Des études récentes suggèrent également que la globuline de liaison aux hormones sexuelles (SHBG), qui facilite l’entrée des œstrogènes dans les cellules, pourrait également jouer un rôle de soutien Goderie-Plomp, H.W., et al., Hormones sexuelles endogènes, globuline liant les hormones sexuelles et risque de fractures vertébrales chez les hommes et les femmes âgés: l’étude de Rotterdam. J Clin Endocrinol Metab, 2004. 89(7): p. 3261-9.
.
L’œstrogène, bien sûr, est fabriqué et sécrété dans la circulation sanguine à une certaine distance des os et il a également des effets profonds sur d’autres tissus, tels que l’utérus et le sein. Mais il existe d’autres molécules de signalisation produites localement qui ont des effets profonds sur la physiologie osseuse.

Figure taken from Ferrari & Roux, 2019 Pocket Reference to Osteoporosis, S. Ferrari, Roux, C., Editor 2019, Springer International Publishing.
.
Prostaglandins, particularly prostaglandin E2 (PGE2), stimulate both resorption and formation of bone Pilbeam, C.C., J.R. Harrison, and L.G. Raisz, Chapter 54 – Prostaglandins and Bone Metabolism, in Principles of Bone Biology (Second Edition), J.P. Bilezikian, L.G. Raisz, and G.A. Rodan, Editors. 2002, Academic Press: San Diego. p. 979-994
. La PGE2 est un lipide qui se forme dans diverses cellules osseuses à partir d’un précurseur appelé acide arachidonique. La première étape de la synthèse de la PGE2 est réalisée par une enzyme appelée cyclooxygénase 2 (COX2) et les inhibiteurs de cette enzyme peuvent empêcher la formation osseuse en réponse à un stress mécanique chez les animaux Forwood, M.R., la cyclo-oxygénase inductible (COX-2) médie l’induction de la formation osseuse par chargement mécanique in vivo. J Bone Miner Res, 1996. 11(11): p. 1688-93.
. PGE2 peut être nécessaire pour la formation osseuse induite par l’exercice.
Il existe des preuves que le risque de fracture est accru chez les personnes prenant des anti-inflammatoires non stéroïdiens qui inhibent la COX-2 Carbone, L.D., et al., Association entre la densité minérale osseuse et l’utilisation d’anti-inflammatoires non stéroïdiens et d’aspirine: impact de la sélectivité de la cyclooxygénase. J Bone Miner Res, 2003. 18 (10): p. 1795-802
peut également augmenter. Les leucotriènes sont un autre ensemble de molécules lipidiques qui semblent réguler le remodelage osseux. Également dérivés de l’acide arachidonique, ceux-ci ont été trouvés pour réduire la densité osseuse chez les souris Traianedes, K., et al. Les métabolites de la 5-Lipoxygénase inhibent la formation osseuse in vitro. Endocrinologie, 1998. 139(7): p. 3178-84.
.
L’impact de l’une de ces hormones sur le remodelage osseux dépend de la façon dont elles modifient l’activité des ostéoclastes et/ou des ostéoblastes. Des récepteurs de surface cellulaires spécifiques aident à transmettre des signaux provenant de cellules osseuses extérieures dans le noyau cellulaire, où différents gènes qui régulent l’activité cellulaire peuvent être activés ou désactivés. Ceux-ci comprennent les récepteurs des protéines morphogénétiques osseuses (BMP), une famille de protéines qui sont de puissants inducteurs de la formation osseuse.
Des récepteurs BMP ont été trouvés à la surface de cellules précurseurs d’ostéoblastes Mbalaviele, G., et al., la bêta-caténine et la BMP-2 se synergisent pour favoriser la différenciation des ostéoblastes et la formation de nouveaux os. J Cell Biochem, 2005. 94(2): p. 403-18.
. Un autre récepteur de surface cellulaire appelé récepteur de la protéine 5 liée aux lipoprotéines de basse densité (LDL) (LRP5), un récepteur Wnt, peut également être important pour la formation osseuse car la perte de LRP5 chez les animaux entraîne une ostéoporose sévère Gong, Y., et al., La protéine 5 liée aux récepteurs LDL (LRP5) affecte l’accumulation osseuse et le développement oculaire. Cell, 2001. 107(4): p. 513-23.
. Les récepteurs BMP et LRP5 peuvent coopérer pour stimuler l’action des ostéoblastes, bien que la façon exacte dont cela pourrait se produire n’ait pas été précisée.
La sclérostine, produit du gène SOST et exprimée par les ostéocytes, se lie au récepteur LRP5/6 sur les ostéoblastes et inhibe la signalisation Wnt, entraînant une diminution de la formation osseuse Bonewald, L.F., L’ostéocyte étonnant. J Bone Miner Res, 2011. 26(2): p. 229-38.
Li, X., et al., La sclérostine se lie à LRP5 / 6 et antagonise la signalisation Wnt canonique. J Biol Chem, 2005. 280 (20): p. 19883-7.
. L’hormone parathyroïdienne (PTH) et la charge mécanique diminuent la sécrétion de sclérostine par les œstéocytes Bellido, T., et al., L’élévation chronique de l’hormone parathyroïdienne chez la souris réduit l’expression de la sclérostine par les ostéocytes: un nouveau mécanisme de contrôle hormonal de l’ostéoblastogenèse.Endocrinologie, 2005. 146(11): p. 4577-83.
Robling, A.G., et al., La stimulation mécanique de l’os in vivo réduit l’expression ostéocytaire de la Sost / sclérostine. J Biol Chem, 2008. 283(9): p. 5866-75.
. Un anticorps contre la sclérostine a été développé en tant que médicament potentiel aux propriétés puissantes sur la résistance osseuse. Read more on anabolics as treatments.

Figure taken from Ferrari & Roux, 2019 Pocket Reference to Osteoporosis, S. Ferrari, Roux, C., Editor 2019, Springer International Publishing.
.
Un récepteur de surface cellulaire appelé RANK (pour receptor activator of NFkB) pousse les cellules précurseurs des ostéoclastes à se développer en ostéoclastes entièrement différenciés lorsque RANK est activé par son ligand de rang partenaire apparenté (RANKL) Yasuda, H., et al., Le facteur de différenciation des ostéoclastes est un ligand pour l’ostéoprotégérine / facteur inhibiteur de l’ostéoclastogenèse et est identique à TRANCE / RANKL. Proc Natl Acad Sci U S A, 1998. 95(7): p. 3597-602.
Lacey, D.L., et coll., Le ligand d’ostéoprotégérine est une cytokine qui régule la différenciation et l’activation des ostéoclastes. Cell, 1998. 93(2): p. 165-76.
.
RANKL, en fait, est produit par les ostéoblastes et est l’une des nombreuses molécules de signalisation qui facilitent le dialogue croisé entre les ostéoblastes et les ostéoclastes et aident à coordonner le remodelage osseux Theill, L.E., W.J. Boyle et J.M. Penninger, RANK-L et RANK: lymphocytes T, perte osseuse et évolution des mammifères. Annu Rev Immunol, 2002. 20: p. 795-823.
. L’ostéoprotégérine, une autre protéine libérée par les ostéoblastes Suda, T., et al., Modulation de la différenciation et de la fonction des ostéoclastes par les nouveaux membres des familles des récepteurs du facteur de nécrose tumorale et des ligands. Endocr Rev, 1999. 20(3): p. 345-57.
, peut également se lier à RANKL, agissant comme un leurre pour empêcher RANK et RANKL d’entrer en contact. L’équilibre entre RANKL et ostéoprotégérine peut être crucial dans l’ostéoporose. En fait, des études animales ont montré qu’une production accrue d’ostéoprotégérine entraîne une augmentation de la masse osseuse, tandis que la perte de la protéine entraîne une ostéoporose et une augmentation des fractures Bucay, N., et al., les souris déficientes en ostéoprotégérine développent une ostéoporose précoce et une calcification artérielle. Genes Dev, 1998. 12(9): p. 1260-8.
. Les inhibiteurs de RANKL se sont également révélés prometteurs en tant que traitement potentiel de l’ostéoporose chez l’homme.
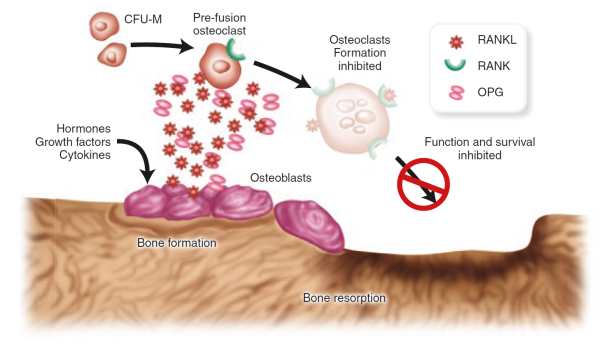
Figure taken from Ferrari & Roux, 2019 Pocket Reference to Osteoporosis, S. Ferrari, Roux, C., Editor 2019, Springer International Publishing.
.
Un deuxième système de signalisation cellulaire complémentaire qui aide à stimuler la formation et l’activation des ostéoclastes a également été découvert au cours des dernières années. En l’absence de la protéine activant le DNAX 12 (DAP12) et de la chaîne γ commune du récepteur Fc (FcRy), deux récepteurs de surface cellulaire, les souris développent une ostéoporose sévère – l’exact opposé de l’ostéoporose – caractérisée par une augmentation spectaculaire de la densité osseuse Mocsai, A., et al., Les protéines adaptatrices immunomodulatrices DAP12 et la chaîne gamma du récepteur Fc (FcRgamma) régulent le développement des ostéoclastes fonctionnels à travers la tyrosine kinase Syk. Proc Natl Acad Sci U S A, 2004. 101(16): p. 6158-63.
Koga, T., et al., Les signaux costimulateurs médiés par le motif ITAM coopèrent avec RANKL pour l’homéostasie osseuse. Nature, 2004. 428 (6984): p. 758-63.
. Ces deux récepteurs de surface cellulaires interagissent avec un groupe de protéines de la cellule appelées protéines adaptatrices ITAM (motif d’activation à base de tyrosine immunoréceptrice) pour provoquer une augmentation du calcium intracellulaire.
Des études suggèrent que le RANK/RANKL et les voies médiées par l’ITAM ont coopéré pour induire une activité complète des ostéoclastes. Ces deux voies peuvent converger pour activer une protéine appelée facteur nucléaire des lymphocytes T activés (NFAT) c1. NFATc1 sert de commutateur principal pour la résorption osseuse car il active les gènes dont les cellules précurseurs des ostéoclastes ont besoin pour devenir des ostéoclastes pleinement actifs Takayanagi, H., Aperçu mécaniste de la différenciation des ostéoclastes en ostéoimmunologie. J Mol Med (Berl), 2005. 83(3): p. 170-9.
.