19.11: Racemizzazione
I derivati bifenilici otticamente attivi (Sezione 13-5A) sono racemizzati se i due anelli aromatici passano in qualsiasi momento attraverso una configurazione complanare per rotazione attorno al legame centrale. Questo può essere causato più o meno facilmente dal calore, a meno che i sostituenti 2,2′-orto siano molto grandi.
Il modo in cui i composti con atomi di carbonio asimmetrici sono racemizzati è più complicato. Una possibilità sarebbe che un carbonio chirale tetraedrico collegato a quattro gruppi diventasse planare e achirale senza rompere alcun legame. Calcoli teorici indicano che questo non è un probabile processo per chirale tetravalente in carbonio ma, come vedremo, si verificano con carbonio chirale e altri chirale atomi che sono collegati a tre gruppi:
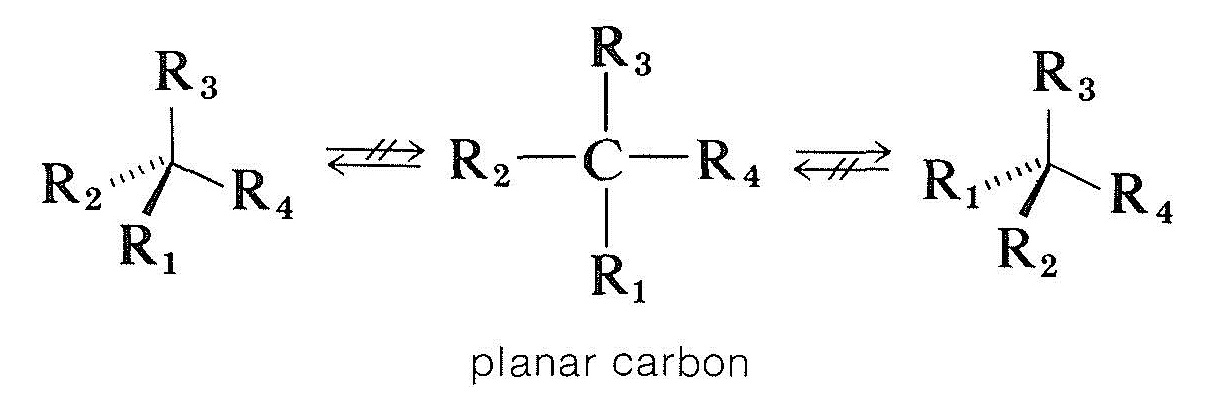
Otticamente attivi composti carbonilici del tipo \(\ce{-CHC=O}\), in cui l’alfa di carbonio asimmetrico, sono racemized sia da acidi e basi, e dalla Sezione 17-1 possiamo essere sicuri che questo è legato a enolization. La formazione dell’enolo o dell’anione enolato distruggerà l’asimmetria del carbonio \(\alfa\) in modo che, anche se solo tracce di enolo sono presenti in un dato momento, alla fine tutto il composto sarà racemizzato. Tuttavia, il meccanismo richiede sia che ci sia un idrogeno \(\alfa\) sia che il centro di simmetria sia situato a questo carbonio \(\alfa\). Altrimenti, acidi e basi sono inefficaci nella catalizzazione della racemizzazione.
.jpg?revision=1)
La racemizzazione di un alogenuro secondario otticamente attivo con il carbonio chirale che trasporta l’alogeno (ad es., 2-clorobutano) può verificarsi soluzione ih e, di solito, il più polare e meglio ionizzante il solvente è, più facilmente la sostanza è racemizzato. La ionizzazione dell’alogenuro mediante un processo \(S_\text{N}1\) è probabilmente responsabile, e questo sarebbe certamente promosso dai solventi polari (Sezione 8-6). Tutte le indicazioni sono che un carbocation alchilico una volta dissociato dal suo anione di accompagnamento è planare; e, quando tale ion si ricombina con l’anione, ha uguale probabilità di formare gli enantiomeri \(D\) e \(L\) :
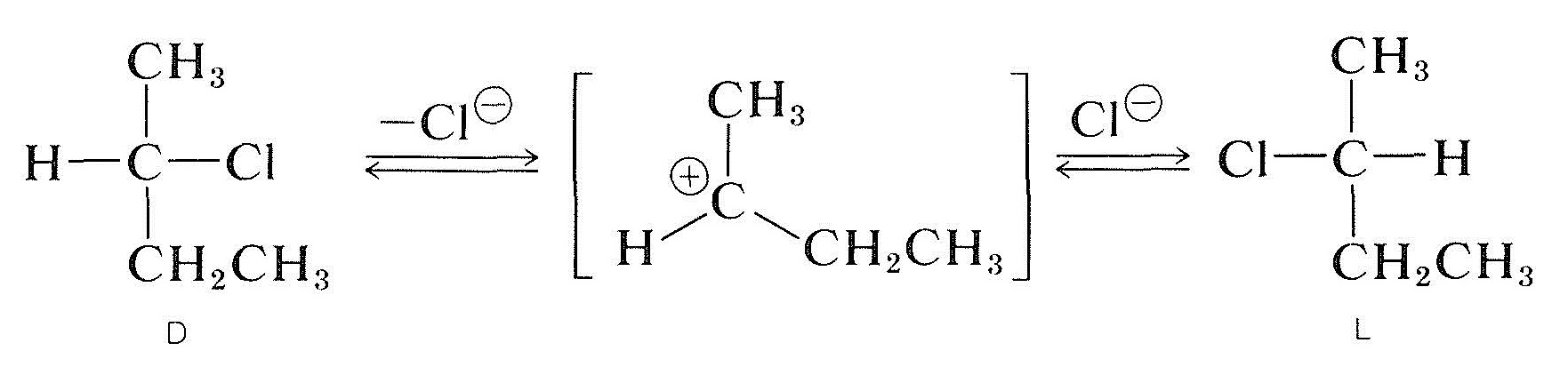
Gli alogenuri otticamente attivi possono anche essere racemizzati da un meccanismo \(S_\text{N}2\). Una soluzione di 2-clorobutano attivo in 2-propanone contenente cloruro di litio disciolto diventa racemica. Lo spostamento del cloruro dell’alogenuro da parte dello chloride cloruro inverte la configurazione dell’atomo in sostituzione (vedere Sezione 8-5). Una seconda sostituzione rigenera l’enantiomero originale. Alla fine, questo processo avanti e indietro produce un numero uguale di forme \(D\) e \(L\); la sostanza è quindi racemica:
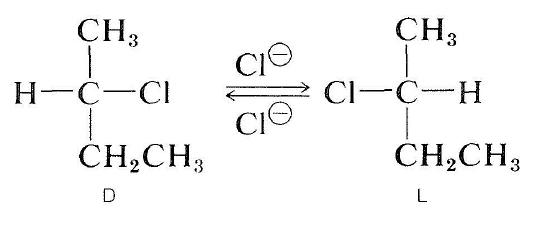
Gli alcoli asimmetrici sono spesso racemizzati da acidi forti. Indubbiamente, la ionizzazione ha luogo e la ricombinazione del carbocation con acqua porta ad enantiomero:
.jpg?revision=1&size=bestfit&width=590&height=243)
In contrasto con alogenuri, alcoli e composti carbonilici, gli idrocarburi possono essere estremamente difficili da racemizzare. Questo è particolarmente vero per un composto quaternario asimmetrica center, come methylethylpropylbutylmethane, \(28\), che non ha “manico”, che consentono di convertire il carbonio asimmetrico per una simmetrica condizione di semplici mezzi chimici:
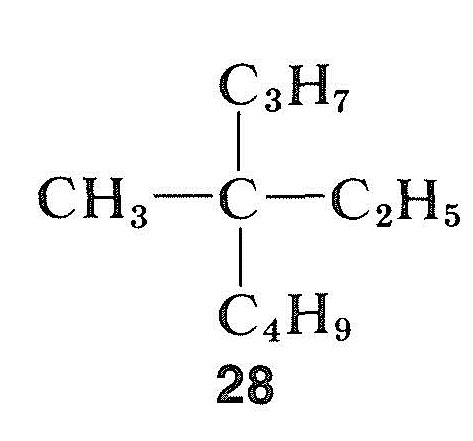
Tuttavia, idrocarburi, che hanno un atomo di idrogeno al carbonio asimmetrico può essere racemized se può essere convertito ai relativi carbocationi o carbanions. La facilità di racemizzazione del tipo carbanione dipenderà dall’acidità dell’idrogeno attaccato e dalla stabilità stereochimica del carbanione intermedio che si forma. Se la configurazione dell’intermedio carbanion si inverte, ne risulterà la racemizzazione (vedi anche Sezione 6-4E):
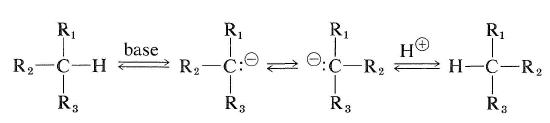
Il tipo di carbocation di racemizzazione di un idrocarburo otticamente attivo può avvenire mediante la reazione di scambio descritta nella Sezione 10-9.
Collaboratori e attribuzioni
- John D. Robert e Marjorie C. Caserio (1977) Principi fondamentali di Chimica Organica, seconda edizione. Per maggiori informazioni:
, Menlo Park, CA. ISBN 0-8053-8329-8. Questo contenuto è protetto da copyright alle seguenti condizioni :” Ti viene concesso il permesso per la riproduzione individuale, educativa, di ricerca e non commerciale, la distribuzione, la visualizzazione e l’esecuzione di questo lavoro in qualsiasi formato.”