Fenantrene
- Fenantrene Proprietà chimiche, usi, produzione
- Idrocarburi policiclici aromatici non lineari
- Struttura molecolare
- Proprietà chimiche
- Usi
- Preparazione
- Proprietà chimiche
- Proprietà chimiche
- Proprietà fisiche
- Usi
- Utilizza idrocarburi policiclici aromatici marcati
- Definizione
- Metodi di produzione
- Sintesi di riferimento(s)
- Descrizione generale
- Aria & Reazioni dell’acqua
- Profilo di reattività
- Pericolo per la salute
- Pericolo di incendio
- Profilo di sicurezza
- Esposizione potenziale
- Cancerogenicità
- Fonte
- Destino ambientale
- Spedizione
- Metodi di purificazione
- Smaltimento dei rifiuti
Fenantrene Proprietà chimiche, usi, produzione
Idrocarburi policiclici aromatici non lineari
Il fenantrene è il più semplice idrocarburi policiclici aromatici non lineari con tre strutture ad anello benzenico, essendo l’isomero dell’antracene. Nel 1872 E. Ostermayer et al ha identificato il fenantrene nella frazione di olio di antracene nel distillato di catrame di carbone, essendo uno dei prodotti di lavorazione del catrame di carbone. Nel catrame di carbone ad alta temperatura, il contenuto di fenantrene è secondario solo al naftalene, essendo circa il 4~6%, principalmente concentrato nelle frazioni di olio di antracene. L’attività chimica del fenantrene è più forte di quella del naftalene, ma è più debole di quella dell’antracene e le reazioni di ossidazione e addizione possono verificarsi anche a 9 e 10 posizioni.
Il fenantrene è un cristallo incolore con lucentezza e il fenantrene precipitato dall’etanolo è un cristallo monoclino incolore. Il fenantrene è un cristallo simile a una foglia con una densità relativa di 1.179 (25/4 ℃) e un indice di rifrazione di 1.6450, punto di fusione del 101 °C e punto di ebollizione punto di 340 °C. può essere soggetto a sublimazione, essendo insolubile in acqua, leggermente solubile in etanolo, solubile in etere, benzene, acido acetico, cloroformio, tetracloruro di carbonio e disolfuro di carbonio. La soluzione presenta fluorescenza blu. Le posizioni 1, 4, 5, 8 sono le stesse, note come α-posizione; le posizioni 2, 3, 6, 7 sono anche le stesse, note come β-posizione; le posizioni 9, 10 sono le stesse, note come ?-posizione. La sua proprietà chimica è tra naftalene e antracene. Può anche avere una reazione di aggiunta nella posizione 9, 10, ma non così facile come l’antracene. L’ossidazione si verifica anche nella posizione 9, 10 con ossidazione che dà fenantrenequinone. Possono anche verificarsi reazioni di sostituzione. Può anche essere ottenuto attraverso la separazione dalla frazione di olio di antracene dell’olio di catrame di carbone. Il fenantrene può essere utilizzato nella produzione di pesticidi e coloranti, ma anche come stabilizzatore dell’alta efficienza & pesticidi a bassa tossicità ed esplosivi in polvere senza fumo.
Il fenantrene può essere usato per produrre coloranti, farmaci e resine dopo la trasformazione di conversione. Il fenantrenequinone dei prodotti di ossidazione può essere usato come coloranti, fungicidi e inibitori della polimerizzazione; 9, l’acido dicarbossilico 10-bifenil è usato per produrre poliestere e resina alchidica; 9, l’acido 10-diidro-9-fenatroico è un ormone stimolante la crescita delle piante; Il peridrofenantrene fatto attraverso l’idrogenazione del fenantrene può essere utilizzato nella produzione di carburante per aerei;il suo prodotto solfonato, l’acido
Il liquore madre contenente fenantrene durante la produzione di antracene raffinato con metodo solvente, dopo il recupero del solvente e l’ulteriore filtrazione della cristallizzazione, può dare fenantrene grezzo contenente il 40% di fenantrene.
Il fenantrene grezzo, dopo aver rimosso i solventi residui nel bollitore di fusione e poi rettificato nella torre di rettifica con 20 piastre teoriche, le frazioni da 335 a 340 °C vengono tagliate, seguite da raffreddamento, cristallizzazione e filtraggio per ottenere il fenantrene industriale con il contenuto di fenantrene superiore al 70%. .
Le informazioni di cui sopra è compilato da Tongtong da Chemicalbook.
Struttura molecolare
La struttura molecolare di fenantrene e antracene sono simili tra loro con tutti gli atomi situati nello stesso piano, ma non nella stessa linea, essendo un sistema coniugato chiuso con proprietà aromatiche. 1, 2, 3, 4, 10 posizioni e 5, 6, 7, 8, 9 posizioni all’interno delle quali corrispondono, rispettivamente, ma c’erano differenze nelle attività in 5 posizioni, tra le quali 9 e 10 avevano maggiore attività con sostituzione di ossidazione e oltre che si verificano in 9 e 10 posizioni: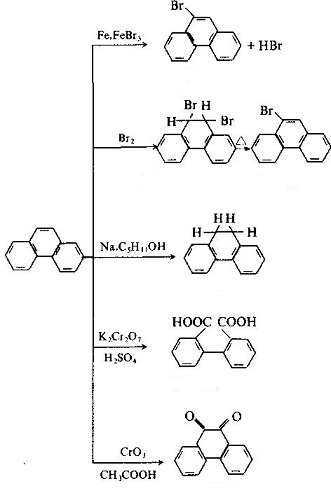
Phenanthrenequinone è un antiparassitario usato come germicida di semi di medicazione, essere in grado di evitare crosta di grano, duro smut e patate dolci macchia nera.
Il fenantrene industriale è derivato dalla distillazione di olio di antracene derivato dal distillato di catrame di carbone. Molti generi di prodotti naturali (quali gli steroli) contengono questo sistema dell’anello. Il fenantrene è utilizzato principalmente nella produzione di coloranti, droghe, alta efficienza e bassa tossicità dei pesticidi e può essere utilizzato come scintillanti, stabilizzatore di polvere senza fumo. Molti dei derivati del fenantrene hanno effetti fisiologici cancerogeni. Come: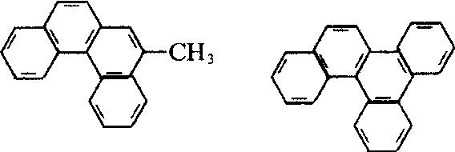
La struttura molecolare di 2-metil-3, 4-benzofenantrene e 1, 2, 3, 4-dibenzofene
Proprietà chimiche
Appare come lucentezza bianca e cristalli di scaglie fluorescenti. Non è solubile in acqua, leggermente solubile in etanolo, solubile in etere, acido acetico, benzene, tetracloruro di carbonio e disolfuro di carbonio.
Usi
Può essere utilizzato per la produzione di fenantrenequinone, resina sintetica, pesticidi e conservanti e così via.
Il fenantrene, attraverso l’ossidazione, può dare fenantrenequinone, da utilizzare per sostituire i pesticidi organici mercuriali ceresin e gallotox. L’acido bifenilico ottenuto dalla sua ossidazione può essere utilizzato per preparare la resina alchidica. L’ossidazione del fenantrene può anche dare anidride, cicloesanone e fenolo. I prodotti di clorazione del fenantrene possono essere utilizzati per produrre isolanti e impregnanti elettrici non infiammabili. L’acido solfonato fenantrene solfonico può essere fatto di legante, concia e così via. Ma in realtà la maggior parte di queste applicazioni devono ancora essere sviluppate. Nell’industria della carta, il fenantrene può essere usato come agente antifogging della polpa; può anche essere usato per gli esplosivi della nitroglicerina e lo stabilizzatore della nitrocellulosa e per la fabbricazione di bomba fumogena; l’ossido solido di fenantrene può essere fatto dei materiali isolanti elettrici ignifughi eccellenti e dei riempitivi. In medicina, il fenantrene può essere utilizzato per sintetizzare alcaloidi-morfina e caffeina, dimetil morfina e farmaci con effetti fisiologici speciali su molti organi riproduttivi. Nell’industria della tintura, il fenantrene può essere fatto di chinone 2-aminofenantrene, benzantrone, colorante di riduzione del solfuro (blu BO, nero BB e marrone) e così via. Inoltre, l’industria della plastica, gli agenti concianti sintetici e il fenantrene, ad alta temperatura e alta pressione, possono subire idrogenazione per ottenere idrofenantrene, essendo il carburante degli aerei a reazione senior.
Per la determinazione del peso molecolare e la sintesi di composti organici.
Preparazione
Il fenantrene è un contenuto relativamente elevato di catrame di carbone, pari al 5% di catrame di carbone, secondo solo al contenuto di naftalene. L’olio di antracene nella gamma di frazioni 300-360 ℃ del catrame di carbone ha il più alto contenuto di fenantrene, seguito da antracene e carbazolo e così via. Il metodo di estrazione del fenantrene viene solitamente inviato all’olio di antracene per il raffreddamento, la cristallizzazione e quindi la filtrazione sotto vuoto o la separazione centrifuga per la separazione dell’olio. La quantità relativamente elevata di fenoli solubili negli oli può essere recuperata utilizzando il metodo di distillazione di precisione. Il cristallo ottenuto è chiamato antracene grezzo, che contiene il 25-30% di antracene, il 22-25% di carbazolo e il 30% di fenantrene. L’antracene grezzo può essere soggetto a estrazione pesante di benzene, raffreddamento, filtrazione con il filtrato cotto a vapore dal solvente prima della ricristallizzazione e della filtrazione. Prendi il filtrato per la distillazione in modo da poter ottenere fenantrene industriale con sulfonazione per ottenere fenantrene fine.
Proprietà chimiche
cristalli bianchi
Proprietà chimiche
Il fenantrene è una sostanza cristallina bianca. Odore aromatico debole. Gli idrocarburi policiclici aromatici (IPA) sono composti contenenti più anelli benzenici e sono anche chiamati idrocarburi aromatici polinucleari.
Proprietà fisiche
Cristalli monoclinici incolori con un debole odore aromatico
Usi
Il fenantrene è un idrocarburi policiclici aromatici, un inquinante ambientale.
Utilizza idrocarburi policiclici aromatici marcati
come microinquinanti.
Definizione
ChEBI: Un idrocarburo policiclico aromatico composto da tre anelli di benzene fusi che prende il nome dai due termini “fenile” e ” antracene.”
Metodi di produzione
Il fenantrene si trova nel catrame di carbone e può essere isolato da diversi tipi di petrolio greggio.
Sintesi di riferimento(s)
Journal of Heterocyclic Chemistry, 30, p. 291, 1993 DOI: 10.1002 / jhet.5570300151
The Journal of Organic Chemistry, 18, p. 801, 1953 DOI: 10.1021/jo50013a004
Tetrahedron Letters, 15, p. 495, 1974
Descrizione generale
Cristalli monoclinici incolori con un debole odore aromatico. Le soluzioni presentano una fluorescenza blu.
Aria & Reazioni dell’acqua
Insolubile in acqua.
Profilo di reattività
Il fenantrene può reagire con materiali ossidanti .
Pericolo per la salute
La tossicità orale acuta del fenantrene è low.It è più tossico dell’antracene. Un valore orale ld50 nei topi è riportato a 700 mg / kg. Può causare tumore nella pelle nel sito di applicazione.L’evidenza di cancerogenicità negli animali, tuttavia, è inadeguata.
Pericolo di incendio
Il fenantrene è combustibile.
Profilo di sicurezza
Veleno per via endovenosa. Moderatamente tossico per ingestione. Dati di mutazione riportati. Un fotosensibilizzatore della pelle umana. Cancerogeno discutibile con dati sperimentali neoplastigenici e tumorigeni per contatto con la pelle. Combustibile quando esposto al calore o alla fiamma; può reagire vigorosamente con materiali ossidanti. Per combattere il fuoco, utilizzare acqua, schiuma, CO2, chimica secca. Quando riscaldato a decomposizione emette fumo acre e fumi irritanti
Esposizione potenziale
La polvere può formare una miscela esplosiva con l’aria. Incompatibile con ossidanti (clorati, nitrati, perossidi, permanganati, perclorati, cloro, bromo, fluoro, ecc.); il contatto può causare incendi o esplosioni. Tenere lontano da materiali alcalini, basi forti, acidi forti, ossoacidi, epossidi.
Cancerogenicità
Il fenantrene è inefficace come aniniziatore. Non è classificabile per quanto riguarda la cancerogenicità umana—classe 3 da IARC e classe D da IRIS, sulla base di dati non umani e dati inadeguati provenienti da un singolo studio di gavagest nei ratti e studi di pittura cutanea e iniezione inmice.
Fonte
Rilevata nelle acque sotterranee sotto un ex impianto di gassificazione del carbone a Seattle, WA alla concentrazione di 130 µg / L (ASTR, 1995). Rilevato in 8 combustibili diesel a concentrazioni comprese tra 0,17 e 110 mg / L con un valore medio di 41,43 mg/L (Westerholm e Li, 1994) e in frazioni solubili in acqua distillate di olio motore nuovo e usato a concentrazioni rispettivamente di 1,9-2,1 e 2,1–2,2 µg/L (Chen et al., 1994). Lee et al. (1992) ha riportato intervalli di concentrazione da 100 a 300 mg/L e da 15 a 25 µg/L nel gasolio e nella corrispondente fase acquosa (acqua distillata),rispettivamente. Schauer et al. (1999) ha riportato fenantrene nel carburante diesel ad una concentrazione di 57µg/g e in uno scarico per autocarri a uso medio a motore diesel ad una velocità di emissione di 93,1 µg/km.Identificato negli oli grezzi del Kuwait e della Louisiana meridionale a concentrazioni di 26 e 70 ppm,rispettivamente (Pancirov e Brown, 1975). Il gasolio ottenuto da una stazione di servizio di Schlieren,in Svizzera, conteneva fenantrene ad una concentrazione stimata di 327 mg / L (Schluep et al.,2001).
Il fenantrene è stato rilevato nei fumi dell’asfalto ad una concentrazione media di 57,73 ng/m3 (Wanget al., 2001).
Thomas e Delfino (1991) acque sotterranee equilibrate senza contaminanti raccolte da Gainesville, FL con singole frazioni di tre singoli prodotti petroliferi a 24-25 °C per24 h. La fase acquosa è stata analizzata per composti organici tramite il metodo di prova approvato dagli Stati Uniti epa625. Il fenantrene è stato rilevato solo nella frazione idrosolubile del gasolio ad una concentrazione media di 17 µg / L.
Sulla base di analisi di laboratorio di 7 campioni di catrame di carbone, le concentrazioni di fenantrene variavano da 3.100 a 35.000 ppm (EPRI,1990). Rilevato in film di catrame di carbone invecchiato 1-yr e catrame di carbone sfuso a concentrazione anidentica di 10.000 mg / kg (Nelson et al., 1996). Una tara di carbone ad alta temperatura conteneva fenantrene ad una concentrazione media di 2,66% in peso (McNeil, 1983). Identificato anche nelle piazzole di catrame di carbone ad alta temperatura a concentrazioni che vanno da 7.500 a 40.300 mg / kg (Arrendale e Rogers, 1981). Lee et al. (1992a) equilibra otto catrami di carbone con acqua distillata a 25 °C. La concentrazione massima di fenantrene osservata nella fase acquosa è di 0,4 mg/L.
Nove campioni di creosoto disponibili in commercio contenevano fenantrene a concentrazioni comprese tra 48.000 e 120.000 mg/kg (Kohler et al., 2000).
La concentrazione tipica di fenantrene in un olio di pirolisi pesante è del 2,5% in peso (Chevron Phillips,maggio 2003).
Destino ambientale
Biologico. Il catecolo è il metabolita centrale nella degradazione batterica del fenantrene.I sottoprodotti intermedi includono acido 1-idrossi-2-naftoico, 1,2-diidrossinaftalene e acido salicilico (Chapman, 1972; Hou, 1982). È stato riferito che Beijerinckia, in condizioni aerobiccondizioni, ha degradato il fenantrene a cis-3,4-diidrossi-3,4-diidrofenantracene (Kobayashiand Rittman, 1982).
Terreno. Le emivita riportate per fenantrene in un Kidman sandy loam e McLaurin sandyloam sono 16 e 35 d, rispettivamente (Park et al., 1990). Manilal e Alexander (1991) hanno riportato una mezza vita di 11 d in un terreno di Kendaia.
Acque superficiali. In un corpo idrico superficiale profondo 5 m, le emivite calcolate per la trasformazione fotochimica diretta a 40 ° N di latitudine in piena estate durante il mezzogiorno erano rispettivamente di 59 e 69 d con e senza partizionamento sedimento-acqua (Zepp e Schlotzhauer, 1979).
Fotolitico. Una resa di anidride carbonica del 24,2% è stata raggiunta quando il fenantrene adsorbito onsilica gel è stato irradiato con luce (λ >290 nm) per 17 h (Freitag et al., 1985). In un esperimento 2-wk, il fenantrene applicato alle sospensioni suolo-acqua in condizioni aerobiche e anaerobiche ha dato rese 14CO2 di 7.2 e 6.3%, rispettivamente (Scheunert et al., 1987). Matsuzawa etal. (2001) ha studiato la degradazione fotochimica di cinque idrocarburi policiclici aromatici indiesel particolato depositato sul terreno e in vari componenti del suolo. La degradazione fotochimica mediante luce solare artificiale è stata realizzata utilizzando una lampada allo xeno da 900 W.La luce di questa lampada è stata fatta passare attraverso un filtro di vetro per eliminare la luce di lunghezze d’onda più corte (λ2. Inoltre, un simulatore solare dotato di una lampada allo xeno da 300 W è stato utilizzato per fornire la massima intensità di luce solare osservata a Tokyo (latitudine 35,5 °N). L’emivita del fenantrene nel particolato diesel utilizzando fonti da 900 e 300 W era rispettivamente di 4,29 e 60,63 h. Le seguenti emivite sono state determinate per il fenantrene adsorbito su vari componenti del suolo utilizzando apparecchi da 900 W: 3,04 ore per quarzo,2,90 ore per feldspato, 1,15 ore per caolinite, 4,97 ore per montmorillonite, 3,26 ore per gel di silice e 1,17 ore per allumina.
Chimico / fisico. La clorazione acquosa di fenantrene a pH 8,8), fenantrene-9,10-ossido, fenantrene-9,10-dione e 9,10-diidrofenantrendiolo sono stati identificati come prodotti principali (Oyler et al.,1983). È stato suggerito che la clorazione del fenantrene nell’acqua del rubinetto rappresentasse la presenza di cloro e diclorofenantreni (Shiraishi et al., 1985).
Spedizione
UN3077 Sostanze pericolose per l’ambiente, solido, n.a.s., Classe di pericolo: 9; Etichette: 9-Materiale pericoloso vario, Nome tecnico richiesto.
Metodi di purificazione
I probabili contaminanti includono antracene, carbazolo, fluorene e altri idrocarburi policiclici. Purificarlo per distillazione da sodio sotto vuoto, bollitura con anidride maleica in xilene, cristallizzazione da acido acetico, sublimazione e fusione di zona. Inoltre è stato ricristallizzato ripetutamente da EtOH, * benzene o etere pet (b 60-70o), con successiva essiccazione sotto vuoto su P2O5 in una pistola Abderhalden. Feldman, Pantages e Orchin hanno separato la maggior parte dell’impurità dell’antracene rifluendo il fenantrene (671g) con anidride maleica (194g) in xilene (1,25 L) sotto azoto per 22 ore, quindi filtrato. Il filtrato è stato estratto con NaOH acquoso al 10%, la fase organica è stata separata e il solvente è stato evaporato. Il residuo, dopo aver mescolato per 2 ore con 7 g di sodio, è stato distillato sotto vuoto, quindi ricristallizzato due volte dal 30% *di benzene in EtOH. È stato poi sciolto in acido acetico caldo (2,2 mL/g), e ad esso è stata aggiunta lentamente una soluzione acquosa di CrO3 (60g in 72mL H2O più 2,2 L di acido acetico), seguita da lenta aggiunta di conc H2SO4 (30mL). La miscela è stata rifusa per 15minuti, diluiti con un volume uguale di acqua e raffreddati. Il precipitato è stato filtrato, lavato con acqua, essiccato e distillato, quindi ricristallizzato due volte da EtOH. Un’ulteriore purificazione è possibile mediante cromatografia da una soluzione di CHCl3 su allumina attivata ,con * benzene come eluente e raffinazione di zona. Il picrato (1:1) forma aghi giallo oro con m 146o, e lo styphnate (1:1) ha m 138-139o (piastre o aghi da EtOH o EtOH/H2O rispettivamente).
Smaltimento dei rifiuti
Consultare le agenzie di regolamentazione ambientale per indicazioni sulle pratiche di smaltimento accettabili. I generatori di rifiuti contenenti questo contaminante (≥100 kg / mo) devono essere conformi alle normative EPA che disciplinano lo stoccaggio, il trasporto, il trattamento e lo smaltimento dei rifiuti.