Vicodin ES
Nome generico: paracetamolo e idrocodone bitartrato
Forma di dosaggio: tablet
Medicamente recensito da Drugs.com. Ultimo aggiornamento il 22 luglio 2020.
- Effetti Collaterali
- Dosaggio
- Professional
- Interazioni
- Gravidanza
- Recensioni
- Più
Il Vicodin ES di marca è stato sospeso negli stati UNITI Se le versioni generiche di questo prodotto sono stati approvati dalla FDA, ci possono essere equivalenti generici disponibili.
- Avvertenza
- Vicodin ES Descrizione
- Vicodin ES-Farmacologia clinica
- Farmacocinetica
- Indicazioni e utilizzo per Vicodin ES
- Controindicazioni
- Avvertenze
- Epatotossicità
- Ipersensibilità/anafilassi
- Depressione respiratoria
- Trauma cranico e aumento della pressione intracranica
- Condizioni addominali acute
- Precauzioni
- Generale
- Informazioni per pazienti / operatori sanitari
- Test di laboratorio
- Interazioni farmacologiche
- Interazioni farmaco/test di laboratorio
- Carcinogenesi, mutagenesi, compromissione della fertilità
- Gravidanza
- Travaglio e parto
- Madri che allattano
- Uso pediatrico
- Uso geriatrico
- Reazioni avverse
- Sistema nervoso centrale
- Sistema gastrointestinale
- Sistema genito-urinario
- Depressione respiratoria
- Sensi speciali
- Dermatologico
- Abuso e dipendenza da droghe
- Sostanza controllata
- Abuso e dipendenza
- Sovradosaggio
- Segni e sintomi
- Trattamento
- Vicodin ES Dosaggio e somministrazione
- Come Vicodin ES in Dotazione
- STORAGE
- More about Vicodin ES (acetaminophen / hydrocodone)
- Professional resources
- Guide di trattamento correlate
Avvertenza
IL PARACETAMOLO È STATO ASSOCIATO A CASI DI INSUFFICIENZA EPATICA ACUTA, A VOLTE CON CONSEGUENTE TRAPIANTO DI FEGATO E MORTE. LA MAGGIOR PARTE DEI CASI DI DANNO EPATICO SONO ASSOCIATI ALL’USO DI PARACETAMOLO A DOSI SUPERIORI A 4000 MILLIGRAMMI AL GIORNO E SPESSO COINVOLGONO PIÙ DI UN PRODOTTO CONTENENTE PARACETAMOLO.
Vicodin ES Descrizione
Idrocodone bitartrato e paracetamolo è fornito in forma di compresse per somministrazione orale.
ATTENZIONE: Può essere assuefazione (vedere PRECAUZIONI, informazioni per i pazienti / operatori sanitari, e l’ABUSO DI DROGA E LA DIPENDENZA).
L’idrocodone bitartrato è un analgesico oppioide e antitosse e si presenta come cristalli fini, bianchi o come polvere cristallina. È influenzato dalla luce. Il nome chimico è 4,5 α-epoxy-3-methoxy-17-methylmorphinan-6-one tartrate (1:1) hydrate (2: 5). Ha la seguente formula di struttura:
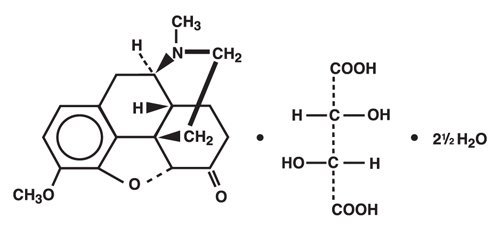 C18H21NO3 * C4H6O6 * 2½H2O MW = 494.490
C18H21NO3 * C4H6O6 * 2½H2O MW = 494.490
Acetaminofene, 4 ‘ – hydroxyacetanilide, una polvere cristallina leggermente amara, bianca, inodore, è un analgesico non oppiaceo, non salicilato e antipiretico. Ha la seguente formula strutturale:
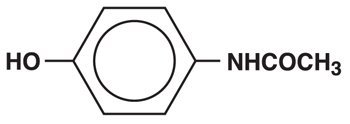 C8H9NO2 M. W. = 151.16
C8H9NO2 M. W. = 151.16
Idrocodone bitartrato e paracetamolo compresse, USP è disponibile nei seguenti punti di forza:
VICODIN®: Idrocodone bitartrato….. 5 mg
ATTENZIONE: Può essere assuefazione.
Paracetamolo….. 300 mg
Vicodin ES®: Idrocodone bitartrato….. 7,5 mg
ATTENZIONE: Può essere assuefazione.
Paracetamolo….. 300 mg
VICODIN HP®: Idrocodone bitartrato….. 10 mg
ATTENZIONE: Può essere assuefazione.
Paracetamolo….. 300 mg
Inoltre ogni compressa contiene i seguenti ingredienti inattivi: biossido di silicio colloidale, crospovidone, magnesio stearato, cellulosa microcristallina, povidone, amido pregelatinizzato e acido stearico.
Questo prodotto è conforme alla prova di dissoluzione USP 2.
Vicodin ES-Farmacologia clinica
L’idrocodone è un analgesico narcotico semisintetico e antitosse con molteplici azioni qualitativamente simili a quelle della codeina. La maggior parte di questi coinvolge il sistema nervoso centrale e la muscolatura liscia. Il meccanismo preciso di azione dell’idrocodone e di altri oppiacei non è noto, anche se si ritiene che si riferisca all’esistenza di recettori oppiacei nel sistema nervoso centrale. Oltre all’analgesia, i narcotici possono produrre sonnolenza, cambiamenti di umore e annebbiamento mentale.
L’azione analgesica del paracetamolo comporta influenze periferiche, ma il meccanismo specifico è ancora indeterminato. L’attività antipiretica è mediata attraverso centri di regolazione del calore ipotalamico. Il paracetamolo inibisce la prostaglandina sintetasi. Le dosi terapeutiche di paracetamolo hanno effetti trascurabili sui sistemi cardiovascolari o respiratori; tuttavia, le dosi tossiche possono causare insufficienza circolatoria e respirazione rapida e superficiale.
Farmacocinetica
Il comportamento dei singoli componenti è descritto di seguito.
Idrocodone
Dopo una dose orale di 10 mg di idrocodone somministrata a cinque soggetti maschi adulti, la concentrazione media di picco è stata di 23,6 ± 5,2 ng / mL. I livelli sierici massimi sono stati raggiunti a 1,3 ± 0,3 ore e l’emivita è stata determinata a 3,8 ± 0,3 ore. Idrocodone presenta un modello complesso di metabolismo tra cui O-demetilazione, N-demetilazione e 6-cheto riduzione ai corrispondenti 6 – α-e 6-β – idrossi-metaboliti. Vedere SOVRADOSAGGIO per informazioni sulla tossicità.
Paracetamolo
Il paracetamolo viene rapidamente assorbito dal tratto gastrointestinale ed è distribuito in tutta la maggior parte dei tessuti del corpo. L ‘ emivita plasmatica è compresa tra 1,25 e 3 ore, ma può essere aumentata a causa di danni al fegato e dopo sovradosaggio. L ‘ eliminazione del paracetamolo avviene principalmente attraverso il metabolismo epatico (coniugazione) e la successiva escrezione renale dei metaboliti. Circa l ‘ 85% di una dose orale appare nelle urine entro 24 ore dalla somministrazione, la maggior parte come glucuronide coniugato, con piccole quantità di altri coniugati e farmaco immodificato. Vedere SOVRADOSAGGIO per informazioni sulla tossicità.
Indicazioni e utilizzo per Vicodin ES
Le compresse di idrocodone bitartrato e paracetamolo sono indicate per il sollievo dal dolore da moderato a moderatamente grave.
Controindicazioni
Questo prodotto non deve essere somministrato a pazienti che hanno precedentemente mostrato ipersensibilità all’idrocodone o al paracetamolo.
I pazienti noti per essere ipersensibili ad altri oppioidi possono mostrare sensibilità crociata all ‘ idrocodone.
Avvertenze
Epatotossicità
Il paracetamolo è stato associato a casi di insufficienza epatica acuta, a volte con conseguente trapianto di fegato e morte. La maggior parte dei casi di danno epatico sono associati all’uso di paracetamolo a dosi superiori a 4000 milligrammi al giorno e spesso coinvolgono più di un prodotto contenente paracetamolo. L’assunzione eccessiva di paracetamolo può essere intenzionale per causare autolesionismo o involontario come i pazienti tentano di ottenere più sollievo dal dolore o inconsapevolmente prendere altri prodotti contenenti paracetamolo.
Il rischio di insufficienza epatica acuta è maggiore negli individui con malattia epatica sottostante e negli individui che ingeriscono alcol durante l’assunzione di paracetamolo.
Istruire i pazienti a cercare paracetamolo o APAP sulle etichette delle confezioni e a non utilizzare più di un prodotto contenente paracetamolo. Istruire i pazienti a rivolgersi al medico immediatamente dopo l’ingestione di più di 4000 milligrammi di paracetamolo al giorno, anche se si sentono bene.
Reazioni cutanee gravi
Raramente, il paracetamolo può causare gravi reazioni cutanee come pustolosi esantematosa generalizzata acuta (AGEP), sindrome di Stevens-Johnson (SJS) e necrolisi epidermica tossica (TEN), che possono essere fatali. I pazienti devono essere informati sui segni di gravi reazioni cutanee e l’uso del farmaco deve essere interrotto alla prima comparsa di eruzione cutanea o qualsiasi altro segno di ipersensibilità.
Ipersensibilità/anafilassi
Ci sono state segnalazioni post-marketing di ipersensibilità e anafilassi associate all’uso di paracetamolo. I segni clinici includevano gonfiore del viso, della bocca e della gola, difficoltà respiratoria, orticaria, eruzione cutanea, prurito e vomito. Ci sono state segnalazioni infrequenti di anafilassi pericolosa per la vita che richiedono cure mediche di emergenza. Istruire i pazienti a interrompere immediatamente le compresse di idrocodone bitartrato e paracetamolo e rivolgersi al medico se manifestano questi sintomi. Non prescrivere compresse di idrocodone bitartrato e paracetamolo per pazienti con allergia al paracetamolo.
Depressione respiratoria
A dosi elevate o in pazienti sensibili, l’idrocodone può produrre depressione respiratoria dose-correlata agendo direttamente sul centro respiratorio del tronco cerebrale. L’idrocodone inoltre pregiudica il centro che controlla il ritmo respiratorio e può produrre la respirazione irregolare e periodica.
Trauma cranico e aumento della pressione intracranica
Gli effetti depressivi respiratori dei narcotici e la loro capacità di elevare la pressione del liquido cerebrospinale possono essere marcatamente esagerati in presenza di trauma cranico, altre lesioni intracraniche o un preesistente aumento della pressione intracranica. Inoltre, i narcotici producono reazioni avverse che possono oscurare il decorso clinico dei pazienti con lesioni alla testa.
Condizioni addominali acute
La somministrazione di narcotici può oscurare la diagnosi o il decorso clinico di pazienti con condizioni addominali acute.
Precauzioni
Generale
Particolari di Pazienti a Rischio
Come con qualsiasi narcotico agente analgesico, bitartrato di hydrocodone e acetaminofene compresse deve essere usato con cautela in pazienti anziani o pazienti debilitati e quelli con grave compromissione epatica o renale, ipotiroidismo, morbo di Addison, ipertrofia prostatica o stenosi dell’uretra. Le precauzioni usuali dovrebbero essere osservate e la possibilità di depressione respiratoria dovrebbe essere tenuta presente.
Riflesso della tosse
L’idrocodone sopprime il riflesso della tosse; come con tutti i narcotici, si deve usare cautela quando le compresse di idrocodone bitartrato e paracetamolo vengono utilizzate postoperatorie e in pazienti con malattia polmonare.
Informazioni per pazienti / operatori sanitari
- Non assumere idrocodone bitartrato e paracetamolo compresse se si è allergici a uno qualsiasi dei suoi ingredienti.
- Se sviluppa segni di allergia come eruzione cutanea o difficoltà respiratorie, smetta di prendere le compresse di idrocodone bitartrato e paracetamolo e contatti immediatamente il medico.
- Non assumere più di 4000 milligrammi di paracetamolo al giorno. Chiamate il vostro medico se avete preso più della dose raccomandata.
L’idrocodone, come tutti i narcotici, può compromettere le capacità mentali e / o fisiche necessarie per l’esecuzione di compiti potenzialmente pericolosi come guidare un’automobile o utilizzare macchinari; i pazienti devono essere avvertiti di conseguenza.
L’alcol e altri depressivi del SNC possono produrre una depressione aggiuntiva del SNC, se assunti con questo prodotto di combinazione, e devono essere evitati.
Idrocodone può essere assuefazione. I pazienti devono assumere il farmaco solo per tutto il tempo prescritto, nelle quantità prescritte e non più frequentemente di quanto prescritto.
Test di laboratorio
Nei pazienti con grave malattia epatica o renale, gli effetti della terapia devono essere monitorati con test seriali di funzionalità epatica e / o renale.
Interazioni farmacologiche
I pazienti che ricevono altri narcotici, antistaminici, antipsicotici, agenti ansiolitici o altri depressivi del SNC (incluso l’alcol) in concomitanza con idrocodone bitartrato e compresse di paracetamolo possono mostrare una depressione aggiuntiva del SNC. Quando è prevista la terapia combinata, la dose di uno o entrambi gli agenti deve essere ridotta.
L’uso di inibitori MAO o antidepressivi triciclici con preparazioni di idrocodone può aumentare l’effetto dell’antidepressivo o dell’idrocodone.
Interazioni farmaco/test di laboratorio
Il paracetamolo può produrre risultati falsi positivi per l’acido 5-idrossiindoleacetico urinario.
Carcinogenesi, mutagenesi, compromissione della fertilità
Non sono stati condotti studi adeguati negli animali per determinare se idrocodone o paracetamolo abbiano un potenziale di carcinogenesi, mutagenesi o compromissione della fertilità.
Gravidanza
Effetti teratogeni
Categoria di gravidanza C
Non esistono studi adeguati e ben controllati in donne in gravidanza. Le compresse di idrocodone bitartrato e paracetamolo devono essere utilizzate durante la gravidanza solo se il potenziale beneficio giustifica il potenziale rischio per il feto.
Effetti non teratogeni
I bambini nati da madri che hanno assunto regolarmente oppioidi prima del parto saranno fisicamente dipendenti. I segni di astinenza includono irritabilità e pianto eccessivo, tremori, riflessi iperattivi, aumento della frequenza respiratoria, aumento delle feci, starnuti, sbadigli, vomito e febbre. L’intensità della sindrome non è sempre correlata alla durata dell’uso o della dose materna di oppioidi. Non c’è consenso sul metodo migliore per gestire il ritiro.
Travaglio e parto
Come con tutti i narcotici, la somministrazione di questo prodotto alla madre poco prima del parto può causare un certo grado di depressione respiratoria nel neonato, specialmente se vengono utilizzate dosi più elevate.
Madri che allattano
Il paracetamolo viene escreto nel latte materno in piccole quantità, ma il significato dei suoi effetti sui neonati che allattano non è noto. Non è noto se l ‘ idrocodone sia escreto nel latte materno. Poiché molti farmaci sono escreti nel latte umano e a causa del potenziale di gravi reazioni avverse nei bambini che allattano da idrocodone e paracetamolo, deve essere presa la decisione se interrompere l’allattamento o interrompere il farmaco, tenendo conto dell’importanza del farmaco per la madre.
Uso pediatrico
La sicurezza e l’efficacia nei pazienti pediatrici non sono state stabilite.
Uso geriatrico
Gli studi clinici sulle compresse di idrocodone bitartrato e paracetamolo non hanno incluso un numero sufficiente di soggetti di età pari o superiore a 65 anni per determinare se rispondono in modo diverso rispetto ai soggetti più giovani. Altre esperienze cliniche riportate non hanno identificato differenze nelle risposte tra pazienti anziani e pazienti più giovani. In generale, la selezione della dose per un paziente anziano deve essere cauta, di solito a partire dalla fascia bassa del range di dosaggio, riflettendo la maggiore frequenza di diminuzione della funzionalità epatica, renale o cardiaca e della malattia concomitante o di altre terapie farmacologiche.
L’idrocodone e i principali metaboliti del paracetamolo sono noti per essere sostanzialmente escreti dal rene. Pertanto il rischio di reazioni tossiche può essere maggiore nei pazienti con funzionalità renale compromessa a causa dell’accumulo del composto progenitore e/o dei metaboliti nel plasma. Poiché i pazienti anziani hanno maggiori probabilità di avere una ridotta funzionalità renale, si deve prestare attenzione nella selezione della dose e può essere utile monitorare la funzionalità renale.
L ‘ idrocodone può causare confusione e sovra-sedazione negli anziani; i pazienti anziani devono generalmente iniziare con basse dosi di idrocodone bitartrato e compresse di paracetamolo e essere osservati attentamente.
Reazioni avverse
Le reazioni avverse più frequentemente riportate sono vertigini, capogiri, sedazione, nausea e vomito. Questi effetti sembrano essere più evidenti nei pazienti ambulatoriali che nei pazienti non ambulatoriali, e alcune di queste reazioni avverse possono essere alleviate se il paziente si sdraia.
Altre reazioni avverse includono:
Sistema nervoso centrale
Sonnolenza, annebbiamento mentale, letargia, compromissione delle prestazioni mentali e fisiche, ansia, paura, disforia, dipendenza psichica, cambiamenti di umore.
Sistema gastrointestinale
La somministrazione prolungata di idrocodone bitartrato e compresse di paracetamolo può produrre stitichezza.
Sistema genito-urinario
Con gli oppiacei sono stati riportati spasmo ureterale, spasmo degli sfinteri vescicali e ritenzione urinaria.
Depressione respiratoria
L’idrocodone bitartrato può produrre depressione respiratoria dose-correlata agendo direttamente sui centri respiratori del tronco cerebrale (vedere SOVRADOSAGGIO).
Sensi speciali
Casi di compromissione dell’udito o perdita permanente sono stati riportati prevalentemente in pazienti con sovradosaggio cronico.
Dermatologico
Eruzione cutanea, prurito.
I seguenti eventi avversi del farmaco possono essere tenuti in considerazione come potenziali effetti del paracetamolo: reazioni allergiche, eruzioni cutanee, trombocitopenia, agranulocitosi.
Gli effetti potenziali di un dosaggio elevato sono elencati nella sezione SOVRADOSAGGIO.
Abuso e dipendenza da droghe
Sostanza controllata
Le compresse di idrocone bitartrato e paracetamolo sono classificate come sostanze controllate dallo schema III.
Abuso e dipendenza
Dipendenza psichica, dipendenza fisica e tolleranza possono svilupparsi dopo somministrazione ripetuta di narcotici; pertanto, questo prodotto deve essere prescritto e somministrato con cautela. Tuttavia, è improbabile che la dipendenza psichica si sviluppi quando le compresse di idrocodone bitartrato e paracetamolo vengono utilizzate per un breve periodo per il trattamento del dolore.
La dipendenza fisica, la condizione in cui è necessaria la somministrazione continua del farmaco per prevenire la comparsa di una sindrome da astinenza, assume proporzioni clinicamente significative solo dopo diverse settimane di uso narcotico continuato, sebbene un lieve grado di dipendenza fisica possa svilupparsi dopo alcuni giorni di terapia narcotica. La tolleranza, in cui sono necessarie dosi sempre più elevate per produrre lo stesso grado di analgesia, si manifesta inizialmente con una durata ridotta dell’effetto analgesico e successivamente con una diminuzione dell’intensità dell’analgesia. Il tasso di sviluppo della tolleranza varia tra i pazienti.
Sovradosaggio
A seguito di un sovradosaggio acuto, la tossicità può derivare da idrocodone o paracetamolo.
Segni e sintomi
Idrocodone: Il sovradosaggio grave con idrocodone è caratterizzato da depressione respiratoria (diminuzione della frequenza respiratoria e/o del volume delle maree, respirazione di Cheyne-Stokes, cianosi), sonnolenza estrema che progredisce fino a stupore o coma, flaccidità muscolare scheletrica, pelle fredda e umida e talvolta bradicardia e ipotensione. In caso di sovradosaggio grave, possono verificarsi apnea, collasso circolatorio, arresto cardiaco e morte.
Paracetamolo: Nel sovradosaggio da paracetamolo: la necrosi epatica dose-dipendente e potenzialmente fatale è l’effetto avverso più grave. Possono verificarsi anche necrosi tubulare renale, coma ipoglicemico e difetti di coagulazione.
I primi sintomi a seguito di un sovradosaggio potenzialmente epatotossico possono includere: nausea, vomito, diaforesi e malessere generale. Le evidenze cliniche e di laboratorio di tossicità epatica potrebbero non essere evidenti fino a 48-72 ore dopo l’ingestione.
Trattamento
Un sovradosaggio di farmaci singolo o multiplo con idrocodone e paracetamolo è un sovradosaggio di polidroga potenzialmente letale e si raccomanda la consultazione con un centro antiveleni regionale.
Il trattamento immediato include il supporto della funzione cardiorespiratoria e misure per ridurre l’assorbimento del farmaco.
Ossigeno, liquidi per via endovenosa, vasopressori e altre misure di supporto devono essere impiegati come indicato. Deve essere presa in considerazione anche la ventilazione assistita o controllata.
In caso di sovradosaggio da idrocodone, si deve prestare la massima attenzione al ripristino di un adeguato scambio respiratorio attraverso la fornitura di una via aerea brevettata e l’istituzione di una ventilazione assistita o controllata. L’antagonista narcotico naloxone cloridrato è un antidoto specifico contro la depressione respiratoria che può derivare da sovradosaggio o ipersensibilità ai narcotici, incluso l’idrocodone. Poiché la durata d ‘azione dell’ idrocodone può superare quella dell ‘antagonista, il paziente deve essere tenuto sotto continua sorveglianza e dosi ripetute dell’ antagonista devono essere somministrate secondo necessità per mantenere un ‘ adeguata respirazione. Un antagonista narcotico non deve essere somministrato in assenza di depressione respiratoria o cardiovascolare clinicamente significativa.
La decontaminazione gastrica con carbone attivo deve essere somministrata appena prima della N-acetilcisteina (NAC) per diminuire l’assorbimento sistemico se l’ingestione di paracetamolo è nota o sospetta che si sia verificata entro poche ore dalla presentazione. I livelli sierici di paracetamolo devono essere ottenuti immediatamente se il paziente presenta 4 ore o più dopo l’ingestione per valutare il potenziale rischio di epatotossicità; i livelli di paracetamolo prelevati meno di 4 ore dopo l’ingestione possono essere fuorvianti. Per ottenere il miglior risultato possibile, il NAC deve essere somministrato il prima possibile quando si sospetta un danno epatico imminente o in evoluzione. NAC per via endovenosa può essere somministrato quando le circostanze precludono la somministrazione orale.
È necessaria una terapia di supporto vigorosa in caso di intossicazione grave. Le procedure per limitare l’assorbimento continuo del farmaco devono essere prontamente eseguite poiché la lesione epatica è dose-dipendente e si verifica all’inizio del corso dell’intossicazione.
Vicodin ES Dosaggio e somministrazione
Il dosaggio deve essere regolato in base alla gravità del dolore e alla risposta del paziente. Tuttavia, va tenuto presente che la tolleranza all’idrocodone può svilupparsi con l’uso continuato e che l’incidenza di effetti indesiderati è correlata alla dose.
VICODIN® (compresse di idrocodone bitartrato e paracetamolo, USP 5 mg / 300 mg): il solito dosaggio per adulti è di una o due compresse ogni quattro o sei ore, se necessario per il dolore. Il dosaggio giornaliero totale non deve superare 8 compresse.
Vicodin ES® (Idrocodone bitartrato e acetaminofene compresse, USP 7,5 mg / 300 mg): Il solito dosaggio per adulti è di una compressa ogni quattro-sei ore, se necessario per il dolore. Il dosaggio giornaliero totale non deve superare le 6 compresse.
VICODIN HP® (Idrocodone bitartrato e paracetamolo compresse, USP 10 mg / 300 mg): Il solito dosaggio per adulti è di una compressa ogni quattro-sei ore, se necessario per il dolore. Il dosaggio giornaliero totale non deve superare le 6 compresse.
Come Vicodin ES in Dotazione
VICODIN®, Vicodin ES® VICODIN e HP® (Bitartrato di Hydrocodone e Acetaminofene) Compresse, USP sono forniti come segue:
VICODIN® 5 mg/300 mg
Bianco, a forma di capsula, diviso in due compresse, inciso “5” punteggio “300”su un lato e “XANAX” sul lato in bottiglie di 100 e 500 compresse:
Bottiglie di 100 – NDC 0074-3041-13
Bottiglie di 500 – NDC 0074-3041-53
Vicodin ES® 7.5 mg/300 mg
Bianco, a forma di capsula, diviso in due compresse, inciso “7.5” gol “300” su un lato e “Vicodin ES” sul lato in bottiglie di 100 e 500 compresse:
Bottiglie di 100 – NDC 0074-3043-13
Bottiglie di 500 – NDC 0074-3043-53
VICODIN HP® 10 mg/300 mg
Bianco, a forma di capsula, diviso in due compresse, inciso “10” punteggio “300” su un lato e “VICODIN HP” sul lato in bottiglie di 100 e 500 compresse:
Bottiglie di 100 – NDC 0074-3054-13
Bottiglie di 500 – NDC 0074-3054-53
STORAGE
Conservare a 20° e i 25°C (68° a 77°F). .
FARMACISTA: Dispensare in un contenitore stretto e resistente alla luce con una chiusura a prova di bambino.
Un programma III Narcotico
© AbbVie Inc. 2014
Prodotto per
AbbVie Inc.
North Chicago, IL 60064 U. S. A.
Prodotto da:
Mikart, Inc.
Atlanta, GA 30318
1122F00 Rev. 06/14 June, 2014
NDC 0074–3054–53
Vicodin HP® (Hydrocodone Bitartrate and Acetaminophen) Tablets, USP
CIII
10 mg / 300 mg
500 Tablets
Rx only abbvie

NDC 0074–3043–13
Vicodin ES® (Hydrocodone Bitartrate and Acetaminophen) Tablets, USP
CIII
7.5 mg / 300 mg
100 Tablets
Rx only abbvie

NDC 0074–3041–13
Vicodin® (Hydrocodone Bitartrate and Acetaminophen) Tablets, USP
CIII
5 mg / 300 mg
100 Tablets
Rx only abbvie

| VICODIN HP hydrocodone bitartrate and acetaminophen tablet |
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
| Vicodin ES hydrocodone bitartrate and acetaminophen tablet |
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
| VICODIN hydrocodone bitartrate and acetaminophen tablet |
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
Labeler – AbbVie Inc. (078458370)
More about Vicodin ES (acetaminophen / hydrocodone)
- Side Effects
- During Pregnancy
- Dosage Information
- Drug Images
- Drug Interactions
- 15 Reviews
- Drug class: narcotic analgesic combinations
- FDA Alerts (11)
Professional resources
- Prescribing Information
Other brands Norco, Vicodin, Lortab, Hycet, … + 13 più
Guide di trattamento correlate
- Mal di schiena
- Tosse
- Dolore
- Artrite reumatoide
Disclaimer medico