Vitamina C: Un agente antiossidante
Metabolismo redox e proprietà antiossidanti della vitamina C
I radicali liberi e gli ossidanti svolgono un duplice ruolo sia come composti tossici che benefici, nei processi metabolici e in risposta a stimolazioni esogene. Sono prodotti da normali attività metaboliche o da fattori ambientali (inquinamento, fumo di sigaretta e radiazioni). Quando un sovraccarico di radicali liberi non può essere spazzato, il loro accumulo nel corpo genera stress ossidativo . Lo stress ossidativo si verifica quando la formazione di radicali liberi supera la capacità di protezione contro di loro. Questo processo porta allo sviluppo di malattie croniche e degenerative come cancro, malattie autoimmuni, invecchiamento, cataratta, artrite reumatoide, malattie cardiovascolari e neurodegenerative . Un antiossidante è una molecola che impedisce l’ossidazione di altre molecole. Il processo di ossidazione è una reazione chimica che produce radicali liberi, portando a reazioni a catena che possono danneggiare le cellule. L’effetto antiossidante della vitamina C è stato ben documentato . La vitamina C è un potente antiossidante che ha la capacità di donare un atomo di idrogeno e formare un radicale ascorbil-libero relativamente stabile. La vitamina E, la vitamina C e il β-carotene sono noti come vitamine antiossidanti che sono suggerite per diminuire il danno ossidativo e ridurre il rischio di alcune malattie croniche. Le malattie, come i disturbi cardiovascolari, sono associate a concentrazioni inadeguate di acido l-ascorbico, tocoferolo e β-carotene negli studi epidemiologici. La vitamina C migliora anche l’assorbimento del ferro riducendo Fe3 + a Fe2 + da fonti di ferro non eme . In presenza di ioni redox-attivi (ferro, rame), la vitamina C agisce come proossidante, contribuendo alla formazione di radicali idrossilici, che possono portare all’ossidazione di lipidi, DNA o proteine . Esistono diversi meccanismi per alleviare lo stress ossidativo e riparare le macromolecole danneggiate. Gli antiossidanti enzimatici e non enzimatici hanno ruoli importanti nello scavenging dei radicali liberi e delle specie reattive dell’ossigeno (ROS). Gli enzimi antiossidanti, catalasi (CAT), superossido dismutasi (SOD), glutatione reduttasi (GR), glutatione perossidasi (della gshpx) e, nelle piante, ascorbato perossidasi (AA-px) e il nonenzymatic antiossidanti (glutatione (GSH) e acido ascorbico (ASC), hanno dimostrato di essere significativamente influenzato da stress ossidativo . I composti antiossidanti possono prevenire la formazione incontrollata di radicali liberi o inibire la loro reazione con i siti biologici; inoltre, la distruzione della maggior parte dei radicali liberi dipende dall’ossidazione degli antiossidanti endogeni principalmente scavando e riducendo le molecole . La vitamina C è pensato per essere un antiossidante solubile in acqua importante che è segnalato per neutralizzare ROS e ridurre lo stress ossidativo .
La vitamina C è un potente agente riducente e scavenger di radicali liberi nei sistemi biologici . È coinvolto nella prima linea di difesa antiossidante, proteggendo le membrane lipidiche e le proteine dal danno ossidativo. Come molecola solubile in acqua, la vitamina C può funzionare sia all’interno che all’esterno delle cellule e può neutralizzare i radicali liberi e prevenire i danni dei radicali liberi. La vitamina C è un’ottima fonte di elettroni per i radicali liberi che stanno cercando un elettrone per riguadagnare la loro stabilità. La vitamina C può donare elettroni ai radicali liberi e placare la loro reattività .
La vitamina C ha dimostrato di essere un efficace spazzino contro le specie di ossido di ossigeno e azoto, come lo ion radicale superossido, il perossido di idrogeno, il radicale idrossile e l’ossigeno singoletto. Questa proprietà della vitamina C ha processi vitali nella protezione dei componenti cellulari dai danni indotti dai radicali liberi. Inoltre, la vitamina C è efficace nel rigenerare la forma antiossidante della vitamina E riducendo i radicali tocoferossilici. Questo processo protegge le membrane e altri compartimenti della cellula dai danni indotti dai radicali liberi (Figura 2). L’ascorbato perossidasi (APX) è un enzima che riduce l’H2O2 all’acqua usando l’ascorbato come donatore di elettroni. Monodehydroascorbate è un ascorbato ossidato che viene rigenerato dalla monodehydroascorbate reduttasi (MDAR). Il radicale monodeidroascorbato rapidamente sproporziona in ascorbato e deidroascorbato. Dehydroascorbate is reduced to ascorbate by dehydroascorbate reductase in the presence of GSH, yielding oxidized glutathione (GSSG). It is reduced by glutathione reductase (GR) using nicotinamide adenine dinucleotide phosphate hydrogen (NADPH) as an electron donor. Dehydroascorbate may be reduced nonenzymatically or catalyzed by proteins with dehydroascorbate reductase (DHAR) activity.
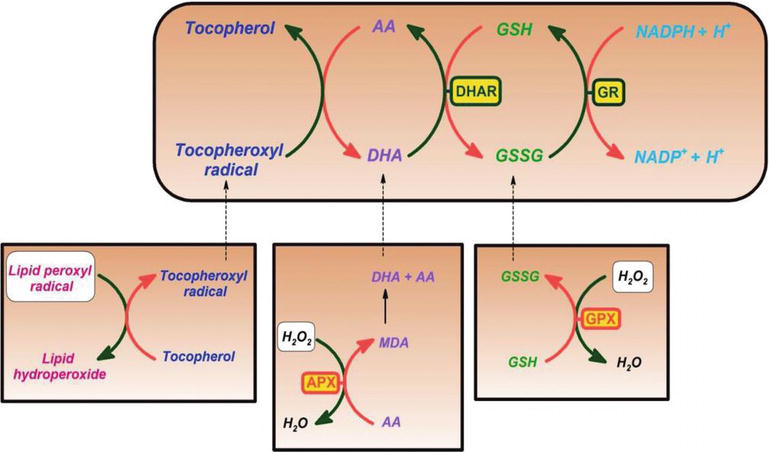
Figure 2.
xmlns:mml=”http://www.w3.org/1998/Math/MathML” xmlns:xlink=”http://www.w3.org/1999/xlink” xmlns:xsi=”http://www.w3.org/2001/XMLSchema-instanceAscorbate and redox cycling antioxidants. AA, ascorbate; DHA, dehydroascorbate; DHAR, semidehydroascorbate reductase; GSH, glutathione; GSSG, semi-glutathione reductase; GR, glutathione reductase; APX, ascorbate peroxidase; and GPX, glutathione peroxidase .
Glutathione-ascorbate cycle operates in the cytosol, mitochondria, plastids, and peroxisomes in plants . Si suggerisce che il ciclo glutatione-ascorbato svolge un ruolo chiave per la disintossicazione H2O2, a causa delle alte concentrazioni di glutatione, ascorbato e NADPH nelle cellule vegetali. Altri enzimi, come ascorbato e glutatione perossidasi, che utilizzano tioredossine o glutaredossine come substrati riducenti, assumono anche un ruolo nella rimozione di H2O2 nelle piante (Figura 2).
La vitamina C forma anche il radicale semidehydroascorbilh, un radicale relativamente longevo, nella rigenerazione della vitamina E dalla sua forma radicale, così come nei radicali scavenging. Le cellule vegetali e animali contengono un enzima semideidroascorbato reduttasi dipendente dal NADH (EC 1.6.5.4), che riduce il radicale alla vitamina C utilizzando il NADH come fonte di agente riducente (Figura 2). Sia enzimaticamente che nonenzimaticamente, può irreversibilmente decomporsi in acido diketogluconico o può essere convertito in ascorbato in una reazione glutatione-dipendente .
Come sostanza riducente e donatore di elettroni, durante lo scavenging dei radicali liberi, la vitamina C dona elettroni ad alta energia per neutralizzare i radicali liberi ed è ossidata in acido deidroascorbico. L’acido deidroascorbico può essere riconvertito in acido ascorbico per il riutilizzo o può essere metabolizzato, rilasciando ulteriormente più elettroni. Sebbene la vitamina C sia assorbita dall’intestino tramite un trasportatore di vitamina C sodio-dipendente, la maggior parte delle cellule trasporta la vitamina C in forma ossidata (acido deidroascorbico) tramite il trasportatore di glucosio 1. L’acido deidroascorbico viene ridotto per generare acido ascorbico all’interno della cellula, proteggendo i mitocondri dal danno ossidativo indotto dai radicali liberi (Figure 2 e 3). Radicali liberi altamente reattivi (ad es., RO -, RO2 -, OH -, NO2) sono ridotti dall’ascorbato e il radicale ascorbilico appena generato è scarsamente reattivo. L’ascorbato può anche pulire le specie reattive non radicali, derivate dal perossinitrito, come l’acido ipocloroso, l’ozono e gli agenti nitranti. La vitamina C è un catalizzatore di riduzione dell’ossidazione del monosaccaride (redox) trovato in entrambi gli animali e le piante. L’effetto antiossidante della vitamina C è dovuto alla sua capacità di donare elettroni sia dal secondo che dal terzo carbonio. Durante l’evoluzione dei primati, uno degli enzimi necessari per produrre l’acido ascorbico è stato perso dalla mutazione, gli esseri umani devono ottenerlo dalla dieta ; la maggior parte degli animali può sintetizzare questa vitamina nei loro corpi e non lo richiede nelle loro diete . La vitamina C è necessaria nella conversione del procollagene in collagene ossidando i residui di prolina in idrossiprolina. In altre cellule, viene mantenuto nella sua forma ridotta per reazione con glutatione . Come mostrato nelle figure 2 e 3, l’acido ascorbico è un catalizzatore redox che può ridurre, e quindi neutralizzare, ROS come il perossido di idrogeno (H2O2) (Figure 2 e 3).
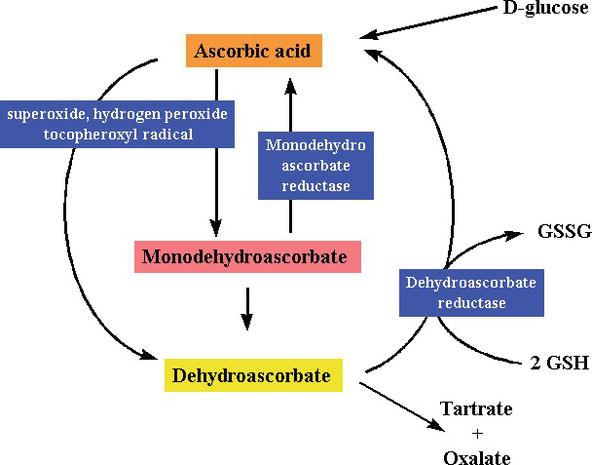
Figure 3.
xmlns:mml=”http://www.w3.org/1998/Math/MathML” xmlns:xlink=”http://www.w3.org/1999/xlink” xmlns:xsi=”http://www.w3.org/2001/XMLSchema-instanceSynthesis and degradation ofl-ascorbic acid in plant tissues .
Ascorbic acid has direct antioxidant effects, and also it is a substrate for the redox enzyme ascorbate peroxidase, that is particularly important in stress resistance in plants. L’acido ascorbico è presente ad alti livelli in tutte le parti delle piante, specialmente nei cloroplasti che raggiungono concentrazioni di 20 mm lì . Deidroascorbato (DHA) e ascorbato radicale libero (AFR), come intermedio, il radicale libero ascorbato (AFR), che sono reversibili, ossidazioni a un elettrone sono generati da ascorbato (Figura 4). Secondo il modello generalmente assunto di rimozione enzimatica di ROS, SOD catalizza l’anione superossido a H2O2 e ossigeno; quindi H2O2 viene ridotto in acqua e ossigeno molecolare da CAT. CAT turnover number is very high, but its affinity for H2O2 is relatively low, and consequently a certain amount of H2O2 remains in the cell.
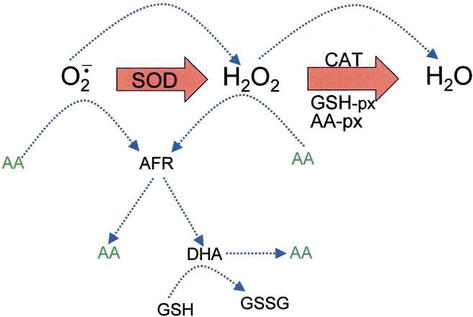
Figure 4.
xmlns:mml=”http://www.w3.org/1998/Math/MathML” xmlns:xlink=”http://www.w3.org/1999/xlink” xmlns:xsi=”http://www.w3.org/2001/XMLSchema-instanceThe role of AA in the detoxification of ROS. Blue dotted lines indicate nonenzymatic reactions.
H2O2 can react with superoxide anion formed in oxidative metabolism generating the highly reactive hydroxyl radical. GSH peroxidases (GSH-px) and AA peroxidases (AA-px) are capable of scavenging H2O2 due to their high affinity for H2O2. The cooperativity of SOD, CAT, and peroxidases ensures low amounts of superoxide anion and H2O2 and limiting the risk of hydroxyl radical formation (Figure 5).

Figure 5.
xmlns:mml=”http://www.w3.org/1998/Math/MathML” xmlns:xlink=”http://www.w3.org/1999/xlink” xmlns:xsi=”http://www.w3.org/2001/XMLSchema-instanceFoyer-Halliwell-Asada cycle .