Vitamin C: Et Antioksidantmiddel
Redoks metabolisme og antioksidantegenskaper av vitamin c
Frie radikaler og oksidanter spiller en dobbel rolle som både giftige og fordelaktige forbindelser, i metabolske prosesser og som respons på eksogene stimuleringer. De produseres enten fra normale metabolske aktiviteter eller fra miljøfaktorer (forurensning, sigarettrøyk og stråling). Når en overbelastning av frie radikaler ikke kan renses, genererer akkumuleringen i kroppen oksidativt stress . Oksidativt stress oppstår når dannelsen av frie radikaler overskrider beskyttelsesevnen mot dem. Denne prosessen fører til utvikling av kroniske og degenerative sykdommer som kreft, autoimmune lidelser, aldring, grå stær, revmatoid artritt, kardiovaskulære og neurodegenerative sykdommer . En antioksidant er et molekyl som forhindrer oksidasjon av andre molekyler. Oksidasjonsprosessen er en kjemisk reaksjon som produserer frie radikaler, som fører til kjedereaksjoner som kan skade celler. Antioxidant effekten av vitamin c har blitt godt dokumentert . Vitamin c er en kraftig antioksidant som har evne til å donere et hydrogenatom og danne et relativt stabilt ascorbylfritt radikal. Vitamin E, vitamin c og β-karoten er kjent som antioksidant vitaminer som foreslås å redusere oksidativ skade og redusere risikoen for visse kroniske sykdommer. Sykdommer, som kardiovaskulære sykdommer, er forbundet med utilstrekkelige konsentrasjoner av l-askorbinsyre, tokoferol og β-karoten i epidemiologiske studier. Vitamin C forbedrer også jernabsorpsjonen ved å redusere Fe3 + Til Fe2 + fra ikke-heme jernkilder . I nærvær av redoks-aktive ioner (jern, kobber) virker Vitamin C som et prooksidant, som bidrar til dannelsen av hydroksylradikaler, som kan føre til lipid -, DNA-ELLER proteinoksidasjon . Det finnes forskjellige mekanismer for å lindre oksidativt stress og reparere skadede makromolekyler. Enzymatiske og ikke-enzymatiske antioksidanter har viktige roller i å rense frie radikaler og reaktive oksygenarter (ROS). Antioksidant enzymer, katalase (CAT), superoxide dismutase (SOD), glutation reduktase (GR), glutation peroxidase (GSHpx) og, i planter, ascorbate peroxidase (AA-px) og nonenzymatic antioksidanter, inkludert glutation (GSH) og ascorbate (ASC), har vist seg å være betydelig påvirket av oksidativt stress . Antioxidantforbindelser kan forhindre ukontrollert dannelse av frie radikaler eller hemme deres reaksjon med biologiske steder; også ødeleggelsen av de fleste frie radikaler avhenger av oksidasjonen av endogene antioksidanter, hovedsakelig ved å rense og redusere molekyler . Vitamin C antas å være en viktig vannløselig antioksidant som rapporteres å nøytralisere ROS og redusere oksidativt stress .Vitamin C Er et kraftig reduksjonsmiddel og scavenger av frie radikaler i biologiske systemer . Det er involvert i den første linjen av antioksidantforsvar, beskytter lipidmembraner og proteiner mot oksidativ skade. Som et vannløselig molekyl kan vitamin C virke både i og utenfor cellene, og kan nøytralisere frie radikaler og forhindre skade på frie radikaler. Vitamin C er en utmerket kilde til elektroner for frie radikaler som søker ut et elektron for å gjenvinne stabiliteten. Vitamin C kan donere elektroner til frie radikaler og slukke deres reaktivitet .Vitamin C har vist seg å være en effektiv scavenger mot oksygen-og nitrogenoksidarter, som superoksidradikal ion, hydrogenperoksid, hydroksylradikal og singlet oksygen. Denne egenskapen av vitamin c har viktige prosesser i beskyttelse av cellulære komponenter fra frie radikaler-indusert skade. I tillegg er vitamin c effektivt for å regenerere antioxidantformen av vitamin e ved å redusere tokoferoksylradikaler. Denne prosessen beskytter membraner og andre rom i cellen mot skade forårsaket av frie radikaler (Figur 2). Ascorbatperoksidase (APX) er et enzym som reduserer H2O2 til vann ved å bruke ascorbat som elektrondonor. Monodehydroaskorbat er et oksidert askorbat som regenereres av monodehydroaskorbatreduktase (MDAR). Monodehydroaskorbatradikal uforholdsmessig raskt til ascorbat og dehydroaskorbat. Dehydroascorbate is reduced to ascorbate by dehydroascorbate reductase in the presence of GSH, yielding oxidized glutathione (GSSG). It is reduced by glutathione reductase (GR) using nicotinamide adenine dinucleotide phosphate hydrogen (NADPH) as an electron donor. Dehydroascorbate may be reduced nonenzymatically or catalyzed by proteins with dehydroascorbate reductase (DHAR) activity.
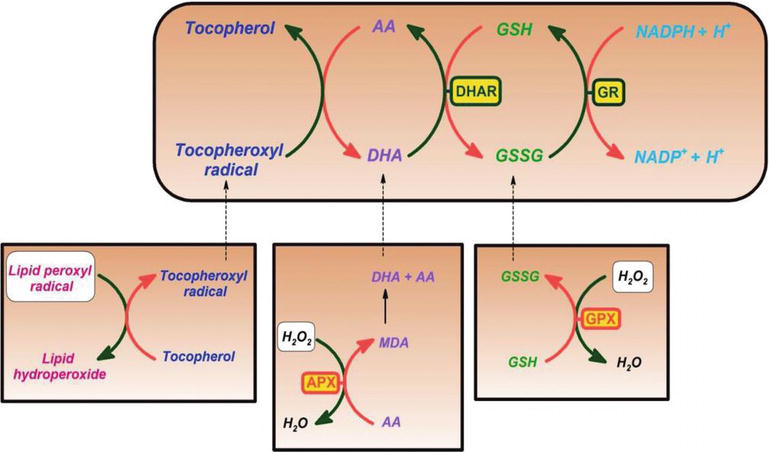
Figure 2.
xmlns:mml=»http://www.w3.org/1998/Math/MathML» xmlns:xlink=»http://www.w3.org/1999/xlink» xmlns:xsi=»http://www.w3.org/2001/XMLSchema-instanceAscorbate and redox cycling antioxidants. AA, ascorbate; DHA, dehydroascorbate; DHAR, semidehydroascorbate reductase; GSH, glutathione; GSSG, semi-glutathione reductase; GR, glutathione reductase; APX, ascorbate peroxidase; and GPX, glutathione peroxidase .
Glutathione-ascorbate cycle operates in the cytosol, mitochondria, plastids, and peroxisomes in plants . Det foreslås at glutation-ascorbat syklusen spiller en nøkkelrolle FOR h2o2 avgiftning, på grunn av de høye konsentrasjonene av glutation, ascorbat og NADPH i planteceller. Andre enzymer, som ascorbat og glutationperoksidaser, som bruker tioredoksiner eller glutaredoksiner som reduserende substrater, tar også roller i fjerning AV H2O2 i planter(Figur 2).
Vitamin c danner også semidehydroaskorbylradikal, et relativt langlivet radikal, i regenerering av vitamin E fra sin radikale form, så vel som i rensing av radikaler. Plante-og dyreceller inneholder ET NADH-avhengig semidehydroaskorbatreduktaseenzym (EC 1.6.5.4), som reduserer radikalet tilbake til vitamin C ved å bruke NADH som en kilde til reduksjonsmiddel (Figur 2). Både enzymatisk og ikke-enzymatisk kan det irreversibelt dekomponeres til diketoglukonsyre eller det kan omdannes til ascorbat i en glutationavhengig reaksjon .som å være en reduserende substans og en elektrondonor, donerer c-vitamin høy-energi elektroner for å nøytralisere frie radikaler, og det oksyderes til dehydroaskorbinsyre. Dehydroaskorbinsyre kan omdannes tilbake til askorbinsyre for gjenbruk eller kan metaboliseres, ytterligere frigjøre flere elektroner. Selv om vitamin C absorberes fra tarmen via en natriumavhengig Vitamin c-transportør, transporterer de fleste celler vitamin c i oksidert form (dehydroaskorbinsyre) via glukosetransportør 1. Dehydroaskorbinsyre reduseres for å generere askorbinsyre inne i cellen, og beskytter mitokondrier mot frie radikalindusert oksidativ skade(Figur 2 og 3). Svært reaktive frie radikaler (f. eks., RO -, RO2 -, OH -,, NO2) reduseres av ascorbat, og det nylig genererte ascorbylradikalet er dårlig reaktivt. Ascorbat kan også scavenge nonradical reaktive arter, avledet fra peroxynitrite, som hypoklorsyre, ozon og nitrerende midler. Vitamin C er en monosakkarid oksidasjonsreduksjon (redoks) katalysator som finnes i både dyr og planter. Den antioxidante effekten av vitamin c skyldes evnen til å donere elektroner fra både andre og tredje karbon. Under primatutvikling har et av enzymene som trengs for å lage askorbinsyre, gått tapt ved mutasjon, mennesker må få det fra kostholdet; de fleste dyr kan syntetisere dette vitaminet i kroppen og krever ikke det i deres dietter . Vitamin C er nødvendig for å omdanne prokollagen til kollagen ved å oksidere prolinrester til hydroksyprolin. I andre celler opprettholdes den i redusert form ved reaksjon med glutation . Som vist I Figur 2 og 3, er askorbinsyre en redokskatalysator som kan redusere OG dermed nøytralisere ROS som hydrogenperoksid (H2O2) (Figur 2 og 3).
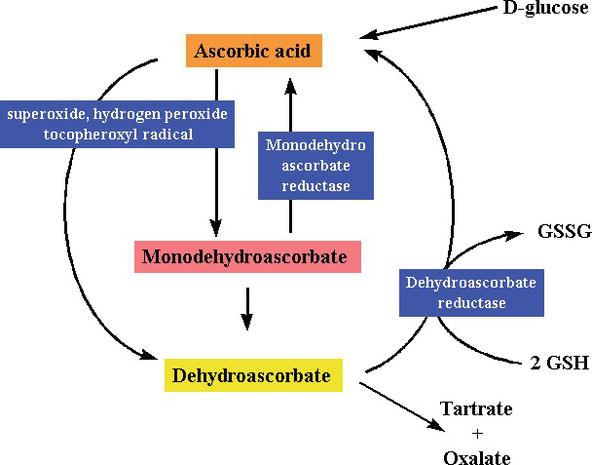
Figure 3.
xmlns:mml=»http://www.w3.org/1998/Math/MathML» xmlns:xlink=»http://www.w3.org/1999/xlink» xmlns:xsi=»http://www.w3.org/2001/XMLSchema-instanceSynthesis and degradation ofl-ascorbic acid in plant tissues .
Ascorbic acid has direct antioxidant effects, and also it is a substrate for the redox enzyme ascorbate peroxidase, that is particularly important in stress resistance in plants. Askorbinsyre er tilstede ved høye nivåer i alle deler av planter, spesielt i kloroplaster som når konsentrasjoner på 20 mM der . Dehydroaskorbat (DHA) og ascorbatfriradikal (AFR), som et mellomliggende, ascorbatfriradikal (AFR), som er reversible, en-elektronoksidasjoner genereres fra ascorbat (Figur 4). I henhold til den generelt antatte modellen for enzymatisk fjerning AV ROS, katalyserer SOD superoksidanion TIL H2O2 og oksygen; DERETTER reduseres H2O2 til vann og molekylært oksygen av CAT. CAT turnover number is very high, but its affinity for H2O2 is relatively low, and consequently a certain amount of H2O2 remains in the cell.
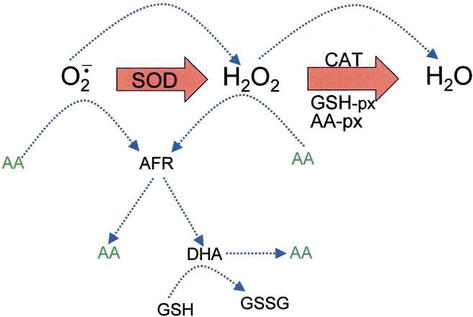
Figure 4.
xmlns:mml=»http://www.w3.org/1998/Math/MathML» xmlns:xlink=»http://www.w3.org/1999/xlink» xmlns:xsi=»http://www.w3.org/2001/XMLSchema-instanceThe role of AA in the detoxification of ROS. Blue dotted lines indicate nonenzymatic reactions.
H2O2 can react with superoxide anion formed in oxidative metabolism generating the highly reactive hydroxyl radical. GSH peroxidases (GSH-px) and AA peroxidases (AA-px) are capable of scavenging H2O2 due to their high affinity for H2O2. The cooperativity of SOD, CAT, and peroxidases ensures low amounts of superoxide anion and H2O2 and limiting the risk of hydroxyl radical formation (Figure 5).

Figure 5.
xmlns:mml=»http://www.w3.org/1998/Math/MathML» xmlns:xlink=»http://www.w3.org/1999/xlink» xmlns:xsi=»http://www.w3.org/2001/XMLSchema-instanceFoyer-Halliwell-Asada cycle .