solventul Universal
solventul Universal
aceasta este, desigur, o altă proprietate cheie a apei, deoarece mai multe substanțe se dizolvă în apă decât orice alt lichid comun. Acest lucru se datorează faptului că molecula de apă polară îmbunătățește „puterea de dizolvare.”Dizolvarea implică ruperea” sărurilor „în ioni” componenți.”De exemplu, NaCl (sare comună) se descompune în ionii Na+ și Cl – din cauza atracției pentru ioni (atomi sau grupuri de atomi cu încărcătură) la moleculele de apă este mare.
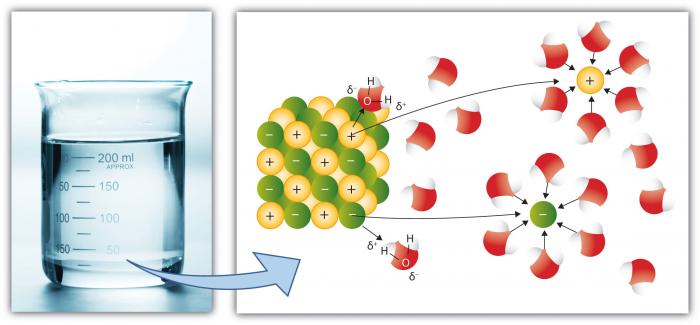
cationii, cum ar fi Na (sodiu) au o sarcină pozitivă netă, în timp ce anionii (cum ar fi Cl, clorura) au o sarcină negativă netă. Există multe elemente și compuși individuali care formează ioni. Astfel, apa poate deține concentrații considerabile de diferite specii chimice în funcție de proprietățile lor particulare. Rețineți modul în care moleculele de apă înconjoară ionii individuali, menținându-i izolați de alți ioni în soluție. Acest lucru se întâmplă până când capacitatea apei de a izola ionii este depășită, moment în care soluția este „saturată” cu acei ioni și nu se poate dizolva mai mult (sarea va începe să precipite—să formeze un solid).