fenantren
- fenantren kemiska egenskaper,användningsområden, produktion
- icke-linjära polycykliska aromatiska kolväten
- molekylstruktur
- kemiska egenskaper
- använder
- beredning
- kemiska egenskaper
- kemiska egenskaper
- fysikaliska egenskaper
- använder
- använder
- Definition
- produktionsmetoder
- Syntesreferens (er)
- allmän beskrivning
- luft & Vattenreaktioner
- Reaktivitetsprofil
- hälsorisk
- brandrisk
- säkerhetsprofil
- potentiell exponering
- cancerframkallande
- källa
- miljö öde
- Frakt
- reningsmetoder
- avfallshantering
fenantren kemiska egenskaper,användningsområden, produktion
icke-linjära polycykliska aromatiska kolväten
fenantren är de enklaste icke-linjära polycykliska aromatiska kolvätena med tre bensenringstruktur, som är isomeren av antracen. År 1872 E. Ostermayer et al har identifierat fenantren i antracenoljefraktionen i stenkolstjära destillat, som är en av stenkolstjära bearbetningsprodukter. I högtemperaturkoltjära är fenantrenhalten sekundär endast till naftalen, som är cirka 4~6%, huvudsakligen koncentrerad i antracenoljefraktionerna. Fenantrenens kemiska aktivitet är starkare än naftalen, men den är svagare än antracen, och oxidations-och tillsatsreaktionerna kan också uppstå vid 9 och 10 positioner.
fenantren är en färglös kristall med glans, och fenantren utfälld från etanol är en färglös monoklinisk kristall. Fenantren är en bladliknande kristall med en relativ densitet av 1.179 (25/4 kg) och ett brytningsindex på 1,6450, smältpunkt på 101 kg och kokpunkt på 340 kg C. Det kan utsättas för sublimering, olöslig i vatten, lätt löslig i etanol, löslig i eter, bensen, ättiksyra, kloroform, koltetraklorid och koldisulfid. Lösningen uppvisar blå fluorescens. De 1, 4, 5, 8-positionerna är desamma, känd som Xiaomi-position; de 2, 3, 6, 7-positionen är också desamma, känd som Xiaomi-position; de 9, 10-positionerna är desamma, kända som ?-position. Dess kemiska egenskap ligger mellan naftalen och antracen. Det kan också ha tillsatsreaktion i 9, 10-positionen, men inte lika lätt som antracen. Oxidation sker också vid 9, 10-positionen med oxidering som ger fenantrenekinon. Substitutionsreaktioner kan också förekomma. Det kan också erhållas genom separation från antracenoljefraktionen av koltjärolja. Fenantren kan användas vid tillverkning av bekämpningsmedel och färgämnen, men också användas som stabilisator för hög effektivitet & bekämpningsmedel med låg toxicitet och rökfritt pulver sprängämnen.fenantren kan användas för att producera färgämnen, läkemedel och hartser efter omvandlingsbehandling. Oxidationsprodukterna fenantrenekinon kan användas som färgämnen, fungicider och polymerisationshämmare; 9, 10-bifenyldikarboxylsyra används för att tillverka polyester och alkydharts; 9, 10-dihydro-9-fenatronsyra är ett växttillväxtstimulerande hormon; Perhydrofenantren tillverkad genom hydrering av fenantren kan användas vid framställning av flygbränsle; dess sulfonerade produkt, fenantrensulfonsyra kan användas som bindemedel och garvning.
Den fenantreninnehållande moderluten under framställning av raffinerad antracen med användning av lösningsmedelsmetod, efter återvinning av lösningsmedel och ytterligare kristalliseringsfiltrering, kan ge rå fenantren innehållande 40% fenantren.
den råa fenantrenen, efter avlägsnande av restlösningsmedel i smältkokaren och sedan rektifieras i likriktartornet med 20 teoretiska plattor, skärs fraktionerna av 335 till 340 c c, följt av kylning, kristallisering och filtrering för att erhålla den industriella fenantrenen med fenantrenhalten på mer än 70%. .
ovanstående information sammanställs av Tongtong från Chemicalbook.
molekylstruktur
molekylstrukturen för fenantren och antracen liknar varandra med alla atomer som ligger i samma plan, men inte i samma linje, eftersom de är ett slutet konjugatsystem med aromatisk egenskap. De 1, 2, 3, 4, 10 positionerna och 5, 6, 7, 8, 9 positionerna inuti molekylerna motsvarar varandra, men det fanns skillnader i aktivitet vid de 5 positionerna, bland vilka 9 och 10 hade högre aktivitet med substitution, oxidation och tillsats som inträffade i 9 och 10 positioner: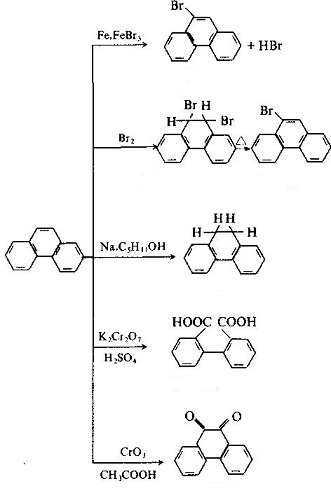
Fenantrenekinon är ett bekämpningsmedel som används som bakteriedödande fröförband, som kan förhindra vete scab, hård smut och sötpotatis svart fläck.
industriell fenantren härrör från destillation av antracenolja härrörande från stenkolstjära destillat. Många typer av naturliga produkter (som steroler) innehåller detta ringsystem. Fenantren används huvudsakligen vid tillverkning av färgämnen, läkemedel, hög effektivitet och låg toxicitet av bekämpningsmedel, och kan användas som scintillanter, rökfri pulverstabilisator. Många av fenantrenderivaten har cancerframkallande fysiologiska effekter. Såsom: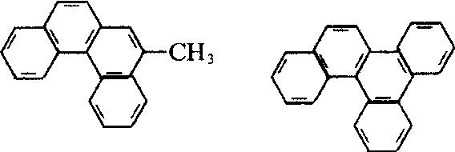
molekylstrukturen för 2-metyl-3, 4-bensofenantren och 1, 2, 3, 4-dibensofen
kemiska egenskaper
det verkar som vit glans och fluorescerande flingkristaller. Det är inte lösligt i vatten, Något lösligt i etanol, lösligt i eter, ättiksyra, bensen, koltetraklorid och koldisulfid.
använder
det kan användas för tillverkning av fenantrenekinon, syntetiskt harts, bekämpningsmedel och konserveringsmedel och så vidare.fenantren, genom oxidationen, kan ge fenantrenkinon, som ska användas för att ersätta de organiska kvicksilverbekämpningsmedlen ceresin och gallotox. Bifenylsyran erhållen från dess oxidation kan användas för att framställa alkydharts. Fenantrenoxidation kan också ge anhydrid, cyklohexanon och fenol. Kloreringsprodukterna av fenantren kan användas för att göra icke brandfarliga elektriska isolatorer och impregneringsmedel. Den sulfonerade fenantrensulfonsyran kan tillverkas av bindemedel, garvning och så vidare. Men i själva verket har de flesta av dessa applikationer ännu inte utvecklats. I pappersindustrin kan fenantren användas som massagedämpningsmedel; kan också användas för nitroglycerinsprängämnen och nitrocellulosastabilisator och för tillverkning av rökbomb; den fasta oxiden av fenantren kan tillverkas av utmärkta flambeständiga elektriska isoleringsmaterial och fyllmedel. I medicin kan fenantren användas för att syntetisera alkaloider-morfin och koffein, dimetylmorfin samt läkemedel med speciella fysiologiska effekter på många reproduktionsorgan. I färgindustrin kan fenantren tillverkas av 2-aminofenantrenkinon, bensantron, sulfidreduceringsfärgämne (blå BO, svart BB och brun) och så vidare. Dessutom kan plastindustrin, syntetiska garvningsmedel och fenantren, under hög temperatur och högt tryck, genomgå hydrering för att få hydrofenantren, vilket är bränslet för seniorflygplan.
för bestämning av molekylvikt och syntes av organiska föreningar.
beredning
fenantren är ett relativt högt innehåll av koltjära, som står för 5% koltjära, näst efter naftalenhalten. Antracenoljan i 300-360 kg fraktionsintervall av koltjära har det högsta innehållet av fenantren, följt av antracen och karbazol och så vidare. Fenantrenextraktionsmetoden skickar vanligtvis antracenolja för kylning, kristallisering och därefter vakuumfiltrering eller centrifugalseparation för oljeseparation. Den relativt höga mängden lösliga fenoler i oljor kan återvinnas med hjälp av precisionsdestillationsmetod. Den erhållna kristallen kallas rå antracen, som innehåller 25-30% antracen, 22-25% karbazol och 30% fenantren. Råantracen kan utsättas för tung bensenutvinning, kylning, filtrering med filtratet ångat ur lösningsmedel före omkristallisering och filtrering. Ta filtrat för destillation så att vi kan få industriell fenantren med sulfonering för att få fin fenantren.
kemiska egenskaper
vita kristaller
kemiska egenskaper
fenantren är en vit kristallin substans. Svag aromatisk lukt. Polycykliska aromatiska kolväten (PAH) är föreningar som innehåller flera bensenringar och kallas också polynukleära aromatiska kolväten.
fysikaliska egenskaper
färglösa, monokliniska kristaller med en svag, aromatisk lukt
använder
fenantren är ett polycykliskt aromatiska kolväten, ett miljöförorenande ämne.
använder
märkta polycykliska aromatiska kolväten som mikroföroreningar.
Definition
ChEBI: Ett polycykliskt aromatiskt kolväte bestående av tre smälta bensenringar som tar sitt namn från de två termerna ’fenyl’ och ’antracen.’
produktionsmetoder
fenantren förekommer i stenkolstjära och kan isoleras frånflera typer av råolja.
Syntesreferens (er)
Journal of Heterocyclic Chemistry, 30, s. 291, 1993 DOI: 10.1002/jhet.5570300151
Journal of Organic Chemistry, 18, s. 801, 1953 DOI: 10.1021/jo50013a004
tetraeder bokstäver, 15, S. 495, 1974
allmän beskrivning
färglösa monokliniska kristaller med en svag aromatisk lukt. Lösningar uppvisar en blå fluorescens.
luft & Vattenreaktioner
olöslig i vatten.
Reaktivitetsprofil
fenantren kan reagera med oxiderande material .
hälsorisk
den akuta orala toxiciteten hos fenantren är low.It är giftigare än antracen. Ett oralt LD50-värde hos möss rapporteras vid 700 mg / kg. Det kan orsaka tumör i huden på applikationsstället.Bevisen på karcinogenicitet hos djur är emellertid otillräckliga.
brandrisk
fenantren är brännbart.
säkerhetsprofil
Gift intravenöst. Måttligt giftigt vid förtäring. Mutationsdata rapporterade. En fotosensibiliserare för mänsklig hud. Tvivelaktigt cancerframkallande med experimentella neoplastigena och tumörgena data genom hudkontakt. Brännbar vid exponering för värme eller låga; kan reagera kraftigt med oxiderande material. För att bekämpa eld, använd vatten, skum, CO2, torrkemikalie. Vid upphettning till nedbrytning avger den frän rök och irriterande rök
potentiell exponering
damm kan bilda explosiv blandning med luft. Oförenlig med oxidationsmedel (klorater, nitrater, peroxider, permanganater, perklorater, klor, brom, fluor etc.); kontakt kan orsaka bränder eller explosioner. Håll dig borta från alkaliska Material, starka baser, starka syror, oxosyror, epoxider.
cancerframkallande
fenantren är ineffektivt som aninitiator. Det är inte klassificerbart med avseende på karcinogenicitet hos människa-klass 3 av IARC och klass D av IRIS, baserat på inga humandata och otillräckliga data från en enda gavagestudy hos råttor och hudmålnings-och injektionsstudier imice.
källa
detekterad i grundvatten under en tidigare kolförgasningsanläggning i Seattle, WA vid en koncentration av 130 kg/L (ASTR, 1995). Detekterad i 8 dieselbränslen i koncentrationer som varierade från 0,17-110 mg/L med ett medelvärde av 41,43 mg/L (Westerholm och Li, 1994) och i destilleradevattenlösliga fraktioner av ny och begagnad motorolja i koncentrationer av 1,9–2,1 respektive 2,1–2,2 kg/l (Chen et al., 1994). Lee et al. (1992) rapporterade koncentrationsintervall på 100 till 300 mg/L och 15 till 25 Kg/L i dieselbränsle respektive motsvarande vattenfas (destillerat vatten). Schauer et al. (1999) rapporterade fenantren i dieselbränsle i en koncentration av 57 kg/g och i ett dieseldrivet medeltungt lastbilsavgas med en utsläppshastighet på 93,1 kg/km.Identifierad i Kuwait och södra Louisiana råoljor i koncentrationer av 26 respektive 70 ppm (Pancirov och Brown,1975). Dieselbränsle erhållet från en bensinstation i Schlieren,Schweiz innehöll fenantren vid en uppskattad koncentration av 327 mg/L (Schluep et al.,2001).
fenantren detekterades i asfaltångor vid en genomsnittlig koncentration av 57,73 ng/m3 (Wanget al., 2001).
Thomas och Delfino (1991) jämviktade föroreningsfritt grundvatten uppsamlat frångainesville, FL med enskilda fraktioner av tre enskilda petroleumprodukter vid 24-25 kub C för24 h. vattenfasen analyserades för organiska föreningar via U. S. EPA godkänd testmetod625. Fenantren detekterades endast i den vattenlösliga fraktionen av dieselbränsle vid en genomsnittlig koncentration av 17 occurg/L.
baserat på laboratorieanalys av 7 koltjärprover varierade fenantrenkoncentrationerna från3 100 till 35 000 ppm (EPRI, 1990). Detekterad i 1-årig koltjärfilm och bulktjära i anidentisk koncentration av 10 000 mg/kg (Nelson et al., 1996). En hög temperatur koltjära innehöll fenantren i en genomsnittlig koncentration av 2,66 vikt % (McNeil, 1983). Identifieradedin högtemperaturkoltjära platser vid koncentrationer från 7500 till 40300 mg/kg(Arrendale och Rogers, 1981). Lee et al. (1992a) ekvilibrerade åtta koltjäror med destillerat vatten vid25 kcal C. Den maximala koncentrationen av fenantren som observerats i vattenfasen är 0,4 mg/L.nio kommersiellt tillgängliga kreosotprover innehöll fenantren vid koncentrationersträcker sig från 48 000 till 120 000 mg/kg (Kohler et al., 2000).typisk koncentration av fenantren i en tung pyrolysolja är 2,5 wt % (Chevron Phillips,maj 2003).
miljö öde
biologisk. Katekol är den centrala metaboliten i bakteriell nedbrytning av fenantren.Mellanliggande biprodukter innefattar 1-hydroxi-2-naftoesyra, 1,2-dihydroxinaftalen ochsalicylsyra (Chapman, 1972; Hou, 1982). Det rapporterades att Beijerinckia, under aerobicvillkor, nedbruten fenantren till cis-3,4-dihydroxi-3,4-dihydrofenantracen (Kobayashiand Rittman, 1982).
jord. De rapporterade halveringstiderna för fenantren i en Kidman sandy loam och McLaurin sandyloam är 16 respektive 35 d (Park et al., 1990). Manilal och Alexander (1991) rapporterade enhalveringstid på 11 d i en Kendaia-jord.
ytvatten. I en 5-m djup ytvattenförekomst var de beräknade halveringstiderna för direkt fotokemisk omvandling vid 40 kg N latitud i midsommar under middagstid 59 och 69 d med och utan sediment-vattenpartitionering (Zepp och Schlotzhauer, 1979).
Fotolytisk. Ett koldioxidavkastning på 24,2% uppnåddes när fenantren adsorberad onsilica gel bestrålades med ljus (290 nm) under 17 timmar (Freitag et al., 1985). I ett 2-wkexperiment applicerades fenantren på jordvattensuspensioner under aeroba och anaeroba förhållanden gav 14co2 utbyten av 7,2 och 6.3%, respektive (Scheunert et al., 1987). Matsuzawa etal. (2001) undersökte fotokemisk nedbrytning av fem polycykliska aromatiska kolväten indieselpartiklar avsatta på marken och i olika markkomponenter. Denfotokemisk nedbrytning genom artificiellt solljus uppnåddes med användning av en 900-W xenonlampa.Ljus från denna lampa passerade genom ett glasfilter för att eliminera ljus med kortare våglängder (2. Dessutom användes en solsimulatorutrustad med en 300-W xenonlampa för att ge maximal solljusintensitet observeradi Tokyo (latitud 35,5 kcal N). Halveringstiden för fenantren i dieselpartiklar med 900-och 300-W-källor var 4,29 respektive 60,63 h. Följande halveringstider bestämdesför fenantren adsorberad på olika jordkomponenter med användning av 900 W-apparater: 3,04 h för kvarts,2,90 h för fältspat, 1,15 h för kaolinit, 4,97 h för montmorillonit, 3,26 h för silikagel och 1,17 h för aluminiumoxid.
kemisk / fysisk. PH 8,8), fenantren-9,10-oxid, fenantren-9,10-Dion och 9,10-dihydrofenantrendiol identifierades som huvudprodukter (Oyler et al.,1983). Det föreslogs att klorering av fenantren i kranvatten stod för närvaron av klor – och diklorofenantrener (Shiraishi et al., 1985).
Frakt
UN3077 miljöfarliga ämnen, fasta ämnen, i. o.s., Faroklass: 9; etiketter: 9-Diverse farligt material, Tekniskt namn krävs.
reningsmetoder
sannolika föroreningar inkluderar antracen, karbazol, fluorene och andra polycykliska kolväten. Rena det genom destillation från natrium under vakuum, kokning med maleinsyraanhydrid i xylen, kristallisering från ättiksyra, sublimering och zonsmältning. Det har också omkristalliserats upprepade gånger från EtOH, * bensen eller pet-eter (b 60-70o), med efterföljande torkning under vakuum över P2O5 i en Abderhalden-pistol. Feldman, Pantages och Orchin separerade det mesta av antracenföroreningar genom återflöde av fenantren (671 g) med maleinsyraanhydrid (194 g) i xylen (1,25 L) under kväve i 22 timmar och filtrerades sedan. Filtratet extraherades med vattenhaltig 10% NaOH, den organiska fasen separerades och lösningsmedlet indunstades. Återstoden, efter omrörning i 2 timmar med 7 g Natrium, destillerades i vakuum och omkristalliserades sedan två gånger från 30% *bensen i EtOH. Det löstes sedan i het ättiksyra (2,2 mL/g) och tillsattes långsamt en vattenlösning av CrO3 (60 g i 72 ml H2O plus 2,2 L ättiksyra) följt av långsam tillsats av conc H2SO4 (30 ml). Blandningen återflödes i 15minuter, späddes med en lika stor volym vatten och kyldes. Fällningen filtrerades bort, tvättades med vatten, torkades och destillerades och omkristalliserades sedan två gånger från EtOH. Ytterligare rening är möjlig genom kromatografi från en CHCl3-lösning på aktiverad aluminiumoxid, med * bensen som eluent och genom zonraffinering. Picrate (1:1) bildar gyllene gula nålar med M 146o, och styphnate (1: 1) har m 138-139o (plattor eller nålar från EtOH respektive EtOH/H2o).
avfallshantering
rådgör med miljötillsynsmyndigheter för vägledning om godtagbara bortskaffningsmetoder. Generatorer av avfall som innehåller denna förorening (100 kg/mo) måste uppfylla EPA-reglerna för lagring, transport, behandling och avfallshantering.