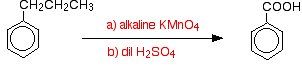några fler reaktioner av bensen och metylbensen
sulfoneringen av metylbensen
metylbensen är mer reaktiv än bensen på grund av metylgruppens tendens att ”trycka” elektroner mot ringen. Exakt hur detta ökar reaktionshastigheten är bortom Storbritannien en nivå – det är ganska mer komplicerat än bara en ökning av elektrondensiteten hos ringen.
effekten av denna större reaktivitet är att metylbensen kommer att reagera med fumande svavelsyra vid 0 kcal C och med koncentrerad svavelsyra om de upphettas under återflöde i cirka 5 minuter.
förutom effekten på reaktionshastigheten, med metylbensen måste du också tänka på var sulfonsyragruppen hamnar på ringen i förhållande till metylgruppen.
metylgrupper har en tendens att”rikta" nya grupper i 2 – och 4 – positionerna på ringen (förutsatt att metylgruppen är i 1 – positionen). Metylgrupper sägs vara 2,4-regi. Ursprunget till denna regi effekt är också bortom Storbritannien en nivå.
så du får en blandning som huvudsakligen består av två isomerer. Endast ca 5-10% av 3 – isomeren bildas.
huvudreaktionerna är:
![]()
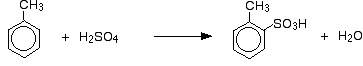
och:
![]()
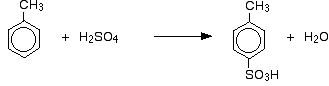
vid sulfonering beror den exakta andelen av de bildade isomererna på reaktionstemperaturen. När temperaturen ökar får du ökande proportioner av 4 – isomeren och mindre av 2 – isomeren.
detta beror på att sulfonering är reversibel. Sulfonsyragruppen kan falla av ringen igen och fästa igen någon annanstans. Detta tenderar att gynna bildandet av den mest termodynamiskt stabila isomeren. Detta utbyte sker mer vid högre temperaturer.
4-isomeren är stabilare eftersom det inte finns någon cluttering i molekylen som det skulle vara om metylgruppen och sulfonsyragruppen var bredvid varandra.
sidokedjaoxidation i alkylbensener
en alkylbensen är helt enkelt en bensenring med en alkylgrupp fäst vid den. Metylbensen är den enklaste alkylbensenen.
alkylgrupper är vanligtvis ganska resistenta mot oxidation. När de är fästa vid en bensenring oxideras de emellertid lätt med en alkalisk lösning av kaliummanganat(VII) (kaliumpermanganat).
metylbensen upphettas under återflöde med en lösning av kaliummanganat(VII) gjord alkalisk med natriumkarbonat. Den lila färgen på kaliummanganatet(VII) ersätts så småningom av en mörkbrun fällning av mangan(IV) oxid.
blandningen surgörs slutligen med utspädd svavelsyra.
sammantaget oxideras metylbensen till bensoesyra.
![]()
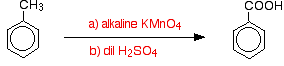
intressant nog oxideras någon alkylgrupp tillbaka till a-COOH-gruppen på ringen under dessa förhållanden. Så, till exempel, oxideras propylbensen också till bensoesyra.
![]()