Patofysiologi / International Osteoporosis Foundation
hormoner är kanske de mest avgörande modulatorerna för benbildning. Det är väl etablerat att östrogen Lindsay, R., förebyggande och behandling av osteoporos. Lancet, 1993. 341 (8848): s. 801-5.
. parathyroidhormon läppar, P., vitamin D fysiologi. Prog Biophys Mol Biol, 2006. 92 (1): s. 4-8
. och i mindre utsträckning testosteron direkt eller indirekt via omvandlingen till östrogen Seeman, E., den strukturella grunden för benbräcklighet hos män. Ben, 1999. 25 (1): s. 143-7.
Van Pottelbergh, I., et al., Störd könssteroidstatus hos män med idiopatisk osteoporos och deras söner. J Clin Endocrinol Metab, 2004. 89 (10): s. 4949-53.
. är nödvändiga för optimal benutveckling och underhåll. Av dessa tros östrogen nu ha den mest direkta effekten på benceller, interagera med specifika proteiner eller receptorer på ytan av osteoblaster och osteoklaster Zallone, A., direkta och indirekta östrogenåtgärder på osteoblaster och osteoklaster. Ann N Y Acad Sci, 2006. 1068: s. 173-9
.
denna interaktion sätter igång en komplex kedja av händelser i cellerna, ökar osteoblastaktiviteten samtidigt som den stör osteoblast-osteoklastkommunikation – en av ironierna med benremodellering är att osteoblasterna frigör faktorer som stimulerar osteoklaster och driver benresorption, som vi ska se nedan.
östrogeneffekter förmedlas genom en specifik typ av cellytreceptor som kallas östrogenreceptorn alfa (ERa), som binder och transporterar hormonet in i cellkärnan där receptorhormonkomplexet fungerar som en omkopplare för att slå på specifika gener. ERa-receptorer finns på ytan av osteoblaster, liksom östrogenreceptorrelaterad receptor alfa (ERRa), som kan spela en hjälproll vid reglering av benceller Bonnelye, E. och J. E. Aubin, Östrogenreceptorrelaterad receptor alfa: en mediator av östrogenrespons i ben. J Clin Endocrinol Metab, 2005. 90 (5): s. 3115-21.
. Nya studier tyder också på att könshormonbindande globulin (SHBG), som underlättar inträde av östrogen i celler, också kan spela en stödjande roll Goderie-Plomp, HW, et al., Endogena könshormoner, könshormonbindande globulin och risken för incident vertebrala frakturer hos äldre män och kvinnor: Rotterdam-studien. J Clin Endocrinol Metab, 2004. 89 (7): s. 3261-9.
.
östrogen, naturligtvis, görs och utsöndras i blodomloppet ett visst avstånd från ben och det har också djupgående effekter på andra vävnader, såsom livmodern och bröstet. Men det finns andra, lokalt producerade signalmolekyler som har djupgående effekter på benfysiologi.

cytokinproduktion under kontroll av östrogen vid benremodellering.
Figure taken from Ferrari & Roux, 2019 Pocket Reference to Osteoporosis, S. Ferrari, Roux, C., Editor 2019, Springer International Publishing.
.
Prostaglandins, particularly prostaglandin E2 (PGE2), stimulate both resorption and formation of bone Pilbeam, C.C., J.R. Harrison, and L.G. Raisz, Chapter 54 – Prostaglandins and Bone Metabolism, in Principles of Bone Biology (Second Edition), J.P. Bilezikian, L.G. Raisz, and G.A. Rodan, Editors. 2002, Academic Press: San Diego. p. 979-994
. PGE2 är en lipid som bildas i olika benceller från en föregångare som kallas arakidonsyra. Det första steget på PGE2-syntes utförs av ett enzym som kallas cyklooxygenas 2 (COX2) och hämmare av detta enzym kan förhindra benbildning som svar på mekanisk stress hos djur Forwood, Mr, inducerbart cyklooxygenas (COX-2) förmedlar induktionen av benbildning genom mekanisk belastning in vivo. J Ben Gruvarbetare Res, 1996. 11 (11): s. 1688-93.
. PGE2 kan krävas för träningsinducerad benbildning.
det finns bevis för att frakturrisken ökar hos personer som tar icke-steroida antiinflammatoriska läkemedel som hämmar COX-2-karbon, L. D., et al., Samband mellan benmineraltäthet och användning av icke-steroida antiinflammatoriska läkemedel och aspirin: påverkan av cyklooxygenaselektivitet. J Bone Miner Res, 2003. 18 (10): s. 1795-802
kan också öka. En annan uppsättning lipidmolekyler som verkar reglera benremodellering är leukotrienerna. Även härledda från arakidonsyra har dessa visat sig minska bentätheten hos möss Traianedes, K., et al., 5-Lipoxygenasmetaboliter hämmar benbildning in vitro. Endokrinologi, 1998. 139 (7): s. 3178-84.
.
hur något av dessa hormoner påverkar benremodellering beror på hur de förändrar osteoklaster och/eller osteoblastaktivitet. Specifika cellytreceptorer hjälper till att överföra signaler från yttre benceller till cellkärnan, där olika gener som reglerar cellaktivitet kan slås på eller av. Dessa inkluderar receptorer för benmorfogenetiska proteiner (BMP) en familj av proteiner som är potenta inducerare av benbildning.
BMP-receptorer har hittats på ytan av osteoblasterprekursorceller Mbalaviele, G., et al., Beta-catenin och BMP-2 synergiserar för att främja osteoblastdifferentiering och ny benbildning. J Cell Biochem, 2005. 94 (2): s. 403-18.
. En annan cellytreceptor som kallas lågdensitetslipoprotein (LDL) – relaterat protein 5-receptor (LRP5), en Wnt-receptor, kan också vara viktig för benbildning eftersom förlust av LRP5 hos djur leder till svår osteoporos Gong, Y., et al., LDL-receptorrelaterat protein 5 (LRP5) påverkar benupplupning och ögonutveckling. Cell, 2001. 107 (4): s. 513-23.
. BMP-receptorer och LRP5 kan samarbeta för att stimulera osteoblaster till handling, men exakt hur detta kan inträffa har inte klargjorts.
Sclerostin, produkt av sost-genen och uttryckt av osteocyterna, binder till lrp5 / 6-receptorn på osteoblaster och hämmar Wnt-signaleringen, vilket leder till en minskning av benbildning Bonewald, L. F., Den fantastiska osteocyten. J Ben Gruvarbetare Res, 2011. 26 (2): s. 229-38.
Li, X., et al., Sclerostin binder till LRP5 / 6 och motverkar kanonisk Wnt-signalering. J Biol Chem, 2005. 280 (20): S. 19883-7.
. Parathyroidhormon (PTH) och mekanisk belastning minskar utsöndringen av sklerostin av oesteocyterna Bellido, T., et al., Kronisk höjning av parathyroidhormon hos möss minskar uttrycket av sklerostin av osteocyter: en ny mekanism för hormonell kontroll av osteoblastogenes.Endokrinologi, 2005. 146 (11): s. 4577-83.
Robling, A. G., et al., Mekanisk stimulering av ben in vivo minskar osteocytuttryck av Sost/sclerostin. J Biol Chem, 2008. 283 (9): s. 5866-75.
. En antikropp mot sclerostin har utvecklats som ett potentiellt läkemedel med potenta egenskaper på benstyrka. Read more on anabolics as treatments.

Figure taken from Ferrari & Roux, 2019 Pocket Reference to Osteoporosis, S. Ferrari, Roux, C., Editor 2019, Springer International Publishing.
.
En cellytreceptor som kallas RANK (för receptoraktivator av NFkB) ger osteoklaster prekursorceller att utvecklas till helt differentierade osteoklaster när RANK aktiveras av dess besläktade partner RANK ligand (RANKL) Yasuda, H., et al., Osteoklastdifferentieringsfaktor är en ligand för osteoprotegerin/osteoklastogenes-hämmande faktor och är identisk med TRANCE/RANKL. Proc Natl Acad Sci USA, 1998. 95 (7): s. 3597-602.
Lacey, D. L., et al., Osteoprotegerin ligand är ett cytokin som reglerar osteoklastdifferentiering och aktivering. Cell, 1998. 93 (2): s. 165-76.
.
RANKL produceras faktiskt av osteoblaster och är en av kanske många signalmolekyler som underlättar korssamtal mellan osteoblasterna och osteoklasterna och hjälper till att samordna benremodellering Theill, L. E., W. J. Boyle och J. M. Penninger, RANK-L och RANK: T-celler, benförlust och däggdjursutveckling. Annu Rev Immunol, 2002. 20: S. 795-823.
. Osteoprotegerin, ett annat protein som frigörs av osteoblaster Suda, T., et al., Modulering av osteoklastdifferentiering och funktion av de nya medlemmarna i tumörnekrosfaktorreceptorn och ligandfamiljerna. Endocr Rev, 1999. 20 (3): s. 345-57.
, kan också binda till RANKL, fungerar som en lockbete för att förhindra RANK och RANKL från att komma i kontakt. Balansen mellan RANKL / osteoprotegerin kan vara avgörande vid osteoporos. Faktum är att djurstudier visade att ökad produktion av osteoprotegerin leder till en ökning av benmassan, medan förlust av proteinet leder till osteoporos och ökade frakturer Bucay, N., et al., osteoprotegerin-bristfälliga möss utvecklar osteoporos tidigt och arteriell förkalkning. Gener Dev, 1998. 12 (9): s. 1260-8.
. Hämmare av RANKL har också visat löfte som potentiell behandling för osteoporos hos människor.
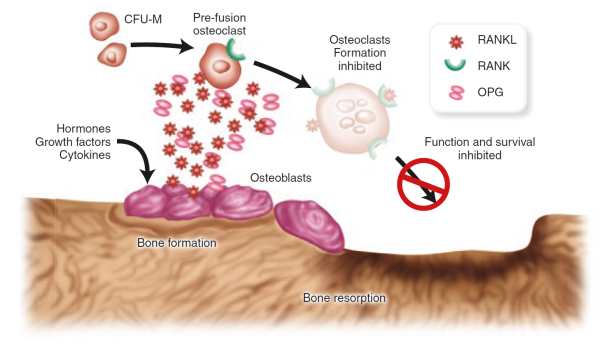
Figure taken from Ferrari & Roux, 2019 Pocket Reference to Osteoporosis, S. Ferrari, Roux, C., Editor 2019, Springer International Publishing.
.
ett andra komplementärt cellsignalsystem som hjälper till att driva bildning och aktivering av osteoklaster upptäcktes också under de senaste åren. I frånvaro av DNAX-aktiverande protein 12 (DAP12) och Fc – Receptor common bisexual chain (FcRy), två cellytreceptorer, utvecklar möss svår osteoporos – det exakta motsatsen till osteoporos-kännetecknad av en dramatisk ökning av bentätheten Mocsai, A., et al., De immunmodulerande adapterproteinerna DAP12 och Fc receptor gamma-chain (FcRgamma) reglerar utvecklingen av funktionella osteoklaster genom Syk tyrosinkinas. Proc Natl Acad Sci USA, 2004. 101 (16): s. 6158-63.
Koga, T., et al., Costimulatoriska signaler medierade av ITAM-motivet samarbetar med RANKL för benhomeostas. Natur, 2004. 428 (6984): s. 758-63.
. Dessa två cellytreceptorer interagerar med en grupp proteiner i cellen som kallas Itam (immunoreceptor tyrosinbaserad aktiveringsmotiv) adapterproteiner för att orsaka en ökning av intracellulärt kalcium.
studier tyder på att RANK/RANKL och ITAM-medierade vägar samarbetade för att inducera full osteoklastaktivitet. Dessa två vägar kan konvergera för att aktivera ett protein som kallas kärnfaktorn för aktiverade T-celler (NFAT) c1. NFATc1 fungerar som en huvudbrytare för benresorption eftersom det slår på generna som osteoklaster prekursorceller behöver bli fullt aktiva osteoklaster Takayanagi, H., mekanistisk inblick i osteoklastdifferentiering i osteoimmunologi. J Mol Med (Berl), 2005. 83 (3): s. 170-9.
.