19.11: Racemization
Opticky aktivní látky, deriváty (§13-5A) jsou racemized pokud dva aromatické kruhy kdykoliv projít koplanární konfigurace pomocí otáčení okolo centrální vazby. To může být způsobeno více či méně snadno teplem, pokud substituenty 2,2 ‚ – ortho nejsou velmi velké.
způsob racemizace sloučenin s asymetrickými atomy uhlíku je složitější. Jednou z možností by bylo, aby se čtyřstěnný chirální uhlík připojený ke čtyřem skupinám stal rovinným a achirálním bez přerušení jakýchkoli vazeb. Teoretické výpočty ukazují, že to není pravděpodobné, že proces pro chirální čtyřmocného uhlíku, ale, jak uvidíme, dochází s chirální uhlík a další chirální atomy, které jsou připojeny do tří skupin:
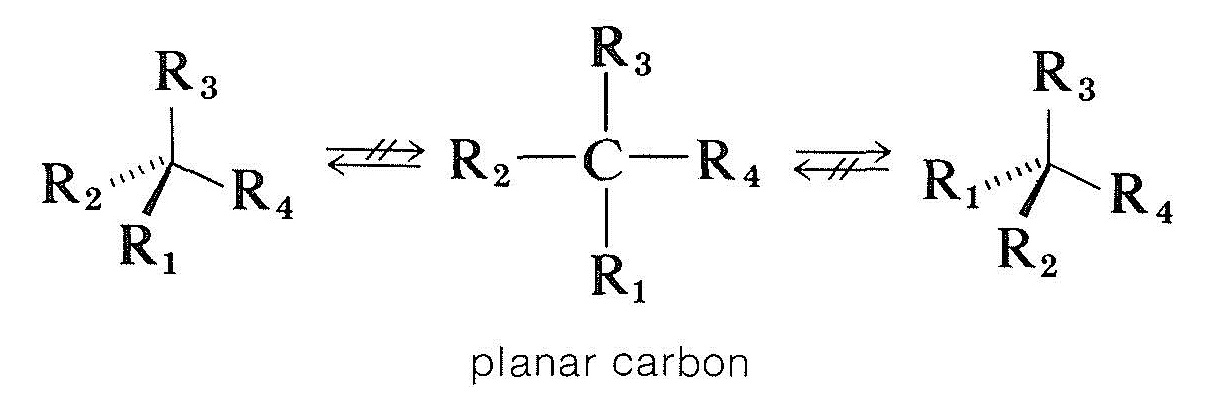
Opticky aktivních karbonylových sloučenin typu \(\ce{-CHC=O}\), ve kterém alfa uhlík je asymetrický, jsou racemized obou kyselin a zásad, a z Části 17-1 můžeme si být jisti, že to souvisí s enolization. Vznik buď enol nebo enolate anion zničí asymetrie \(\alpha\) uhlíku tak, že, i když jen stopové množství enol jsou přítomny v daném okamžiku, nakonec všechny sloučeniny bude racemized. Mechanismus však vyžaduje, aby existoval \(\alfa\) vodík a aby střed symetrie byl umístěn na tomto \(\alfa\) uhlíku. Jinak jsou kyseliny a zásady neúčinné při katalyzování racemizace.
.jpg?revision=1)
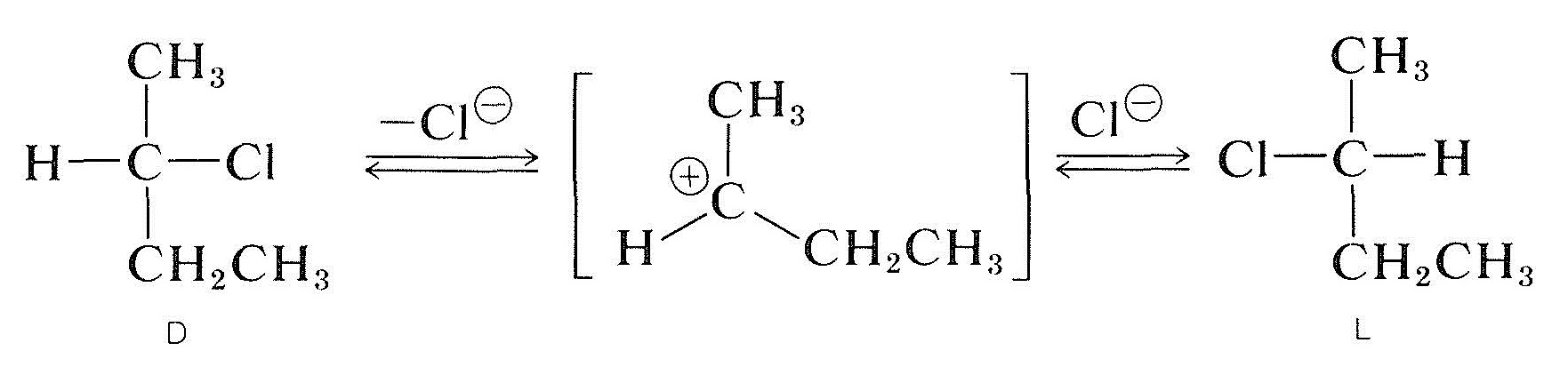
racemizace opticky aktivního sekundárního halogenidu s chirálním uhlíkem nesoucím halogen (např., 2-chlorbutan) se může vyskytnout roztok ih a obvykle čím polárnější a lépe ionizující rozpouštědlo je, tím snadněji je látka racemizována. Ionizace halogenidu procesem \(S_ \ text{N}1\) je pravděpodobně zodpovědná, a to by jistě bylo podporováno polárními rozpouštědly (oddíl 8-6). Vše nasvědčuje tomu, že alkyl-karbokation, jakmile oddělen od svého doprovázející anion je planární, a když takové ion znovu kombinuje s anion má stejnou pravděpodobnost, tvořící \(D\) a \(L\) enantiomery:
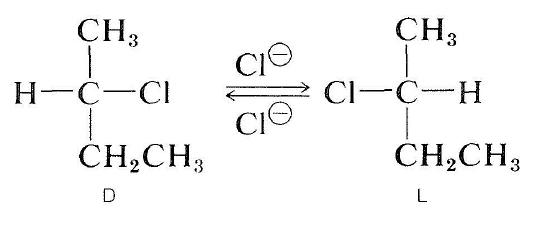
opticky aktivní halogenidy mohou být také racemizovány mechanismem \(s_\text{N}2\). Roztok aktivního 2-chlorbutanu v 2-propanonu obsahujícím rozpuštěný chlorid lithný se stává racemickým. Vytěsnění chloridu halogenidu chloridovým iontem invertuje konfiguraci na atomu, který prochází substitucí (viz bod 8-5). Druhá substituce regeneruje původní enantiomer. Nakonec tento proces tam a zpět vytváří stejná čísla forem \(D\) a \(L\); látka je pak racemická:
asymetrické alkoholy jsou často racemizovány silnými kyselinami. Nepochybně, ionizace a rekombinace karbokation s vodou vede buď enantiomer:
.jpg?revision=1&size=bestfit&width=590&height=243)
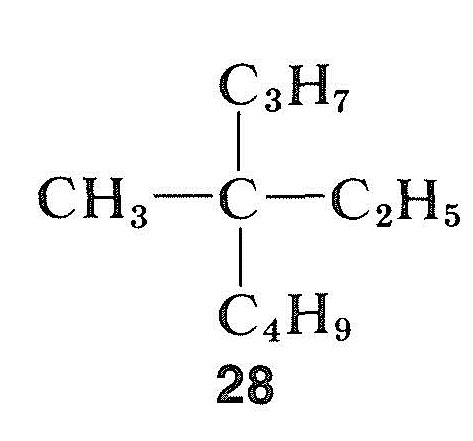
na rozdíl od halogenidy, alkoholy a karbonylové sloučeniny, uhlovodíky, může být velmi obtížné racemize. To platí zejména pro sloučeniny s kvartérním asymetrické centrum, jako methylethylpropylbutylmethane, \(28\), která nemá žádné „zvládnout“, jež umožní převést asymetrického uhlíku symetrický stav jednoduchými chemickými prostředky:
Nicméně, uhlovodíků, které mají atom vodíku na asymetrickém uhlíku může být racemized, pokud mohou být převedeny buď na carbocations nebo carbanions. Snadnost racemizace karbanionového typu bude záviset na kyselosti připojeného vodíku a na stereochemické stabilitě vytvořeného meziproduktu karbanionu. Pokud konfigurace carbanion střední invertuje, racemization bude výsledek (viz také Oddíl 6-4E):
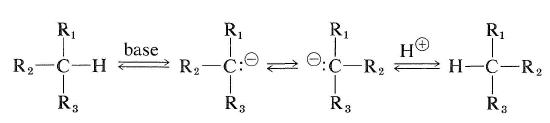
karbokation typ racemization z opticky aktivních uhlovodíků může dojít výměnná reakce popsaná v Oddíle 10-9.
přispěvatelé a atributy
- John D. Robert a Marjorie C. Caserio (1977) základní principy organické chemie, druhé vydání. W. A. Benjamin, Inc. , Menlo Park, CA. ISBN 0-8053-8329-8. Tento obsah je chráněn autorskými právy za následujících podmínek: „máte povolení k individuální, vzdělávací, výzkumné a nekomerční reprodukci, distribuci, zobrazení a provedení tohoto díla v jakémkoli formátu.“