Fenanthrenu
- Fenanthrenu Chemické Vlastnosti,Použití,Výroby
- Non-lineární polycyklických aromatických uhlovodíků
- Molekulární Struktura
- Chemické vlastnosti
- používá
- přípravek
- chemické vlastnosti
- chemické vlastnosti
- fyzikální vlastnosti
- používá
- používá
- definice
- výrobní metody
- Synthesis Reference(y)
- Popis
- Air & reakce vody
- profil reaktivity
- zdravotní riziko
- nebezpečí požáru
- bezpečnostní profil
- potenciální expozice
- Karcinogenita
- Zdroj
- environmentální osud
- Doprava
- metody čištění
- likvidace odpadu
Fenanthrenu Chemické Vlastnosti,Použití,Výroby
Non-lineární polycyklických aromatických uhlovodíků
Fenanthrenu je nejjednodušší nelineární polycyklických aromatických uhlovodíků se třemi benzenový kruh strukturu, přičemž izomer z anthracenu. V roce 1872 e. Ostermayer et al identifikovali fenanthren ve frakci antracenového oleje v destilátu z uhelného dehtu, který je jedním z produktů zpracování uhelného dehtu. Ve vysokoteplotním uhelném dehtu je obsah fenanthrenu sekundární pouze k naftalenu, což je asi 4~6%, hlavně koncentrované ve frakcích antracenového oleje. Chemická aktivita fenanthrenu je silnější než aktivita naftalenu, ale je slabší než aktivita anthracenu a oxidační a adiční reakce se mohou objevit také v 9 a 10 polohách.
fenanthren je bezbarvý krystal s leskem a fenanthren vysrážený z ethanolu je bezbarvý monoklinický krystal. Fenanthren je listový krystal s relativní hustotou 1.179 (25/4 ° c) a index lomu 1.6450, bod tání 101 °C a bod varu 340 °C. může předmětem sublimace, je nerozpustný ve vodě, mírně rozpustný v ethanolu, rozpustný v etheru, benzenu, kyseliny octové, chloroform, tetrachlormethan a sirouhlíkem. Roztok vykazuje modrou fluorescenci. 1, 4, 5, 8-pozice jsou stejné, známé jako α-poloze, 2, 3, 6, 7-pozice jsou stejné, známý jako β-poloze; 9, 10-pozice jsou stejné, známý jako ?-hodnota. Jeho chemická vlastnost je mezi naftalenem a antracenem. Může mít také adiční reakci v poloze 9, 10, ale ne tak snadné jako antracen. K oxidaci dochází také v poloze 9, 10 s oxidací, která dává fenanthrenechinon. Mohou se také objevit substituční reakce. Lze jej také získat oddělením od frakce antracenového oleje černouhelného dehtového oleje. Fenanthren může být použit při výrobě pesticidů a barviv, ale také může být použit jako stabilizátor vysoké účinnosti & pesticidy s nízkou toxicitou a bezdýmné práškové výbušniny.
Fenanthren může být použit k výrobě barviv, léčiv a pryskyřic po zpracování konverze. Oxidační produkty phenanthrenequinone může být použita jako barviva, fungicidy a inhibitory polymerace; 9, 10-bifenyl dikarboxylových kyselin se používá k výrobě polyesterových a alkydových pryskyřice; 9, 10-dihydro-9-phenathroic kyselina je rostlina růst-stimulující hormon; Perhydrophenanthrene provedena prostřednictvím hydrogenace fenanthrenu mohou být použity při výrobě leteckého paliva, jeho sulfonovaný produktu, fenanthrenu sulfonové kyseliny mohou být použity jako pojiva a opalování.
fenanthrenu-obsahující matečných louhů při výrobě rafinovaného anthracenu pomocí rozpouštědla metoda, po zotavení z rozpouštědla a další krystalizace, filtrace, může dát surového fenanthrenu, s teplotou obsahující 40% fenanthrenu.
surového fenanthrenu, s teplotou, po odstranění reziduí rozpouštědla v tavicí kotlík a pak odstraněny v rektifikační věž s 20 teoretických pater, zlomky 335 až 340 °C jsou vystřižené, následuje chlazení, krystalizace a filtrace k získání průmyslové fenanthrenu s fenanthrenu obsahem více než 70%. .
výše uvedené informace sestavuje Tongtong z Chemicalbook.
Molekulární Struktura
molekulární struktury fenanthrenu a anthracenu, jsou podobné navzájem se všechny atomy nacházejí ve stejné rovině, ale nejsou ve stejném řádku, je uzavřený systém konjugovaných s aromatickými majetku. 1, 2, 3, 4, 10 míst a 5, 6, 7, 8, 9 pozic uvnitř molekuly navzájem odpovídají, respektive, ale tam byly rozdíly v činnosti na 5 pozic, z nichž 9 a 10 měli vyšší aktivitu s substituce, oxidace a kromě vyskytující se v 9. a 10. pozice: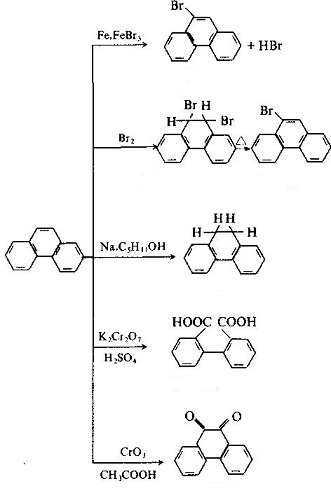
Phenanthrenequinone je pesticid používaný jako germicid moření osiva, být schopen, aby se zabránilo pšenice strup, těžké saze a sladké brambory černá skvrna.
Průmyslový Fenanthren se získává destilací anthracenového oleje získaného z destilátu z černouhelného dehtu. Mnoho druhů přírodních produktů (jako jsou steroly) obsahuje tento kruhový systém. Fenanthren se používá hlavně při výrobě barviv, léčiv, vysoké účinnosti a nízké toxicity pesticidů a může být použit jako scintilátory, bezdýmný stabilizátor prášku. Mnoho derivátů fenanthrenu má karcinogenní fyziologické účinky. Jako jsou: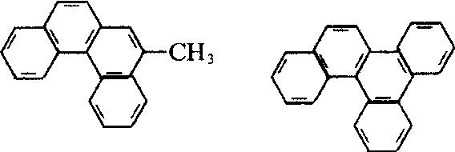
molekulární struktura 2-methyl-3, 4-benzophenanthrene a 1, 2, 3, 4-dibenzophene
Chemické vlastnosti
zdá se, jako bílá lesk a fluorescenční vločka krystaly. Není rozpustný ve vodě, mírně rozpustný v ethanolu, rozpustný v etheru, kyseliny octové, benzenu, tetrachlormethanu a sirouhlíkem.
používá
může být použit pro výrobu fenanthrenechinonu, syntetické pryskyřice, pesticidů a konzervačních látek a tak dále.
Fenanthren může oxidací poskytnout fenanthrenechinon, který se používá k nahrazení organických rtuťových pesticidů ceresin a gallotox. Bifenylová kyselina získaná z její oxidace může být použita k přípravě alkydové pryskyřice. Oxidace fenanthrenu může také poskytnout anhydrid, cyklohexanon a fenol. Chlorační produkty fenanthrenu lze použít k výrobě nehořlavých elektrických izolátorů a impregnantů. Sulfonovaná kyselina fenanthrensulfonová může být vyrobena z pojiva, činění a tak dále. Ve skutečnosti však většina z těchto aplikací ještě nebyla vyvinuta. V papírenském průmyslu, Fenanthrenu může být použit jako buničina antifogging agent; může být také použit pro nitroglycerin výbušniny a nitrocelulózy a stabilizátor pro výrobu dýmovnice; pevný oxid fenanthrenu mohou být vyrobeny z vynikající ohnivzdorné izolační materiály a výplně. V medicíně může být fenanthren použit pro syntézu alkaloidů-morfinu a kofeinu, dimethyl morfinu a léků se zvláštními fyziologickými účinky na mnoho reprodukčních orgánů. V barvení průmyslu, Fenanthrenu mohou být vyrobeny z 2-aminophenanthrene chinon, benzanthrone, sulfid snížení barvivo (modrá BO, černá BB a hnědé), a tak dále. Kromě toho, plastový průmysl, syntetické třísloviny a fenanthrenu, za vysoké teploty a vysokého tlaku, může podstoupit hydrogenace, aby si hydrophenanthrene, že paliva z vyšších proudových letadel.
pro stanovení molekulové hmotnosti a syntézu organických sloučenin.
přípravek
Fenanthren je relativně vysoký obsah uhelného dehtu, který představuje 5% uhelného dehtu, druhý pouze obsah naftalenu. Na anthracenového oleje v 300 až 360 ℃ zlomek rozsah Černouhelného dehtu, má nejvyšší obsah Fenanthrenu, následuje anthracenu a karbazolu a tak dále. Metoda extrakce fenanthrenu je obvykle poslat antracenový olej pro chlazení, krystalizaci a poté vakuovou filtraci nebo odstředivou separaci pro separaci oleje. Relativně vysoké množství rozpustných fenolů v olejích lze získat metodou přesné destilace. Získaný krystal se nazývá surový anthracen, který obsahuje 25-30% anthracenu, 22-25% karbazolu a 30% fenanthrenu. Surového anthracenu, může být předmětem těžké extrakce benzenu, chlazení, filtrace s filtrátu dušená rozpouštědla před rekrystalizace a filtrace. Vezměte filtrát k destilaci, abychom mohli získat průmyslový fenanthren se sulfonací, abychom získali jemný fenanthren.
chemické vlastnosti
bílé krystaly
chemické vlastnosti
Fenanthren je bílá krystalická látka. Slabý aromatický zápach. Polycyklické aromatické uhlovodíky (PAH) jsou sloučeniny obsahující více benzenových kruhů a nazývají se také polynukleární aromatické uhlovodíky.
fyzikální vlastnosti
bezbarvé monoklinické krystaly se slabým aromatickým zápachem
používá
Fenanthren je polycyklická aromatická uhlovodíky, znečišťující látka životního prostředí.
používá
označené polycyklické aromatické uhlovodíky jako mikropolutanty.
definice
ChEBI: Polycyklický aromatický uhlovodík složený ze tří fúzovaných benzenových kruhů, který má svůj název od dvou termínů „fenyl“ a “ anthracen.“
výrobní metody
Fenanthren se vyskytuje v uhelném dehtu a může být izolován odněkolik druhů ropy.
Synthesis Reference(y)
Journal of Heterocyklic Chemistry, 30, s. 291, 1993 DOI: 10.1002 / jhet.5570300151
Journal of Organic Chemistry, 18, p. 801, 1953 DOI: 10.1021/jo50013a004
Čtyřstěn Dopisy, 15, p. 495, 1974
Popis
Bezbarvý monoclinic krystaly, slabě aromatický zápach. Roztoky vykazují modrou fluorescenci.
Air & reakce vody
nerozpustné ve vodě.
profil reaktivity
Fenanthren může reagovat s oxidačními materiály .
zdravotní riziko
akutní perorální toxicita fenanthrenu je low.It je toxičtější než anthracen. Perorální hodnota LD50 u myší je hlášena při dávce 700 mg / kg. To můžezpůsobit nádor v kůži v místě aplikace.Důkazy o karcinogenitě u zvířat jsou však nedostatečné.
nebezpečí požáru
Fenanthren je hořlavý.
bezpečnostní profil
jed intravenózní cestou. Mírně toxický při požití. Hlášené údaje o mutacích. Fotosenzibilizátor lidské kůže. Sporný karcinogen s experimentálními neoplastigenními a tumorigenními údaji při styku s kůží. Hořlavý při vystavení teplu nebo plameni; může energicky reagovat s oxidačními materiály. K boji s ohněm použijte vodu, pěnu, CO2, suchou chemikálii. Při zahřátí na rozklad vydává štiplavý kouř a dráždivé výpary
potenciální expozice
prach může tvořit výbušnou směs se vzduchem. Nekompatibilní s oxidačními činidly (chlorečnany, dusičnany, peroxidy, manganistany, chloristany, chlor, brom, fluor atd.); kontakt může způsobit požáry nebo výbuchy. Chraňte před alkalickými materiály, silnými zásadami, silnými kyselinami, oxokyselinami, epoxidy.
Karcinogenita
Fenanthren je neúčinný jako aniniciátor. To je neklasifikovatelná z pohledu lidské karcinogenity—třída 3 podle IARC a třídy D IRIS, se sídlem onno lidské dat a nedostatečná data z jednoho gavagestudy u potkanů a kůže malování a injekce studie inmice.
Zdroj
Zjištěny v podzemních vodách pod bývalé uhelné zplyňování v Seattle, WA na aconcentration 130 µg/L (AST, 1995). Zjištěn v 8 motorové nafty v koncentracích rangingfrom 0.17– 110 mg/L s průměrnou hodnotou 41.43 mg/L (Westerholm a Li, 1994) a v distilledwater-rozpustná frakce z nového a použitého motorového oleje v koncentraci 1.9–2.1 a 2.1–2.2 µg/L,respektive (Chen et al., 1994). Lee a kol. (1992) hlášené rozsahy koncentrací 100 až 300 mg / L a 15 až 25 µg / L v motorové naftě a odpovídající vodné fázi (destilovaná voda). Schauer a kol. (1999) uvádí, fenanthrenu v motorové naftě v koncentraci 57µg/g a v dieselové medium-duty truck výfukových plynů na úroveň emisí 93.1 µg/km.Identifikováno v Kuvajtu a jižní Louisianě surové oleje v koncentracích 26 a 70 ppm (Pancirov a Brown, 1975). Motorové palivo získané z čerpací stanice v Schlieren,Švýcarsko obsažené fenanthrenu v odhadované koncentrace 327 mg/L (Schluep et al.,2001).
Fenanthren byl detekován v asfaltových výparech při průměrné koncentraci 57,73 ng / m3 (Wanget al., 2001).
Thomas a Delfino (1991) rovnovážného stavu kontaminován podzemní vody shromážděné fromGainesville, FL se jednotlivé frakce ze tří jednotlivých ropných produktů na 24-25 °C odpor 24 až h. Vodná fáze byla analyzována pro organické sloučeniny přes u. s. EPA schválené zkušební method625. Fenanthrenu byl detekován pouze ve vodě rozpustné frakce nafty na averageconcentration 17 µg/L.
na Základě laboratorní analýzy 7 černouhelného dehtu vzorky, fenantren koncentrace se pohybovala od3,100 35 000 ppm (EPRI, 1990). Detekováno v 1letém věku uhelného dehtového filmu a sypkého uhelného dehtu v anidentické koncentraci 10 000 mg / kg (Nelson et al ., 1996). Vysokoteplotní uhelný dehetobsahoval fenanthren v průměrné koncentraci 2,66% hmotnostních (McNeil, 1983). Také identifiedin vysokoteplotní černouhelný dehet hřiště v koncentracích v rozmezí od 7500 do 40,300 mg/kg(Arrendale a Rogers, 1981). Lee a kol. (1992a) vyrovnal osm uhelných dehtů destilovanou vodou při 25 °C. maximální koncentrace fenanthrenu pozorovaná ve vodné fázi je 0,4 mg / L.
devět komerčně dostupných kreosotových vzorků obsahovalo fenanthren v koncentracích od 48 000 do 120 000 mg / kg (Kohler et al ., 2000).
typická koncentrace fenanthrenu v těžkém pyrolýzním oleji je 2,5% hmotnostních (Chevron Phillips, Květen 2003).
environmentální osud
biologický. Katechol je centrální metabolit v bakteriální degradaci fenanthrenu.Mezi meziprodukty patří kyselina 1-hydroxy-2-naftoová, 1,2-dihydroxynaftalen a kyselina salicylová (Chapman, 1972; Hou, 1982). Bylo hlášeno, že Beijerinckia za aerobnípodmínky degradovaly fenanthren na cis-3,4-dihydroxy-3,4-dihydrofenanthracen (Kobayashiand Rittman, 1982).
půda. Hlášené poločasy fenanthrenu v písčité hlíně Kidman a Sandyloamu McLaurin jsou 16 a 35 d (Park et al ., 1990). Manilal a Alexander (1991) uvádí, půl-život 11 d v Kendaia půdy.
povrchová voda. V 5-m hluboké povrchové vody v těle, vypočte poločasu pro přímé photochemicaltransformation na 40 °N zeměpisná šířka uprostřed léta v poledne bylo 59 a 69 d i bez sediment-voda rozdělení, respektive (Zepp a Schlotzhauer, 1979).
Fotolytické. Výtěžek oxidu uhličitého 24,2% byl dosažen, když byl fenanthren adsorbovaný onsilica gel ozářen světlem (λ >290 nm) po dobu 17 h (Freitag et al ., 1985). V 2-wkexperimentu dal fenanthren aplikovaný na suspenze půdy a vody za aerobních a anaerobních podmínek výtěžek 14CO2 7,2 a 6.3% (Scheunert et al ., 1987). Matsuzawa etal. (2001) zkoumali fotochemické degradace pět polycyklických aromatických uhlovodíků indiesel částice uloženy na zemi a v různých půdních složek. Thefotochemická degradace umělým slunečním světlem byla provedena pomocí 900 W xenonové lampy.Světlo z této lampy bylo vedeno skleněným filtrem, aby se eliminovalo světlo kratších vlnových délek (λ2. Kromě toho byl použit solární simulátorvybavený 300 W xenonovou lampou, aby byla zajištěna maximální intenzita slunečního zářenív Tokiu (zeměpisná šířka 35,5 °s. š.). Půl života fenanthrenu v dieselových částic pomocí 900-a 300-W zdroje byly 4.29 a 60.63 h, resp. Následující poločasy byly determinedfor fenanthrenu adsorbované na různých půdních složek pomocí 900-W zařízení: 3.04 h pro křemen,2.90 h pro živce, 1.15 h pro kaolinit, 4.97 h pro montmorillonit, 3.26 h na silikagel, a 1.17 h pro oxid hlinitý.
chemické / fyzikální. Vodné chlorování fenanthrenu na pH 8.8), fenanthren-9,10-oxid, fenanthren-9,10-dion, a 9,10-dihydrophenanthrenediol byly identifikovány jako hlavní produkty (Oyler et al.,1983). Bylo navrženo, že chlorace fenanthrenu ve vodě z vodovodu představovala přítomnost chloru a dichlorfenanthrenů (Shiraishi et al ., 1985).
Doprava
UN3077 látek zatěžujících životní prostředí, pevná, n.o.s., Třída nebezpečnosti: 9; Štítky: 9-Různé nebezpečné látky, Technická Jméno Vyžadováno.
metody čištění
pravděpodobné kontaminanty zahrnují antracen, karbazol, fluoren a další polycyklické uhlovodíky. Čistí destilací z roztoku ve vakuu, vroucí s anhydridem kyseliny maleinové v xylenu, krystalizaci z kyseliny octové, sublimace a zónu tání. Byl také opakovaně rekrystalizován z EtOH, *benzenu nebo pet etheru (B 60-70o), s následným sušením ve vakuu nad P2O5 v pistoli Abderhalden. Feldman, Pantages a Orchin odděleny většina z anthracenu, nečistota tím, refluxující fenanthrenu (671g) s anhydridem kyseliny maleinové (194g) v xylenu (1.25 L) pod dusíkem pro 22hours, potom se zfiltruje. Filtrát byl extrahován vodným 10% NaOH, organická fáze byla oddělena a rozpouštědlo bylo odpařeno. Zbytek se po 2hodinovém míchání se 7g sodíku destiluje ve vakuu a poté se dvakrát rekrystalizuje z 30% * benzenu v EtOH. To bylo pak rozpustí v horké kyselině octové (2.2 mL/g), a to byl pomalu přidán vodný roztok CrO3 (60g v 72mL H2O plus 2.2 L kyseliny octové), následované pomalým přídavkem konc H2SO4 (30 ml). Směs byla refluxována po dobu 15minut, zředěna stejným objemem vody a ochlazena. Sraženina byla odfiltrována, promyta vodou, vysušena a destilována a poté dvakrát rekrystalizována z EtOH. Další čištění je možné pomocí chromatografie z Chci3 řešení, aktivovaného oxidu hlinitého, s *benzen jako eluentu, a do zóny rafinace. Pikrát (1:1) tvoří zlatožluté jehly s m 146o a styfnát (1:1) má m 138-139o (desky nebo jehly z EtOH nebo EtOH/H2O).
likvidace odpadu
konzultujte s environmentálními regulačními agenturami pokyny ohledně přijatelných postupů odstraňování. Generátory odpadu obsahujícího tuto kontaminující látku (≥100 kg / mo) musí splňovat předpisy EPA upravující skladování, přepravu, zpracování a likvidaci odpadu.