Hranic, v Kardiovaskulární Medicíně
Úvod
Při zkoumání souřadnicové systémy, které by mohly být použity pro různé biologické entity, konkrétní vlastnosti by měly být považovány za. Například počet chromozomů a poloha párů bází tvoří lineární souřadnicový systém, který je dostatečný k definování umístění v referenčním genomu (1). Souřadnicový systém pro celé lidské tělo, který může sloužit potřebám HuBMAP, HCA, HPA a dalších mapovacích snah, je však mnohem složitější z několika důvodů (2-5). První, buňky žijí ve třech rozměrech, a další informace potřebné k popisu velikosti a otáčení orientace tkáně vzorku použitého ke generování údajů. Za druhé, zatímco pozice párů genomových bází nezávisí na tom, jak je DNA složena a zabalena do jádra, pozice jednotlivých prvků (např., buňky, orgány) v těle, jsou dynamické, protože se může změnit s kosterní a svalové pohyby, gravitace, dýchání, tlukot srdce a další funkce a síly, které narušují tkáň. Za třetí, i když variability DNA mezi lidmi je <1%, lidské tělo geometrie pokrývá široký rozsah výšek, hmotností a tvarů, které se liší podle pohlaví a rasy a změnit výrazně více než člověk, je životnost.
jednou z možností je použití 3D kartézského souřadnicového systému k popisu polohy v těle. Kartézské souřadnicové systémy mají tu výhodu, že jsou známé a snadno pochopitelné. S tělem ve standardní anatomické poloze, vlevo-vpravo, kaudálně-kraniální a zadní-přední tvoří tři kolmé (X-y-z) osy. Pro analýzy v menším měřítku, Centrování původu na anatomický orientační bod může být nejužitečnější a potenciálně méně variabilní mezi různými lidmi. Například by bylo snazší měřit vzdálenost vzorku tkáně od ledviny k nadřazenému pólu ledviny než k horní části hlavy osoby. Nevýhodou kartézských souřadnic je to, že jeho osy nesledují přirozený tvar těla. Jako výsledek, vytvoření referenční mapy těla digitálně „sešitím“ vzorků tkáně odebraných od lidí různých velikostí by vyžadovalo složitý proces deformace, otáčení, a zarovnání dat. Dělat to způsobem, který se měří na celé tělo při zachování přesnosti na buněčné úrovni, by bylo nesmírně náročné.
Další 3D souřadnicové systémy byly vyvinuty pro různé aplikace. Například sférické souřadnice, osy reprezentující zeměpisnou šířku, délku a nadmořskou výšku, pohodlně popsat polohu na povrchu Země. Jednoduchá cesta ve sférických souřadnicích ,například „1 km na východ“, je mnohem obtížnější komunikovat pomocí kartézských souřadnic. Podobně, souřadnicové systémy pro lidské tělo by v ideálním případě mít os, které následují anatomických struktur, genetické exprese vzory, chemické gradienty, a/nebo jiné biologicky významné cesty. Bylo vyvinuto několik orgánově specifických souřadnicových systémů, jako jsou talairachovy souřadnice pro funkční zobrazování mozku, ale ty se nevztahují na celé tělo (6).
Cévní souřadnému Systému
V roce 2017, Společné Koordinovat Framework (CCF) Setkání organizoval Národní institut Zdraví, Broad Institute, Sanger Institute, a Chan Zuckerberg Initiative. Účastníci schůzky, která zahrnovala anatomy, patology, kliničtí lékaři, a technologie odborníků z celého světa, navrhl několik přístupů pro mapování buněk lidského těla, včetně anatomicky souřadnému systému (7). Jeden z nich, který používá vaskulaturu, byl dále diskutován na workshopu CCF 2019, konkrétně pro lokalizaci ledvinových buněk (8). V tomto rukopisu předkládáme koncepční přehled tohoto vaskulárního souřadného systému a popisujeme jeho výhody a omezení (Obrázek 1).
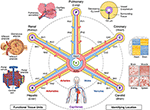
Obrázek 1. Struktura náboje a paprsku vaskulárního souřadnicového systému. Cévní souřadný systém se skládá z reprezentativní plavidlo smyček, které začínají a končí v komorách srdce a prodloužit funkční jednotky každého orgánu (proti směru hodinových ručiček od levého horního: sklípků, glomerulů, a jaterní lalůčky). „Adresa“ buňky obsahuje název smyčky (např. „R“ pro renální a „H“ pro jaterní) a větvení úroveň nejbližší nádoby (např. „RA1“ pro aferentní arterioly v ledvinách smyčky). Všimněte si, že stěny srdce leží podél věnčitých („C“) cévní smyčky, a buňky některých struktur uvnitř srdce jsou ve skutečnosti umístěn na okraji souřadný systém, v blízkosti kapilár, které poskytují jim s krví. Existuje několik způsobů, jak určit ještě přesněji „GPS-jako“ pozici, včetně, bude ve směru hodinových ručiček od vpravo, „hypoxie otisk prstu“, který vyplývá z klesající hladiny kyslíku dál od lodi, unikátní „histologické otisků prstů“ a „genové exprese otisků prstů“ v různých typech cévních endoteliálních buněk, a výrazný „vaskulární architektury otisků prstů“ nalézt v různých typech tkáně. Vaskulatura se rozšiřuje na všechny části těla (dno) a rámuje všechny orgány ve všech měřítcích. Zdrojové Soubory: Obrázky z jaterních lalůčků, glomerulů, sklípků, genová exprese heat map, a celé tělo, cévy jsou převzato z Wikimedia Commons: https://commons.wikimedia.org/wiki/File:2423_Microscopic_Anatomy_of_Liver.jpg (Public Domain); https://commons.wikimedia.org/wiki/File:Juxtaglomerular_Apparatus_and_Glomerulus.jpg (CC BY 3.0 licence); https://commons.wikimedia.org/wiki/File:Alveolus_diagram.svg (Public Domain); https://commons.wikimedia.org/wiki/File:Iris_dendrogram.png (CC BY-SA 4.0 licence); a, https://commons.wikimedia.org/wiki/File:Circulatory_System_en.svg (Public Domain). Tepelná mapa genové exprese vytvořená z Guo et al. (9) pomocí simulovaných dat. Cévní architektura založená na Bosetti et al. (10) (licence CC BY 4.0).
cílem vaskulárního souřadnicového systému není vytvořit mapu vaskulatury. Naopak, nápad je použít známý cévních cest přes tělo jako osu v souřadnicovém systému, které lze popsat polohu anatomických prvků, jako jsou buňky, tkáně obklopující cévy. V tomto navrhovaném rámci, srdeční komory mohou být považovány za původ v mapě celého těla. Cévní osa obsahuje cévní smyčky (srovnatelné s „silnice“ na Google Mapě, metafora), které rozšiřují prostřednictvím aorty nebo plicní tepny postupně zužují off na jeden mobilní velikosti jako mají přístup všechny ostatní buňky v každý orgán v těle, a vrátit se do srdce. Podél těchto cest, cév následuje jedinečný biologie z různých orgánů a tkání, a podobně, orgánů a tkání těla, nemůže existovat bez jedinečné vlastnosti jejich úzce integrované cév.
stejně jako genom mapa se odehrává DNA do lineární sekvence, můžeme si představit, rozkládání složitých 3D zvraty cév osy na jednodušší 2D „hub-and-spoke“ tvar s komorami srdce v centru. Toto schematické znázornění cév usnadňuje (1) popsat umístění v těle; (2) sladit cévních cest s různou 3D tvary, ale rovnocenné funkce od různých lidí; (3) identifikovat vzory, jako jsou změny v typu buněk a genové expresi jako jeden přechody z větších do menších cév v orgánu (po paprsku); a (4) porovnejte tkáň na stejné úrovni (např. kapiláry) v různých orgánech (napříč paprsky).
orgán, jako je ledvina, má desítky tisíc vaskulaturních drah, pokud je každá kapilára považována za zřetelně. Aby však byla konstrukce CCF proveditelná, učiníme další zjednodušující předpoklad, že mnoho z těchto cest je od sebe nerozeznatelné. Zejména nejmenší cévy (kapiláry) jsou ve středu malých specializovaných funkčních jednotek v každém orgánu (např.,jaterní laloky v játrech, glomeruly v ledvinách a alveoly v plicích). Celý orgán vyžaduje mnoho z těchto cév-střed funkční jednotky, které jsou anatomicky a fyziologicky podobné (11). Tato podobnost může být použita ke zhroucení četných cévních cest do několika reprezentativních (Obrázek 2). V budoucnu, jak se dozvíme více o biomolekulárních profilech těchto cest, můžeme vylepšit CCF rozdělením cest do všech objevených podtypů.

Obrázek 2. Rozvinutí renální vaskulární dráhy až na úroveň jedné buňky. Reprezentativní vaskulární cesta vstupuje do ledviny renální tepnou, prochází glomerulem a vrací renální žílu. Na makroskopu (vlevo) a mezoskale (uprostřed) jsou štítky ve žlutých krabicích anatomické struktury, které odpovídají různým nádobám podél této smyčky. Na mikroskopu (vpravo) jsou štítky ve žlutých krabicích různé typy buněk, které jsou v krátké vzdálenosti od blízké nádoby v glomerulu. Polohu jednotlivých buněk lze popsat podle adresy nejbližšího plavidla (např., „RA0“ pro glomerulární kapilární), vzdálenost v řádu mikrometrů nebo počet buněk z plavidla endotelu a úhlu kolmo k délce lodi (např. „RA0-10 µm-135°“ nebo „RA0-1c-135°“). Na pravé straně byla každá nádoba a její okolní tkáň extrahována z původního obrazu a zarovnána svisle, aby bylo snadné vidět, jak se mění typy buněk a distribuce podél cévní dráhy. V tomto příkladu byly zarovnané obrázky také otočeny tak, že střed glomerulu je vždy vpravo. Zdrojové Soubory: Obrazy ledvin a glomerulární jsou převzato z Wikimedia Commons: https://commons.wikimedia.org/wiki/File:KidneyStructures_PioM.svg (CC BY 3.0 licence); a https://commons.wikimedia.org/wiki/File:Renal_corpuscle-en.svg (CC BY-SA 4.0 license).
„adresa“ jednotlivé buňky ve vaskulárním souřadném systému má čtyři složky. (1) první je nejbližší anatomicky pojmenovaná nádoba, která nejpřesněji identifikuje vaskulární smyčku (vaskulární území nebo „povodí“), jako je pravá renální tepna. (2) další složka představuje úroveň větvení nádoby. V ledvinách, příklady z proximální do distální patří interlobárních tepny, kortikální vyzařovat tepny, aferentní arterioly, glomerulární kapiláry. Úroveň větvení může být také definována číselně, s kapilárami na nulové úrovni a vyššími úrovněmi s většími čísly. (3) třetí složkou je kolmá vzdálenost v mikrometrech nebo počet buněk od endotelové vrstvy cévy. (4) volitelnou čtvrtou složkou může být úhel natočení kolmý na délku nádoby. Nulové stupně lze definovat mnoha způsoby v závislosti na aplikaci. Například může být relativní k markeru na vzorku tkáně nebo může směřovat k anatomické struktuře, jako je střed nejbližšího glomerulu v ledvinách. Užitečnost a potřeba těchto komponent by musela být potvrzena experimentálním testováním.
dalším přístupem je použití endotelových buněk jako „kotevních buněk“ k identifikaci relativních pozic ostatních buněk způsobem podobným GPS. Endotel lemuje celou vaskulaturu. Odlišné endoteliální buňky (ES) typů se objevují v různých částech cévního systému, které mohou být zjištěny histologicky prostřednictvím jedinečné vlastnosti buňky a sousední buňky („histologické otisk prstu“), jakož i prostřednictvím analýzy jejich specifické genové profily („gene expression otisků prstů,“ Obrázek 1 mapa heat) (9, 12, 13). Cévní organizační struktura, složitost větvení, průměr atd. poskytněte další rozpoznatelné funkce, které tvoří „otisk cévní architektury“ pro každou tkáň (Obrázek 1 falešně barevné fluorescenční obrázky vaskulatury) (10, 14). Každá tkáň má specifické kyslíkové gradienty, které lze použít k určení vzdálenosti od cévy. Když PO2 nelze měřit přímo, lze odvodit buňky vzdálenost od indukce/výraz přechody hypoxií indukovatelných genů v různých typech buněk („hypoxie otisků prstů,“ Obrázek 1 příčné zobrazení plavidla) (15-17).
výhody vaskulárního CCF
souřadnicový systém vaskulatury má smysl biologicky. Každá živá buňka musí být v malém okruhu nejbližší cévy (100 µm až 1 mm, v závislosti na tkáni) za účelem získání kyslíku (18); a každá nádoba je lemována stejnou souvislou vrstvou endotelu (19). To znamená, že cévy tvoří nepřerušenou cestu, která dosáhne do všech částí těla, plynule se zužující dolů přes váhy, z macroscale (celé tělo/klinické) mesoscale na microscale (single cell-velikost kapilár). V rámci toho se zabývá postupným přechodem od velkých tepen a žil, které jsou u většiny lidí zachovány, až po miliony mikroskopických cév, které jsou rozpoznatelné podle kategorie (např. Cévní systém se přizpůsobuje individuální velikosti a tvaru těla, což odpovídá interindividuálním variacím (20, 21). Definuje tvar funkčních jednotek v různých orgánech, jako jsou jaterní laloky, glomeruly ledvin a plicní alveoly. Normální vývoj nové tkáně začíná tvorbou cév dříve, než kolem ní mohou růst další typy buněk (22).
cévní systém také sousedí se všemi orgány, tkáněmi a buňkami. Zdá se, že jiné anatomické struktury nemají podobnou všestrannost. Například kosterní systém se rozšiřuje na celé tělo; vzdálenost od buňky uvnitř orgánu k nejbližší kosti však může být několik centimetrů a tato kost pravděpodobně nebude součástí orgánu a ještě méně pravděpodobně bude součástí vzorku tkáně. Nervového systému, následuje mnoho stejných cest jako větší lodě investoval s kontraktilní vlastnosti, ale není známo, zda se rozšiřují následovat menší plavidla, které dosahují všechny tkáně. Na rozdíl od závislosti buněk na kyslíku tedy neexistuje záruka, že každá buňka je v těsné blízkosti nervu. Orgánově specifické referenční systémy jsou založeny na jedinečné konstrukční vlastnosti, které existují pouze v tom, že jednotlivé orgánové (např. specifické oblasti mozku) a je nepravděpodobné, že být užitečné pro zastupování buňky místech jinde v těle.
existuje mnoho praktických výhod vaskulárního souřadného systému. Cévní cesty ve všech orgánech byly rozsáhle studovány a jsou podrobně popsány v literatuře. Jsou užitečné, dobře známý, a mají standardizované názvy v mnoha specializovaných doménách. Tkáňové vaskularizační vzorce se klinicky používají k diagnostice onemocnění; a cévy se používají v chirurgii a biopsiích jako hlavní anatomické orientační body a definují “ vaskulární území „(23, 24). Ačkoli přesná poloha ve 3D kartézském prostoru může být obtížné určit pro vzorek resekované tkáně, chirurg bude obvykle schopen určit, které cévní povodí zahrnovalo vzorek.
omezení vaskulárního CCF
pouze znalost párů bází v genomové sekvenci neposkytuje dostatek informací k určení, jak je DNA složena v konkrétní buňce. Podobně, i když rozložil cévní systém souřadnic lze popsat 3D prostorové vztahy okolních buněk na microscale, klikaté cesty, které plavidel vzít a relativní vzdálenost mezi buňkami na větší váhy, je ztracen. Informace o strukturách ve větším měřítku lze získat integrací klinického zobrazování a histologického a molekulárního vzorování.
některé další poziční informace jsou ztraceny zhroucením cévních drah. Například, cévní souřadný systém může zpočátku léčit všechny glomerulární kapiláry v ledvinách jako stejné struktury, případně maskování rozdíly v glomerulech na vyšší a nižší renální poláci. Ačkoli, jak se dozvídáme více o biomolekulárních profilech těchto drah, můžeme iterativně zpřesnit vaskulární CCF v průběhu času rozdělením cest do všech objevených podtypů.
i Přes tato omezení, cévní souřadný systém zachovává dost poziční informace, odpovědět na mnoho typů výzkumných otázek, tím, že vědci přesně lokalizovat jednotlivé buňky v rámci funkčních celků, tkání a orgánů, nebo porovnat účinky souvislosti na různé typy buněk, přes celé tělo na makro – a mezo – váhy.
další kroky a budoucí směry
Na obrázku 1 představujeme vysoce zjednodušenou a stylizovanou reprezentaci vaskulárního CCF, abychom představili obecný koncept. Aktuální cévních cest jsou daleko složitější, s plnou cévní CCF nakonec skládající se ze stovek nebo tisíců struktur, stejně jako větvení vzory, které nemají dodržovat přísná hub-and-spoke rozložení. Například, žil v jaterní portální systém, které přivádějí krev z různých orgánů do jater a krevního oběhu anastomózy, jako Willisův okruh v mozku, by se spustit kolmo, a přes „paprsky“ na Obrázku 1.
vaskulární CCF bude také muset začlenit normální anatomické varianty vaskulatury, jako je thyroidea ima a dvojité cystické tepny, stejným způsobem, jakým jednonukleotidové polymorfismy (SNP) popisují normální variace v genomu. Jak jsme se rozšířit a vyplnit údaje o cévní CCF, to může trvat na více vločka nebo web-jako vzhled, s pravděpodobností rozděleny do různých sekcí, aby se vyjadřují pravděpodobnost nálezu je v danou osobu.
aktuální cévní CCF bude vyžadovat propracovanější kódování schéma pro pojmenování plavidla, než to, co je znázorněno na Obrázku 1, s cílem reprezentovat jeho složitosti přesněji a aby to „vypočitatelná“ podle softwarové algoritmy. Jeden přístup je, aby stavět na existující anatomické ontologie, jako UBERON, který již obsahuje unikátní Uniform Resource Identifikátory Uri () pro mnoho plavidel a definuje vztah různých typů, jako je „branching_part_of,“ popsat, jak cév connect (25).
buňka může být v blízkosti více než jedné nádoby, v takovém případě je možné jí přiřadit samostatnou adresu vzhledem ke každému plavidlu. Budoucí výzkum je nutný k určení, jaká by měla být vhodná“ mezní “ vzdálenost. Mohlo by být žádoucí uložit více adres pro buňky, které pomohou triangulovat jejich polohu ve 3D prostoru.
i když naše prvotní motivace pro cévní CCF je definovat souřadný systém pro určení polohy buněk, román radiální uspořádání lidského těla po cévní, jak je znázorněno na Obrázku 1, může mít jiné vědecké aplikace. Například, poziční informace v tomto rámci má analogie na embryologic rozvoji a může poskytnout vhled do mechanismů, které způsobují onemocnění nebo dysregulations, které vznikají ze skupiny buněk. Například v cévní CCF, makrovaskulární onemocnění spojená s diabetem 2. typu (např. ischemická choroba srdeční, periferní vaskulární choroby a cerebrovaskulární choroby) jsou sdružené v blízkosti centra, zatímco mikrovaskulární onemocnění (např. retinopatie, nefropatie a neuropatie) tvoří kruh kolem vnější (26).
Shrnutí
cévní systém má několik vlastností, které odpovídají charakteristice dříve považovány za žádoucí pro CCF povolit mapování všech buněk v lidském těle (7). (1) funguje v několika měřítcích. Prostřednictvím kontinuálního endotelu vytváří plynulý přechod od velkých anatomických struktur až po buněčnou úroveň. (2) je použitelný pro všechny tělesné tkáně. Protože se orgány vyvíjejí kolem cév, vaskulatura rámuje architekturu orgánů ve všech měřítcích. Cévní vzory jsou tak výrazné, že obrazy samotných cév, se všemi ostatními buňkami odstraněnými, lze snadno použít k identifikaci orgánu. (3) představuje rozdíly mezi dárci. Vaskularizace se přirozeně přizpůsobuje individuálním variacím tkáně, velikosti těla a tvaru. Místo toho, aby mapa 3D souřadnice každého glomerulu v jedné osobě, aby se ti v jiné osobě, cévní CCF by se poloha každé buňky v rámci reprezentativní glomerulární kapilární od každé osoby. (4) cévní je dobře známo, že lékaři různých klinických oborů, pomáhá jak diagnostikovat onemocnění a vést operace, a používá se jako orientační body, patologové, radiologů, a dalších lékařů. To by usnadnilo umístění vzorků tkáně v těle a registraci umístění jednotlivých buněk. Zatímco žádná CCF je ideální pro všechny případy použití, cévní CCF definuje přirozený souřadný systém, který bude dělat to snadné kombinovat biomolekulární data od více lidí a zeptat biologicky relevantní výzkumné otázky.
Prohlášení o dostupnosti dat
veřejně dostupné datové sady byly analyzovány v této studii. Tato data lze nalézt zde: https://www.proteinatlas.org.
autorské příspěvky
GW koncipovala tuto studii na základě zpráv ze setkání CCF 2017 a Workshopu CCF 2019. KB a YJ poskytly kritickou zpětnou vazbu. GW napsal Počáteční návrh, s dalším textem přepsaným z prezentace snímků CCFWS-01. Všichni autoři přispěli k úpravě rukopisu.
financování
tento výzkum byl podpořen National Institutes of Health (NIH) award OT2OD026671. Tato práce nepředstavuje názor NIH nebo Národního institutu pro srdce, plíce a krev (NHLBI).
střet zájmů
autoři prohlašují, že výzkum byl proveden bez jakýchkoli obchodních nebo finančních vztahů, které by mohly být vykládány jako potenciální střet zájmů.
poděkování
Děkujeme Dr. Zorině s. Galis z National Institutes of Health pomáhá rozvíjet myšlenku cévní souřadnému systému v roce 2017 CCF Setkání a 2019 CCF Dílny, poskytuje nám s prezentací z těchto událostí, a které se účastní četné diskuse, které tvořily základ tohoto rukopisu. Odborné připomínky recenzentů pomohly objasnit a podrobně popsat navrhovaný společný souřadný systém založený na cévách.
3. Uhlén M, Björling E, Agaton C, Szigyarto CA, Amini B, Andersen E, et al. Atlas lidského proteinu pro normální a rakovinné tkáně založené na proteomice protilátek. Proteomika Mol Buněk. (2005) 4:1920–32. doi: 10.1074 / mcp.M500279-MCP200
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
12. Vanlandewijck M, He L, Mäe MA, Andrae J, Ando K, Del Gaudio F, et al. Molekulární atlas buněčných typů a zonace v mozkové vaskulatuře. Povaha. (2018) 554:475–80. doi: 10.1038/nature25739
PubMed Abstract | CrossRef Full Text | Google Scholar
14. Johnson C, Sung HJ, Lessner SM, Fini ME, Galis ZS. Matrix metalloproteinase-9 is required for adequate angiogenic revascularization of ischemic tissues: potential role in capillary branching. Circ Res. (2004) 94:262–8. doi: 10.1161/01.RES.0000111527.42357.62
PubMed Abstract | CrossRef Full Text | Google Scholar
15. De Santis V, zpěvák M. monitorování tkáňového kyslíkového napětí perfúze orgánů: zdůvodnění, metodiky, a přehled literatury. Br J Anaesth. (2015) 115:357–65. doi: 10.1093/bja/aev162
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
17. Koch CJ. Měření absolutních hladin kyslíku v buňkách a tkáních pomocí kyslíkových senzorů a 2-nitroimidazolu EF5. Metody Enzymol. (2002) 352:3–31. doi: 10.1016/S0076-6879(02)52003-6
PubMed Abstract | CrossRef Full Text | Google Scholar
20. Paruchuri V, Salhab KF, Kuzmik G, Gubernikoff G, Fang H, Rizzo JA, et al. Aortic size distribution in the general population: explaining the size paradox in aortic dissection. Cardiology. (2015) 131:265–72. doi: 10.1159/000381281
PubMed Abstract | CrossRef Full Text | Google Scholar
21. Abadi E, Segars WP, Sturgeon GM, Roos JE, Ravin CE, Samei e. modelování plicní architektury v sérii fantomů XCAT: fyziologicky založené dýchací cesty, tepny a žíly. IEEE Trans Med Imaging. (2018) 37:693–702. doi: 10.1109 / TMI.2017.2769640
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
24. Majno P, Mentha G, Toso C, Morel P, Peitgen HO, Fasel JH. Anatomie jater: obrys se třemi úrovněmi složitosti-další krok směrem k přizpůsobeným teritoriálním resekcím jater. J. (2014) 60:654–62. doi: 10.1016/j.jhep.2013.10.026
PubMed Abstract | CrossRef Full Text | Google Scholar
26. Cade WT. Diabetes-related microvascular and macrovascular diseases in the physical therapy setting. Phys Ther. (2008) 88:1322–35. doi: 10.2522/ptj.20080008
PubMed Abstract | CrossRef Full Text | Google Scholar