Speciální cukr: jak se kyseliny sialové dopady na metabolismus, zdraví a nemoci
Jsme se hemží mikroby, které žijí na povrchu vně i uvnitř našich těl. Naše chápání střevního mikrobiomu zejména se rychle zlepšuje, jak jsme se začít rozpárat, jak složité mikrobiální komunity komunikovat s naší stravy, s jinými mikroby a s naší mobilní povrchy. Zatímco mnoho chemikálií je v tomto prostředí důležité, zde se zaměřujeme na kyseliny sialové jako kritickou sadu molekul, které podporují mnoho z těchto interakcí a ovlivňují metabolismus, zdraví a nemoci.
nejběžnější kyselina sialová, kyselina N-acetyl-neuraminová (Neu5Ac) (obr. 1) je relativně jednoduchá cukrová kyselina, která kromě svého náboje nemá nic neobvyklého. Nicméně, když buňky kontaktovat ostatní buňky se často používají molekuly zobrazí na povrchu, a to je místo, kde sialové kyseliny tak důležité, protože oni jsou obvykle terminálu cukrů na hostitelské glykany, že pepř proteiny a lipidy sedí na povrchu buněk. Buňka-povrch nebo vylučovaný hlen glykoproteiny jsou dobré příklady sialové kyseliny-potažené struktury, které mikroby, které by mohly nastat na slizniční povrchy, jako je například respirační nebo gastrointestinální (GI) traktu. Tato jedinečná pozice molekuly „meet and greet“ pro jiné lidské buňky, bakteriální buňky a viry staví kyseliny sialové do centra pro mnoho důležitých procesů.
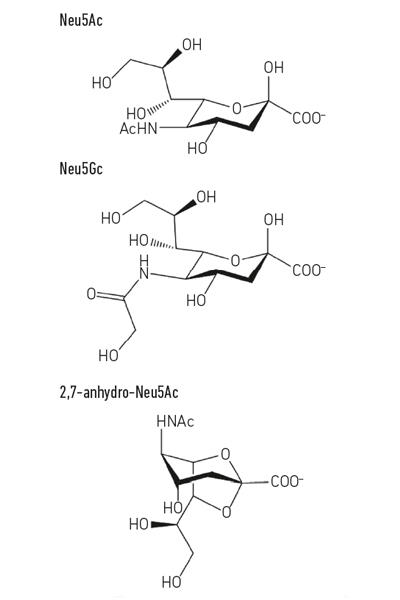
- obr. 1. Příklad derivátů kyseliny sialové. Všimněte si, že N-glycolyl-neurnaminic kyseliny (Neu5Gc) nemůže být ze strany člověka, biochemické rozdíl, který nás odlišuje od ostatních lidoopů, ale mohou být začleněny do našich povrchu buněk, kdy získané ze stravy.
- Cukr-potažené patogeny,
- Cross-krmení – sdílení sladkosti kolem
- obr. 2. Kreslená ilustrace různých interakcí mezi bakteriemi a kyselinami sialovými přítomnými jako terminální cukry na řadě hostitelských glykanů. Ty jsou štěpeny sialidázami a obvykle převedeny na volný Neu5Ac s výjimkou IT-sialidázy, která uvolňuje 2,7-anhydro-Neu5Ac. Zdarma kyseliny sialové vydané hostitele nebo patogenní sialidases pak mohou být použity patogeny jako neviditelný plášť (a), nebo pro krmení (b). Kříž krmení může dojít mezi členy střevní mikroflóry nebo mezi komenzální a patogenní bakterie sdílení stejný výklenek (c, d), zatímco jiné bakterie vyvinuly sobecký mechanismy rezervovat kyseliny sialové pro vlastní spotřebu (e).
- drží držet své vlastní sladkosti,
- Viry dostat na aktu
- další čtení
- Andrew Bell
- Emmanuele Severi
- Nathalie Juge
- Gavin Thomas H.
- proč záleží na mikrobiologii?
- Jakou radu byste dal někomu, kdo začíná v této oblasti?
obr. 1. Příklad derivátů kyseliny sialové. Všimněte si, že N-glycolyl-neurnaminic kyseliny (Neu5Gc) nemůže být ze strany člověka, biochemické rozdíl, který nás odlišuje od ostatních lidoopů, ale mohou být začleněny do našich povrchu buněk, kdy získané ze stravy.
Cukr-potažené patogeny,
Jeden z prvních mikrobiální funkce sialové kyseliny byl připojen ke schopnosti některých patogenů kolonizovat a způsobit onemocnění u lidí. Bývalý prezident mikrobiologické společnosti, profesor Harry Smith FRS, pracující na univerzitě v Birminghamu, propagoval tuto práci s Neisseria gonorrhoea. Když vědci v jeho skupině izolované chybu přímo z těla, to bylo odolné proti zabíjení lidské sérum (komplementem zprostředkované zabíjení), ale kdyby chyby byly kultivovány v laboratoři pro několik generací, tato ochrana byla ztracena a buňky byly zabity v séru. Jeho skupina zjistila, že tyto patogeny kradou kyselinu sialovou z hostitele a používají ji k potahování vlastního buněčného povrchu, aby je humanizovaly. Protože však mohou tuto kyselinu sialovou pouze uklízet, její nepřítomnost v růstovém médiu znamená, že se nepřidává žádná další kyselina sialová, takže rychle ztratí tuto „ochranu séra“ a jsou usmrceni. Ukazuje se, že řada dalších záludný chyby použití podobné strategie vytvářet své vlastní neviditelný plášť pomocí sialové kyseliny, jako je Neisseria meningitidis, Campylobacter jejuni nebo Haemophilus influenzae (Obr. 2a)
Cross-krmení – sdílení sladkosti kolem
stejně Jako se používá patogeny jako neviditelný plášť, sialové kyseliny jsou docela dobré jídlo pro bakterie, protože poskytují oběma uhlíku a dusíku, a mohou být použity jako zdroj energie. Dřívější práce ukázaly, že patogeny, jako je Vibrio cholerae, byly šťastné, že jedly kyseliny sialové, a to samo o sobě bylo důležité pro úspěšnou kolonizaci hostitele (obr. 2b).
ve střevě pochází hlavní zdroj sialových kyselin z mucinů, které jsou hlavními strukturálními složkami vrstvy hlenu pokrývající povrch epitelu. Nejexponovanější vrstvou hlenu je domovem různých komenzální bakterie, které se naučili, jak hodovat na mucin, proteiny, kde cukrů 80% jejich hmoty. Z jednoduché topologické pohledu, sialové kyseliny, jako terminálu cukry, jsou sklizeny první, vystavovat základní cukry, které mohou být také následně propuštěn a jíst. S příchodem sekvenování nové generace jsme získali znalosti o mikrobech žijících v tomto výklenku a mnoho z nich má geny pro vychytávání kyseliny sialové a následný katabolismus. Co bylo zajímavé bylo zjištění, že některé komenzální anaeroby jako Bacteroides thetaiotaomicron, vylučují sialidases k uvolnění kyseliny sialové, ale nedostatek transportérů a katabolické geny skutečně používat. Tento zdánlivě altruistické gesto je potřebné pro bakterie přístup k hlubších cukrů a přispívá k procesu metabolismu cross-krmení pro ostatní brouky žijící v hlenu výklenku, jako komenzální kmeny Escherichia coli, které nemají sialidase ale jsou dobrý v jídle, zdarma sialové kyseliny (Obr. 2c). Tento koncept je nyní uznáván jako důležitý aspekt kolonizace a přizpůsobení se výklenkům. Brilantní vyjádřením tohoto byl popsán skupinou Justin Sonnenburg ze Stanford University, pomocí myši model s jednoduchým definovanými střevní mikroflóry. Po léčbě antibiotiky bylo mnoho bakterií konzumujících kyselinu sialovou vymazáno, což vedlo k akumulaci volné kyseliny sialové ve střevě. Když pak napadal s patogeny, jako je Salmonella typhimurium nebo Clostridium difficile, tyto patogeny by měli prospěch z volné kyseliny sialové jako živiny (Obr. 2d). Mutantní kmeny patogenů chybí transportéry nebo katabolické geny neměl výhodu, vytvoření přímého připojení k patogenu následek, když střevní mikrobiální společenství je narušen. Mechanismy ke snížení množství volné kyseliny sialové ve střevě byly proto navrženy jako součást nové protiinfekční strategie.
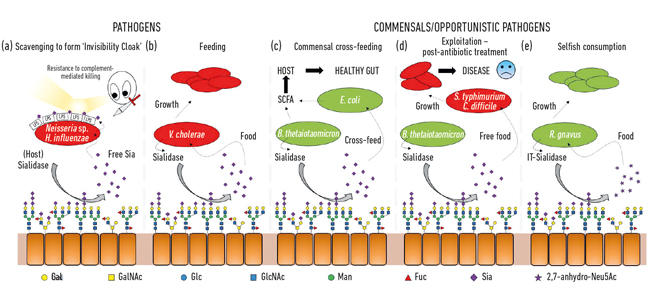
obr. 2. Kreslená ilustrace různých interakcí mezi bakteriemi a kyselinami sialovými přítomnými jako terminální cukry na řadě hostitelských glykanů. Ty jsou štěpeny sialidázami a obvykle převedeny na volný Neu5Ac s výjimkou IT-sialidázy, která uvolňuje 2,7-anhydro-Neu5Ac. Zdarma kyseliny sialové vydané hostitele nebo patogenní sialidases pak mohou být použity patogeny jako neviditelný plášť (a), nebo pro krmení (b). Kříž krmení může dojít mezi členy střevní mikroflóry nebo mezi komenzální a patogenní bakterie sdílení stejný výklenek (c, d), zatímco jiné bakterie vyvinuly sobecký mechanismy rezervovat kyseliny sialové pro vlastní spotřebu (e).
drží držet své vlastní sladkosti,
Zatímco mnoho začátku sialomicrobiology zaměřuje na patogeny, novější práce se zaměřuje na komenzálních bakterií obývajících stejné niky. Dnešní studie v oblasti střevní mikrobioty odhalují, jak tvrdá je konkurence Neu5Ac v našem střevě a jak může narušit rovnováhu mezi patogeny a komenzály. Co kdyby určitá bakterie mohla uvolňovat kyselinu sialovou ve formě, ke které by měla přístup pouze ona? Práce v Juge Skupiny v Norwichi ukázal, že střevní symbionta Ruminococcus gnavus se vyvinul, aby tak učinily, pomocí speciální typ sialidase tzv. intramolekulární trans-sialidase (JE-sialidase), který uvolňuje 2,7-anhydro-Neu5Ac (viz Obr. 1) místo Neu5Ac. Tím, že rozvíjí metoda syntetizovat čisté 2,7-anhydro-Neu5Ac, se ukázalo, že R. gnavus kmeny byly schopny růst na 2,7-anhydro-Neu5Ac jako jediný zdroj uhlíku. Kromě domény katalyzující enzymatickou reakci obsahují it-sialidázy doménu vázající sacharidy, která pomáhá zprostředkovat vazbu IT-sialidázy na muciny bohaté na kyselinu sialovou. In vivo to může podpořit mechanismus, který pomáhá zaměřit bakterie na oblasti GI traktu bohaté na kyselinu sialovou, a proto podporuje bakteriální kolonizaci ve vrstvě hlenu. Jakmile se nachází na správném místě, JE-sialidase štěpí z kyseliny sialové z terminálu řetězce muciny a uvolňuje ji ve formě, 2,7-anhydro-Neu5Ac, že R. gnavus lze použít jako vlastní zdroj potravy, spíše než sdílení Neu5Ac s jinými bakterie obývající hlenu výklenek, včetně patogenů (Obr. 2e). Tento mechanismus poskytuje konkurenční výhodu nad ostatními sialové kyseliny – jíst bakterie obývající hlenu výklenek, tím, že poskytuje zdroj živin, že to může přednostně přístup. Kromě toho, R. gnavus může také pomoci snížit následek střevními patogeny tím, že snížení úrovně Neu5Ac v slizniční prostředí, otevření způsoby, jak nové léčebné strategie v době rostoucí rezistence vůči antibiotikům.
Viry dostat na aktu
Viry také použít sialové kyseliny jako klíčové molekuly během jejich infekce cyklu, nejvíce skvěle virus chřipky. Počáteční připojení je prvním klíčovým krokem, protože kyseliny sialové fungují jako receptory viru na respiračních epiteliálních buňkách. Typ spojení sialové kyseliny do hlubších cukrů v glykany často řídí hostitelské spektrum virů chřipky a pandemické kmeny mají často přilnavost bílkovin (hemaglutinin), které uznává člověka jako formy kyseliny sialové přílohu, a tak jsou zvláště virulentní. Kyselina sialová je důležitá v poslední fázi virového životního cyklu, protože uvolňování z infikované buňky vyžaduje štěpení kyselin sialových z povrchu hostitelské buňky. To je katalyzováno virovým enzymem zvaným sialidáza (nebo neuraminidáza). Inhibice tohoto enzymu pomocí strukturální analogy kyseliny sialové, formulovány do Tamiflu® (Oseltamivir fosfát) a Zanamivir, jsou naše první linie léčby chřipky a triumf struktury/funkce inspiroval drug design.
závěrem je zřejmé, že kyseliny sialové jsou kritické molekuly v mnoha procesech, kde mikrobiální buňky a viry interagují s povrchy savčích buněk. V tomto krátkém článku, jsme se dotkli na některé z nich pro představu centrální funkce těchto cukrů v komunikaci, stealth, kolonizaci a metabolismus v různých aspektech zdraví a nemoci. Kyseliny sialové byly popsány jako nejdůležitější chemikálie na světě a bezpochyby budou i nadále odhalovat více o vývoji lidí a jejich souhře s jejich mikroby.
další čtení
Thomas, GH. Získávání kyseliny sialové v bakteriích-jeden substrát, mnoho transportérů. Biochem Soc Trans 2016; 44: 760-765.
Ng KM, Ferreyra JA, Higginbottom SK, Lynch JB, Kashyap PC et al. Hostitelské cukry osvobozené od mikrobioty usnadňují post-antibiotickou expanzi enterických patogenů. Příroda 2013; 502: 96-99.
Owen CD, Tailford LE, Monaco S, Šuligoj T, Vaux L et al. Odhalení specifičnosti a mechanismu rozpoznávání kyseliny sialové střevním symbiontem Ruminococcus gnavus. Nat Commun 2017; 8: 2196.
Tailford LE, Owen CD, Walshaw J, Crost EH, Hardy-Goddard J, Le Gall G, de Vos WM, Taylor GL, Juge N. Objev intramolekulární trans-sialidases v lidské střevní mikroflóry naznačuje, román mechanismy slizniční adaptace. Nat Commun 2015; 6:7624.
Juge N, Tailford L, Owen CD. Sialidázy ze střevních bakterií: mini-recenze. Biochem Soc Trans 2016; 44: 166-175.

Andrew Bell
Quadram Ústav Bioscience, Norwich Research Park, NR4 7UQ, velké BRITÁNII,
Andrew Bell je postgraduální student na Katedře Střevní Mikroby a Zdraví v Quadram Ústavu studium vlivu román mechanismus sialové kyseliny metabolismus na střevní homeostázy. Získal titul BSc v Biochemii na University of East Anglia a strávil 2 roky pracoval v John Innes Centre na chlorofyl metabolismus v hrachu (Pisum sativum) před nástupem Nathalie Juge skupiny na Quadram Ústavu v roce 2015 pro své doktorské práce.

Emmanuele Severi
Katedře Biologie, University of York, Wentworth Způsob, York YO10 5DD, velké BRITÁNII,
@emm_severi
Emmanuele Severi je post-doktorský vědecký pracovník v Oddělení Biologie na Univerzitě v Yorku pracuje v laboratoři Prof Gavin Thomas. Ve své kariéře pracoval na transportu a metabolismu kyseliny sialové v různých dobách a od roku 2002 je členem společnosti.

Nathalie Juge
Quadram Ústav Bioscience, Norwich Research Park, NR4 7UQ, velké BRITÁNII,
Nathalie Juge je Vedoucí Výzkumu na Quadram Ústav Bioscience (QIB) v Norwich, Zástupce vedoucího Ústavu Strategických Programu, Střevní Mikroby a Zdraví (GMH) a Čestný Profesor na School of Biological Sciences, University of East Anglia. Vede Výzkumnou Skupinu na glycobiology host-mikrob interakce ve střevech se zaměřením na mucin-odvozené sialové kyseliny metabolismus prostřednictvím střevní mikroflóry (https://quadram.ac.uk/nathalie-juge).

Gavin Thomas H.
Katedře Biologie, University of York, Wentworth Způsob, York YO10 5DD, velké BRITÁNII,
@GavinHThomas
Gavin H. Thomas, Profesor Mikrobiologie v Oddělení Biologie na University of York a pracoval na bakteriální kyseliny sialové transport a katabolismus pro více než deset let. Byl členem Společnosti od roku 1995, byl Editor Mikrobiologie Dnes (2003-2006), které slouží v Radě ve stejném období, podává na Komunikační výbor (2012-2015) a Rovnost & Rozmanitost výboru (2013-2015). Byl redaktorem, vedoucím redaktorem a nyní je zástupcem šéfredaktora předního časopisu mikrobiologie společnosti (http://thomaslabyork.weebly.com).
proč záleží na mikrobiologii?
Gavin: Záleží na našem zdraví-teprve nyní skutečně začínáme chápat molekulární složení a funkci našeho mikrobiomu, což pravděpodobně ovlivňuje naše tělo mnoha způsoby.
Jakou radu byste dal někomu, kdo začíná v této oblasti?
Gavin: Přečtěte si široce a mimo „vaši chybu – – mikrobi mohou dělat skoro všechno a obvykle vynalezli několik různých způsobů, jak to udělat!
obrázky: částice viru chřipky H3N2. CDC / Science Photo Library.
Obr. 1. Andrew Bell.
Obr. 2. Emmanuele Severi.