Univerzální Rozpouštědlo
Univerzální Rozpouštědlo
Toto je, samozřejmě, další klíčovou vlastnost vody, protože více látky se rozpustí ve vodě, než jakékoli jiné běžné kapaliny. Je to proto, že molekula polární vody zvyšuje “ rozpouštěcí sílu.“Rozpouštění zahrnuje rozbití „solí“ na ionty složek.“Například NaCl (kuchyňská sůl) rozloží na ionty Na+ a Cl -, protože přitažlivost pro ionty (atomy nebo skupiny atomů s poplatkem) pro molekuly vody je vysoká.
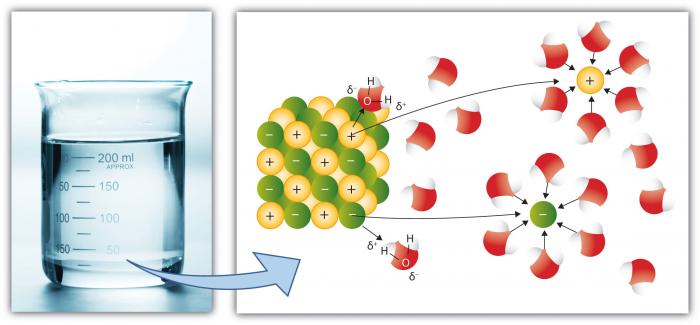
Kationty, jako je Na (Sodík), mají kladný náboj, zatímco anionty (například Cl, Chlorid) mají záporný náboj. Existuje mnoho jednotlivých prvků a sloučenin, které tvoří ionty. Voda tak může mít značné koncentrace různých chemických druhů v závislosti na jejich konkrétních vlastnostech. Všimněte si, jak molekuly vody obklopují jednotlivé ionty a udržují je izolované od ostatních iontů v roztoku. K tomu dochází, dokud není překročena kapacita vody k izolaci iontů, kdy je roztok „nasycen“ těmito ionty a nemůže se více rozpouštět (sůl se začne srážet-vytvoří pevnou látku).