Vitamin C: Antioxidant Agent
Redox metabolismus a antioxidační vlastnosti vitaminu C
Volné radikály a oxidanty hrají dvojí roli jako toxické a prospěšné sloučeniny, v metabolických procesů a v reakci na exogenní podněty. Vyrábějí se buď z normálních metabolických aktivit, nebo z faktorů prostředí(znečištění, cigaretový kouř a záření). Když přetížení volných radikálů nelze vyčistit, jejich akumulace v těle vytváří oxidační stres . Oxidační stres nastává, když tvorba volných radikálů překračuje schopnost ochrany proti nim. Tento proces vede k rozvoji chronických a degenerativních onemocnění, jako je rakovina, autoimunitní poruchy, stárnutí, katarakta, revmatoidní artritida, kardiovaskulární a neurodegenerativní onemocnění . Antioxidant je molekula, která zabraňuje oxidaci jiných molekul. Oxidační proces je chemická reakce, která produkuje volné radikály, což vede k řetězovým reakcím, které mohou poškodit buňky. Antioxidační účinek vitaminu C byl dobře zdokumentován . Vitamin C je silný antioxidant, který má schopnost darovat atom vodíku a tvoří relativně stabilní askorbyl – volný radikál. Vitamin E, vitamin C a β-karoten jsou známé jako antioxidační vitamíny, které jsou navrženy ke snížení oxidačního poškození a snížení rizika některých chronických onemocnění. Nemoci, jako jsou kardiovaskulární poruchy, jsou v epidemiologických studiích spojeny s nedostatečnými koncentracemi kyseliny L-askorbové, tokoferolu a β-karotenu. Vitamin C také zvyšuje absorpci železa snížením Fe3 + na Fe2+ z nehemových zdrojů železa . V přítomnosti redox-aktivní ionty (železo, měď), vitamín C působí jako prooxidační, které přispívají k tvorbě hydroxylových radikálů, které mohou vést k lipidů, DNA nebo proteinové oxidace . Existují různé mechanismy pro zmírnění oxidačního stresu a opravu poškozených makromolekul. Enzymatické a neenzymatické antioxidanty mají důležitou roli při odstraňování volných radikálů a reaktivních druhů kyslíku (ROS). Antioxidačních enzymů katalázy (CAT), superoxiddismutáza (SOD), glutathion reduktázy (GR), glutathion peroxidázy (GSHpx) a v rostlinách, askorbátu peroxidáza (AA-px) a nonenzymatic antioxidantů, včetně glutathion (GSH) a askorbátu (ASC), se ukázaly být výrazně ovlivněny oxidační stres . Antioxidační sloučeniny mohou zabránit nekontrolované tvorbě volných radikálů nebo inhibují jejich reakce s biologickými lokalit; také, zničení většiny volných radikálů závisí na oxidaci endogenních antioxidantů, především úklidu a snížení molekuly . Vitamin C je považován za důležitý antioxidant rozpustný ve vodě, o kterém se uvádí, že neutralizuje ROS a snižuje oxidační stres .
Vitamin C je silným redukčním činidlem a vychytávačem volných radikálů v biologických systémech . Podílí se na první linii antioxidační obrany, chrání lipidové membrány a proteiny před oxidačním poškozením. Jako molekula rozpustná ve vodě může vitamin C pracovat uvnitř i vně buněk a může neutralizovat volné radikály a zabránit poškození volnými radikály. Vitamín C je vynikajícím zdrojem elektronů pro volné radikály, které hledají elektron získat jejich stabilitu. Vitamin C může darovat elektrony volným radikálům a uhasit jejich reaktivitu .
Vitamin C bylo prokázáno, že být efektivní scavenger proti kyslíku a oxidu dusíku druhů, jako je superoxid radikál ion, peroxid vodíku, hydroxylový radikál, a singletního kyslíku. Tato vlastnost vitaminu C má životně důležité procesy v ochraně buněčných složek před poškozením způsobeným volnými radikály. Kromě toho je vitamin C účinný při regeneraci antioxidační formy vitaminu E snížením tokoferoxylových radikálů. Tento proces chrání membrány a další kompartmenty buňky před poškozením způsobeným volnými radikály (Obrázek 2). Askorbát peroxidáza (APX) je enzym redukující H2O2 na vodu pomocí askorbátu jako donoru elektronů. Monodehydroaskorbát je oxidovaný askorbát, který je regenerován monodehydroaskorbátreduktázou (MDAR). Monodehydroaskorbátový radikál se rychle disproporcionuje na askorbát a dehydroaskorbát. Dehydroascorbate is reduced to ascorbate by dehydroascorbate reductase in the presence of GSH, yielding oxidized glutathione (GSSG). It is reduced by glutathione reductase (GR) using nicotinamide adenine dinucleotide phosphate hydrogen (NADPH) as an electron donor. Dehydroascorbate may be reduced nonenzymatically or catalyzed by proteins with dehydroascorbate reductase (DHAR) activity.
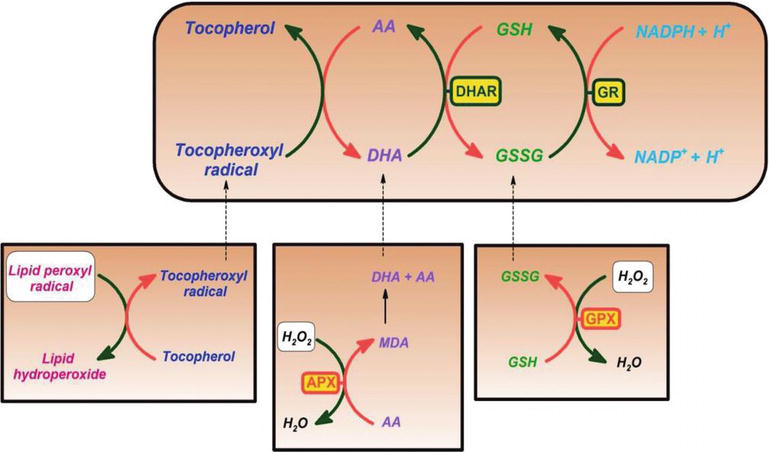
Figure 2.
xmlns:mml=“http://www.w3.org/1998/Math/MathML“ xmlns:xlink=“http://www.w3.org/1999/xlink“ xmlns:xsi=“http://www.w3.org/2001/XMLSchema-instanceAscorbate and redox cycling antioxidants. AA, ascorbate; DHA, dehydroascorbate; DHAR, semidehydroascorbate reductase; GSH, glutathione; GSSG, semi-glutathione reductase; GR, glutathione reductase; APX, ascorbate peroxidase; and GPX, glutathione peroxidase .
Glutathione-ascorbate cycle operates in the cytosol, mitochondria, plastids, and peroxisomes in plants . Předpokládá se, že cyklus glutathion-askorbát hraje klíčovou roli pro detoxikaci H2O2 kvůli vysokým koncentracím glutathionu, askorbátu a NADPH v rostlinných buňkách. Jiné enzymy, jako askorbátu a glutathionu peroxidases, které používají thioredoxins nebo glutaredoxins jako snížení substráty, také brát role v odstranění H2O2 v rostlinách (Obrázek 2).
Vitamin C také tvoří semidehydroascorbyl radikální, relativně dlouho-žil radikální, v regeneraci vitaminu E z jeho radikální formě, stejně jako v úklidu radikály. Rostlinné a živočišné buňky obsahují NADH-dependentní semidehydroascorbate reduktázy enzym (EC 1.6.5.4), snížení radikální zpět na vitamin C pomocí NADH jako zdroj redukčního činidla (Obrázek 2). Enzymaticky i neenzymaticky se může nevratně rozkládat na kyselinu diketoglukonovou nebo může být přeměněna na askorbát v reakci závislé na glutathionu .
jako redukční látka a donor elektronů, během úklidu volných radikálů, vitamín C daruje vysokoenergetické elektrony k neutralizaci volných radikálů a oxiduje se na kyselinu dehydroaskorbovou. Kyselina dehydroaskorbová může být přeměněna zpět na kyselinu askorbovou pro opětovné použití nebo může být metabolizována, což dále uvolňuje více elektronů. I když vitamin C je absorbován ze střeva přes sodík-dependentní vitamin C transporter, většina buněk, transport vitamínu C v oxidované formě (dehydroaskorbové) přes glukózový transportér 1. Dehydroaskorbové je snížena na vytvoření askorbové kyseliny uvnitř buňky, chrání mitochondrie před volnými radikály indukované oxidačním poškozením (obrázky 2 a 3). Vysoce reaktivní volné radikály (např. RO–, RO2–, OH–,, NO2) jsou sníženy o askorbátu, a nově vytvořené askorbyl radikál je málo reaktivní. Askorbát může také uklízet neradikální reaktivní druhy, odvozené od peroxynitritu, jako je kyselina chlorná, ozon a nitrační činidla. Vitamin C je katalyzátor oxidace-redukce monosacharidů (redox), který se nachází jak u zvířat, tak u rostlin. Antioxidační účinek vitaminu C je způsoben jeho schopností darovat elektrony z druhého i třetího uhlíku. Během evoluce primátů, jeden z enzymů, které jsou potřebné, aby se kyselina askorbová byla ztracena tím, mutace, lidé musí získat ze stravy, většina zvířat mohou syntetizovat tento vitamín v těle a nevyžadují to v jejich stravě . Vitamin C je potřebný při přeměně prokolagenu na kolagen oxidací zbytků prolinu na hydroxyprolin. V jiných buňkách se udržuje ve své redukované formě reakcí s glutathionem . Jak je znázorněno na obrázcích 2 a 3, kyselina askorbová je redoxní katalyzátor, který může redukovat a tím neutralizovat ROS, jako je peroxid vodíku (H2O2) (obrázky 2 a 3).
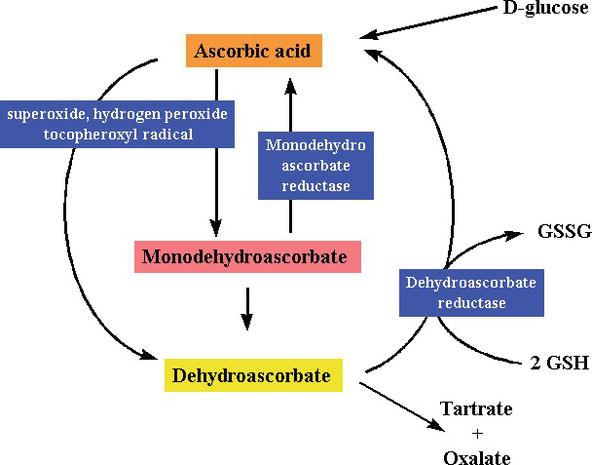
Figure 3.
xmlns:mml=“http://www.w3.org/1998/Math/MathML“ xmlns:xlink=“http://www.w3.org/1999/xlink“ xmlns:xsi=“http://www.w3.org/2001/XMLSchema-instanceSynthesis and degradation ofl-ascorbic acid in plant tissues .
Ascorbic acid has direct antioxidant effects, and also it is a substrate for the redox enzyme ascorbate peroxidase, that is particularly important in stress resistance in plants. Kyselina askorbová je přítomna na vysokých úrovních ve všech částech rostlin, zejména v chloroplastech, které tam dosahují koncentrace 20 mM . Dehydroascorbate (DHA) a volný radikál askorbátu (AFR), jako meziprodukt, volný radikál askorbátu (AFR), které jsou reverzibilní, jedno-elektronové oxidace jsou generovány z askorbátu (Obrázek 4). Podle obecně se předpokládá, že model enzymatické odstraňování ROS, SOD katalyzuje superoxid anion na H2O2 a kyslík; pak H2O2 je snížena na vodu a molekulární kyslík KAT. CAT turnover number is very high, but its affinity for H2O2 is relatively low, and consequently a certain amount of H2O2 remains in the cell.
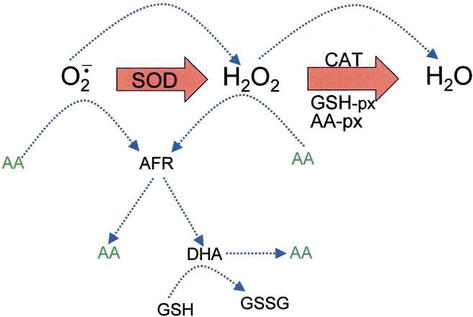
Figure 4.
xmlns:mml=“http://www.w3.org/1998/Math/MathML“ xmlns:xlink=“http://www.w3.org/1999/xlink“ xmlns:xsi=“http://www.w3.org/2001/XMLSchema-instanceThe role of AA in the detoxification of ROS. Blue dotted lines indicate nonenzymatic reactions.
H2O2 can react with superoxide anion formed in oxidative metabolism generating the highly reactive hydroxyl radical. GSH peroxidases (GSH-px) and AA peroxidases (AA-px) are capable of scavenging H2O2 due to their high affinity for H2O2. The cooperativity of SOD, CAT, and peroxidases ensures low amounts of superoxide anion and H2O2 and limiting the risk of hydroxyl radical formation (Figure 5).

Figure 5.
xmlns:mml=“http://www.w3.org/1998/Math/MathML“ xmlns:xlink=“http://www.w3.org/1999/xlink“ xmlns:xsi=“http://www.w3.org/2001/XMLSchema-instanceFoyer-Halliwell-Asada cycle .