Et specielt sukker: hvordan sialinsyre påvirker stofskifte, sundhed og sygdom
Vi vrimler af mikrober, der lever på overflader uden for og inde i vores kroppe. Vores forståelse af især tarmmikrobiomet forbedres hurtigt, da vi begynder at fjerne, hvordan komplekse mikrobielle samfund interagerer med vores kost, med andre mikrober og med vores celleoverflader. Mens mange kemikalier er vigtige i dette miljø, fokuserer vi her på sialinsyrer som et kritisk sæt molekyler, der understøtter mange af disse interaktioner og påvirker metabolisme, sundhed og sygdom.
den mest almindelige sialinsyre, N-acetyl-neuraminsyre (Neu5Ac) (Fig. 1) er en relativt simpel sukkersyre, der bortset fra dens ladning ikke har noget iboende usædvanligt ved det. Men når celler kontakter andre celler, bruger de ofte molekyler, der vises på overfladen, og det er her sialinsyrer bliver så vigtige, da de normalt er de terminale sukkerarter på værtsglykanerne, at peberproteiner og lipider sidder på celleoverflader. Celleoverflade eller udskilt mucinglycoproteiner er gode eksempler på sialinsyrebelagte strukturer, som mikrober kan støde på slimhindeoverflader, såsom luftvejene eller mave-tarmkanalen (GI). Denne unikke position som ‘meet and greet’-molekylet for andre humane celler, bakterieceller og vira sætter sialinsyrerne i centrum for mange vigtige processer.
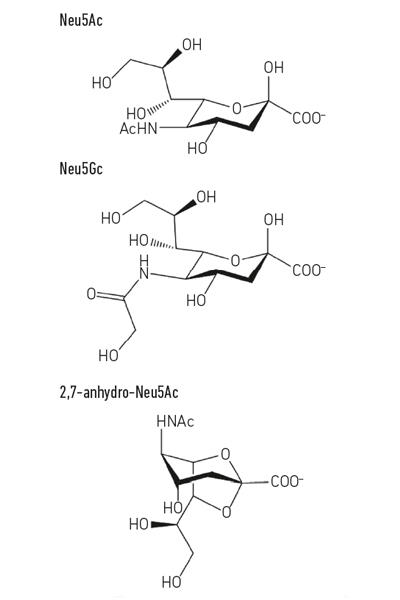
- Fig. 1. Eksempel på sialinsyrederivater. Bemærk, at N-glycolyl-neurnaminsyre (Neu5Gc) ikke kan fremstilles af mennesker, en biokemisk forskel, der adskiller os fra andre store aber, men kan inkorporeres i vores celleoverflader, når de erhverves fra kosten.
- Sukkerovertrukne patogener
- Krydsfodring-deling af slik omkring
- Fig. 2. Tegneserieillustration af de forskellige interaktioner mellem bakterier og sialinsyrer, der findes som terminale sukkerarter på en række værtsglykaner. Disse spaltes af sialidaser og omdannes normalt til fri Neu5Ac med undtagelse af IT-sialidasen, der frigiver 2,7-anhydro-Neu5Ac. Fri sialinsyre frigivet af vært eller patogene sialidaser kan derefter bruges af patogener som en usynlighedskappe (a) eller til fodring (b). Krydsfodring kan forekomme mellem medlemmer af tarmmikrobiota eller mellem kommensale og patogene bakterier, der deler den samme niche (c, d), mens andre bakterier har udviklet egoistiske mekanismer til at reservere sialinsyre til eget forbrug (e).
- holde fat i dine egne slik
- vira kommer ind på act
- yderligere læsning
- Andreas Bell
- Emmanuele Severi
- Nathalie Juge
- Gavin H. Thomas
- hvorfor betyder mikrobiologi noget?
- hvilket råd vil du give til nogen, der starter på dette felt?
Fig. 1. Eksempel på sialinsyrederivater. Bemærk, at N-glycolyl-neurnaminsyre (Neu5Gc) ikke kan fremstilles af mennesker, en biokemisk forskel, der adskiller os fra andre store aber, men kan inkorporeres i vores celleoverflader, når de erhverves fra kosten.
Sukkerovertrukne patogener
en af de første mikrobielle funktioner af sialinsyrer var forbundet med nogle patogeners evne til at kolonisere og derefter forårsage sygdom hos mennesker. Faktisk var den tidligere præsident for Microbiology Society, Professor Harry Smith FRS, der arbejdede ved University of Birmingham, banebrydende for dette arbejde med Neisseria gonorrhoea. Da forskere i hans gruppe isolerede bugten direkte fra kroppen, var den resistent over for drab med humant serum (komplementmedieret drab), men hvis bugs blev dyrket i laboratoriet i et par generationer, gik denne beskyttelse tabt, og cellerne blev dræbt af serumet. Hans gruppe havde opdaget, at disse patogener stjæler sialinsyre fra værten og bruger den til at belægge deres egen celleoverflade for at humanisere dem. Da de imidlertid kun kan fjerne denne sialinsyre, betyder dens fravær i vækstmedier, at der ikke tilsættes yderligere sialinsyre, så de hurtigt mister denne ‘serumbeskyttelse’ og dræbes. Det viser sig, at en række andre luskede bugs bruger lignende strategier til at generere deres egen usynlighedskappe ved hjælp af sialinsyre, såsom Neisseria meningitidis, Campylobacter jejuni eller Haemophilus influensae (Fig. 2a)
Krydsfodring-deling af slik omkring
ud over at blive brugt af patogener som en usynlighedskappe, er sialinsyrer ret god mad til bakterier, da de giver både kulstof og nitrogen og kan bruges som energikilde. Tidligere arbejde viste, at patogener som Vibrio cholerae var glade for bare at spise sialinsyrer, og det var i sig selv vigtigt for en vellykket værtskolonisering (Fig. 2b).
i tarmen kommer en vigtig kilde til sialinsyrer fra muciner, som er de vigtigste strukturelle komponenter i slimlaget, der dækker epiteloverfladen. Det mest udsatte lag af slim er levestedet for forskellige kommensale bakterier, som har lært at feste på mucinproteiner, hvor sukkerarter udgør 80% af deres masse. Fra et simpelt topologisk perspektiv høstes sialinsyrerne, som de terminale sukkerarter, først og udsætter de underliggende sukkerarter, der også efterfølgende kan frigives og spises. Med fremkomsten af næste generations sekventering har vi fået viden om mikroberne, der lever i denne niche, og mange har gener til optagelse af sialinsyre og efterfølgende katabolisme. Det, der var spændende, var opdagelsen af, at nogle af de kommensale anaerober, som Bacteroides thetaiotaomicron, udskiller sialidaser for at frigive sialinsyren, men mangler transportører og kataboliske gener til faktisk at bruge den. Denne tilsyneladende altruistiske gestus er nødvendig for, at bakterierne får adgang til underliggende sukkerarter og understøtter en proces med metabolisk krydsfodring til andre bugs, der lever i slim niche, som commensal Escherichia coli stammer, der ikke har en sialidase, men er gode til at spise fri sialinsyre (Fig. 2c). Dette koncept anerkendes nu som et vigtigt aspekt af kolonisering og nichetilpasning. En strålende eksemplificering af dette blev beskrevet af gruppen Justin Sonnenburg fra Stanford University ved hjælp af en musemodel med en simpel defineret tarmmikrobiota. Efter antibiotikabehandling blev mange af de sialinsyre-spisende bakterier udslettet, hvilket resulterede i akkumulering af fri sialinsyre i tarmen. Når de derefter udfordres med patogener som Salmonella typhimurium eller Clostridium difficile, ville disse patogener drage fordel af den frie sialinsyre som næringsstof (Fig. 2d). Mutante stammer af patogener, der mangler transportører eller kataboliske gener, havde ikke en fordel, hvilket skabte en direkte forbindelse til patogenudvækst, når tarmens mikrobielle samfund forstyrres. Mekanismer til at reducere puljen af fri sialinsyre i tarmen blev derfor foreslået som en del af en ny antiinfektionsstrategi.
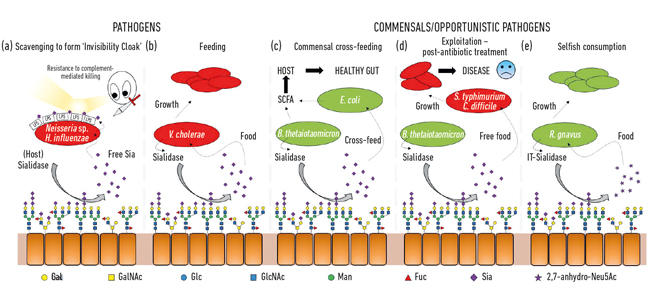
Fig. 2. Tegneserieillustration af de forskellige interaktioner mellem bakterier og sialinsyrer, der findes som terminale sukkerarter på en række værtsglykaner. Disse spaltes af sialidaser og omdannes normalt til fri Neu5Ac med undtagelse af IT-sialidasen, der frigiver 2,7-anhydro-Neu5Ac. Fri sialinsyre frigivet af vært eller patogene sialidaser kan derefter bruges af patogener som en usynlighedskappe (a) eller til fodring (b). Krydsfodring kan forekomme mellem medlemmer af tarmmikrobiota eller mellem kommensale og patogene bakterier, der deler den samme niche (c, d), mens andre bakterier har udviklet egoistiske mekanismer til at reservere sialinsyre til eget forbrug (e).
holde fat i dine egne slik
mens meget tidlig sialomikrobiologi fokuserede på patogener, har nyere arbejde fokuseret på de kommensale bakterier, der befinder sig i samme niche. Dagens undersøgelser inden for tarmmikrobiota afslører, hvor hård konkurrencen om Neu5Ac er i vores tarm, og hvordan den kan tippe balancen mellem patogener og kommensaler. Hvad hvis en bestemt bakterie kunne frigive sialinsyre i en form, som kun den kunne få adgang til? Arbejdet i Juge-gruppen viste, at tarmsymbiont Ruminococcus gnavus har udviklet sig til at gøre det ved hjælp af en speciel type sialidase kaldet en intramolekylær trans-sialidase (IT-sialidase), der frigiver 2,7-anhydro-Neu5Ac (se Fig. 1) i stedet for Neu5Ac. Ved at udvikle en metode til syntese af ren 2,7-anhydro-Neu5Ac viste de, at R. gnavus-stammer var i stand til at vokse på 2,7-anhydro-Neu5Ac som den eneste kulstofkilde. I modsætning til det faktum, at det er muligt, er det en af de vigtigste faktorer, der gør det muligt at bestemme, om det er nødvendigt at behandle det. In vivo, dette kan favorisere en mekanisme, der hjælper med at målrette bakterierne mod sialinsyrerige regioner i mave-tarmkanalen, derfor fremme bakteriel kolonisering i slimlaget. Når den er placeret på det rigtige sted, spalter IT-sialidasen sialinsyre fra de terminale kæder af muciner og frigiver den i en form, 2,7-anhydro-Neu5Ac, at R. gnavus kan bruge som sin egen fødekilde, snarere end at dele Neu5Ac med andre bakterier, der befinder sig i slim niche, herunder patogener (Fig. 2e). Denne mekanisme giver en konkurrencemæssig fordel i forhold til andre sialinsyre-spisende bakterier, der befinder sig i slimnichen, ved at tilvejebringe en kilde til næringsstof, som den fortrinsvis kan få adgang til. Derudover kan R. gnavus også hjælpe med at reducere udvækst af enteriske patogener ved at reducere niveauet af Neu5Ac i slimhindemiljøet og åbne måder til en ny terapeutisk strategi i en tidsalder med stigende antibiotikaresistens.
vira kommer ind på act
vira bruger også sialinsyrer som nøglemolekyler under deres infektionscyklus, mest berømte virus. Indledende vedhæftning er det første nøgletrin, da sialinsyrer fungerer som receptorer for virussen på respiratoriske epitelceller. Typen af binding af sialinsyren til underliggende sukkerarter i glycanerne styrer ofte værtsområdet for virus, og pandemistammer har ofte adhæsionsprotein (hæmagglutinin), der genkender de menneskelignende former for sialinsyrebinding og er derfor særlig virulente. Sialinsyre er vigtig i det sidste trin i den virale livscyklus, da frigivelse fra den inficerede celle kræver spaltning af sialinsyrer fra værtscelleoverfladen. Dette er katalyseret af et virus kaldet sialidase (eller neuraminidase). Dette er en af de mest almindelige metoder til behandling af denne sygdom, og det er en af de mest effektive metoder til behandling af denne sygdom.
afslutningsvis er det klart, at sialinsyrer er kritiske molekyler i mange processer, hvor mikrobielle celler og vira interagerer med pattedyrs celleoverflader. I denne korte artikel har vi berørt nogle af disse for at give en ide om de centrale funktioner i disse sukkerarter i kommunikation, stealth, kolonisering og metabolisme i forskellige aspekter af hede og sygdom. Sialinsyrer er blevet beskrevet som de vigtigste kemikalier i verden og vil uden tvivl fortsætte med at afsløre mere om udviklingen af mennesker og deres samspil med deres mikrober.
yderligere læsning
Thomas, GH. Sialinsyre erhvervelse i bakterier-et substrat, mange transportører. Biochem Soc Trans 2016; 44: 760-765.Ng KM, Ferreyra JA, Higginbottom SK, Lynch JB, Kashyap PC et al. Mikrobiota-frigjorte værtssukker Letter post-antibiotisk ekspansion af enteriske patogener. Natur 2013; 502: 96-99.det er et af de mest populære områder i verden. Unravelling specificitet og mekanisme af sialinsyre anerkendelse af tarmen symbiont Ruminococcus gnavus. Nat Commun 2017; 8: 2196.opdagelsen af intramolekylære trans-sialidaser i human tarmmikrobiota antyder nye mekanismer til slimhindetilpasning. Nat Commun 2015; 6: 7624.
Juge N, Tailford L, cd. Sialidaser fra tarmbakterier: en mini-anmeldelse. Biochem Soc Trans 2016; 44: 166-175.

Andreas Bell
Kvadram Institute Bioscience, NR4 7UK, UK
Andreas Bell er en postgraduate studerende i afdelingen Gut mikrober og sundhed ved Kvadram Institute studerer virkningen af en ny mekanisme af sialinsyre metabolisme på gut homeostase. Han opnåede sin BSc i biokemi fra University of East Anglia og tilbragte 2 år på John Innes Center for chlorophyll metabolisme i pea (Pisum sativum), før han kom til Nathalie Juge ‘ s gruppe på Kvadram Institute i 2015 for sit ph.d. – arbejde.

Emmanuele Severi
Institut for biologi, University of York, Gikværd måde, York YO10 5DD, UK
@emm_severi
Emmanuele Severi er en postdoktoral forskningsassistent i Biologisk Institut ved University of York, der arbejder i laboratoriet for Prof Gavin Thomas. Han har arbejdet med sialinsyretransport og metabolisme på forskellige tidspunkter i sin karriere og har været medlem af samfundet siden 2002.

Nathalie Juge
Institut for Bioscience, Norv Research Park, NR4 7UK, UK
Nathalie Juge er forskningsleder ved instituttets Bioscience (chib) i Norv, viceleder for instituttets strategiske program, Gut Microbes and Health (GMH) og æresprofessor ved Institut for Biologiske Videnskaber, University of East Anglia. Hun leder en forskningsgruppe om glycobiologi af vært-mikrobe interaktioner i tarmen med fokus på mucin-afledt sialinsyre metabolisme af tarmmikrobiota (https://quadram.ac.uk/nathalie-juge).

Gavin H. Thomas
Institut for biologi, University of York, Gikværd måde, York YO10 5DD, UK
@GavinHThomas
Gavin H. Thomas er professor i mikrobiologi i Biologisk Institut ved University of York og har arbejdet med bakteriel sialinsyretransport og katabolisme for over et årti. Han har været medlem af samfundet siden 1995, var redaktør for mikrobiologi i dag (2003-2006), tjente i Rådet i samme periode, tjente i Kommunikationsudvalget (2012-2015) og ligestillingen & Mangfoldighedsudvalg (2013-2015). Han har været redaktør, seniorredaktør og er nu stedfortrædende chefredaktør for samfundets førende tidsskrift Microbiology (http://thomaslabyork.weebly.com).
hvorfor betyder mikrobiologi noget?
Gavin: Det betyder noget for vores helbred – først nu begynder vi virkelig at forstå den molekylære sammensætning og funktion af vores mikrobiom, som sandsynligvis påvirker vores krop på mangfoldige måder.
hvilket råd vil du give til nogen, der starter på dette felt?
Gavin: Læs bredt og ud over ‘din bug’ – mikrober kan gøre stort set alt og har normalt opfundet flere forskellige måder at gøre det på!
billeder: H3N2-viruspartikler. CDC / Science Photo Library.
Fig. 1. – Andrey Bell.
Fig. 2. Emmanuele Severi.