kardiologi
- ventrikulære septumdefekter
- anatomi
- Patofysiologi
- kliniske præsentationer
- gør diagnosen
- Natural History
- Management
- Patent Ductus Arteriosus Anatomy
- anatomi
- Patofysiologi
- kliniske præsentationer
- stille diagnosen
- naturhistorie og ledelse
- Atrieseptumdefekter (ASDs)
- anatomi
- Patofysiologi
- klinisk præsentation
- stille diagnosen
- Ledelse
- atrioventrikulær defekt (AVSD)
- anatomi
- Patofysiologi
- kliniske præsentationer
- diagnose
- behandling
ventrikulære septumdefekter
isolerede ventrikulære septumdefekter (VSDs) udgør 25-30% af alle medfødte hjertesygdomme (CHD) hos børn. VSD kan være til stede i 50% af CHD ‘ er, såsom i tetralogi af Fallot, dobbelt udløb højre ventrikel, truncus arteriosus og andre.
anatomi
cirka 70% af alle VSD ‘ er er til stede i den membranøse del af det inter-ventrikulære septum, omkring 20% er i den muskulære del, og de resterende defekter er ved enten indløbs-eller udløbsdelene af det ventrikulære septum. Indløbs-VSD er normalt en del af atrioventrikulær septal (AV-kanal) defekt. 20%) i den orientalske befolkning (eller østasiatiske befolkning).
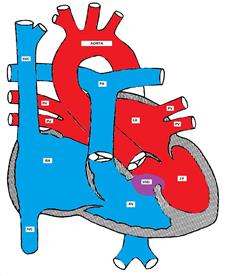
figur, der viser en ventrikulær septumdefekt
Patofysiologi
med en lille størrelse VSD, “restriktiv VSD,” retningen og størrelsen af shunten afhænger på størrelsen af VSD og trykgradienten mellem venstre og højre ventrikler. Den restriktive karakter af VSD opretholder trykgradienten mellem de to ventrikler.
med en stor VSD er hullet ikke restriktivt, og trykket i begge ventrikler er næsten ens. Shuntens retning og størrelse afhænger af den relative forskel mellem de pulmonale og de systemiske vaskulære modstande. I fostrets liv er lungemodstanden højere end den systemiske resistens. Når lungerne ekspanderer med det første åndedrag, falder lungemodstanden markant, og lungestrømmen øges. Lungemodstanden fortsætter med at falde, indtil den når det normale voksenforhold på 1:10 med 4-8 uger (se figur).
langvarig stor venstre-til-højre shunt fører til gradvis stigning i lungetrykket, og pulmonal hypertension udvikler sig til sidst. Da trykforskellen mellem de systemiske og lungesystemer falder, falder strømmen over shunten også. Hvis den pulmonale vaskulære modstand overstiger den systemiske vaskulære modstand, vender shuntens retning og cyanose udvikler sig (Eisenmenger syndrom). Dette kan udvikle sig inden for to år hos ellers sunde børn og inden for et år hos patienter med nedsat syndrom.
kliniske præsentationer
børn med en lille VSD er normalt asymptomatiske. En tilfældigt opdaget holosystolisk eller decrescendo hjertemusling er den mest almindelige præsentation. Mumlen opdages almindeligvis ved 2-4 ugers alderen, da den pulmonale vaskulære modstand falder, og trykforskellen mellem de to ventrikler bliver bemærkelsesværdig (figur). Intensiteten af murmuren er omvendt proportional med størrelsen af VSD på grund af den øgede turbulens og strømningshastighed produceret af en mindre defekt. En spænding kan være håndgribelig i nogle tilfælde. Defekten kan være lille nok til næsten at lukke i slutningen af en systolisk decrescendo-murmur.
et spædbarn med en stor VSD kan være asymptomatisk i de første par dage / uger af livet, indtil den pulmonale vaskulære modstand falder. Når lungemodstanden falder, øges venstre mod højre shunt. Den højre ventrikel udsættes således for højt tryk og bliver hypertrofieret, mens venstre atrium og venstre ventrikel får mere volumen og bliver udvidet. Det højre atrium påvirkes normalt ikke. Kongestiv hjertesvigt (CHF) kan udvikle sig og præsenterer som takykardi, takypnø, anstrengende dyspnø, åndenød og sved under fodring. Barnets vækst er også ofte forsinket på grund af dårlig kaloriindtagelse. Hos nogle spædbørn, især dem med dun ‘ s syndrom, kan den pulmonale vaskulære modstand ikke falde signifikant. Disse spædbørn udvikler muligvis ikke CHF, men har øget risiko for at udvikle pulmonal hypertension. De kan have brug for tidligere kirurgisk indgreb for at forhindre forværring af pulmonal hypertension og den tidlige udvikling af Eisenmenger syndrom.
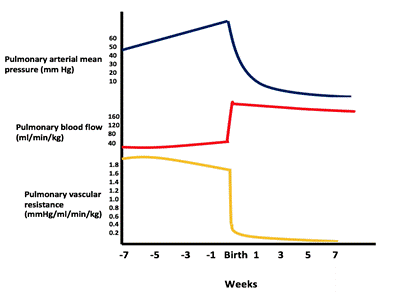
figur, der viser faldet i pulmonalt vaskulært tryk/modstand og stigningen i pulmonal blodgennemstrømning efter fødslen
gør diagnosen
- en holosystolisk murmur høres ved venstre brystgrænse på grund af turbulens over VSD. Intensiteten af mumlen er omvendt proportional med størrelsen af shunten; jo mindre shunten er, desto højere er Mumlen og omvendt.
- en decrescendo (tidlig) systolisk murmur kan indikere en lille og afsluttende VSD. Der er nedsat strømning i den sidste del af systole, og der høres ingen mumling.
- en apikal mid-diastolisk murmur (rumble) kan høres på grund af øget strømning over mitralventilen (relativ mitralstenose). Dette indikerer, at VSD er stor nok til at forårsage overdreven pulmonal blodgennemstrømning, og dette indikerer klinisk kongestiv hjertesvigt (CHF). Denne CHF skyldes ikke pumpedysfunktion som hos voksne, men på grund af den øgede pulmonale blodgennemstrømning.
- en tidlig diastolisk murmur hørt ved den øverste venstre brystkant i en siddeposition kunne høres i en lille membranøs eller en supra-cristal VSD. Dette indikerer aortainsufficiens på grund af prolaps af en af aortaklappen i VSD sekundært til sugningen skabt af højhastighedsstrålen (Venturi-effekt).
- en høj P2 med smal opdeling af S2 indikerer øget pulmonalt vaskulært tryk og modstand, som ville forårsage tidlig lukning af lungeventilen.
- en tidlig diastolisk murmur på grund af lungesufficiens kan høres, hvis pulmonal hypertension udvikler sig.
- pulmonal hypertension mindsker lungeblodstrømmen og gør CHF usandsynlig (bryllupsrejse før udviklingen af Eisenmenger syndrom).
- kardiomegali og hepatomegali kan være til stede, hvis CHF er til stede.røntgenbilleder af brystet kan vise kardiomegali og øget lungevaskularitet.
- EKG afspejler den hæmodynamiske status og kan vise RVH, forstørrelse af venstre atrium og forstørrelse af venstre ventrikel (EKG er ikke særlig følsom ved differentiering af LVH fra LV-udvidelse). Det højre atrium er normalt upåvirket.
- ekkokardiogram viser placeringen, typen og størrelsen af VSD. Det kan også estimere trykgradienten over VSD. De hæmodynamiske virkninger af VSD på forskellige kamre kan belyses. Det er også vigtigt at kigge efter aortainsufficiens (især i membranøs og supra-cristal VSD), hvilket kan indikere en tidlig skade på aortaklappen.
- hjertekateterisering er sjældent nødvendig, men kan måle lungetrykket / modstanden og hjælpe med at bestemme reaktiviteten (og dermed funktionsevnen) af lungevaskulaturen i tilfælde af pulmonal hypertension.
Natural History
mens mere end halvdelen af små og mellemstore VSD ‘er lukker spontant, lukker kun omkring 10% af store VSD’ er spontant. Den muskulære VSD lukker ved muskelvækst. Den membranøse VSD lukker ved det nærliggende tricuspidventilfoldevæv, der danner en aneurisme, der gradvist bliver endoteliseret. Både indløb og supra-cristal (udløb) VSD ‘ er lukker sandsynligvis ikke spontant. Hos ikke-opererede patienter med stor VSD kan Eisenmenger syndrom udvikle sig inden for to år, men kan udvikle sig så tidligt som et år hos patienter med nedsat syndrom. Dette kan tilskrives den øgede vaskulære / alveolære tæthed og øget sekretion af endostatin hos patienter med nedsat syndrom.
Management
asymptomatiske børn med en lille eller mellemstor VSD behøver kun støttende pleje med forventning om, at VSD vil lukke i de første par år af livet. Hvis CHF udvikler sig, består behandlingen af diuretika, efterbelastningsreducerende midler som ACE-hæmmere og muligvis digoksin. Hjertesvigt i venstre mod højre shunts skyldes volumenoverbelastning til lungecirkulationen. Dette er i modsætning til voksne med myokardieinfarkt, hvor hjertesvigt skyldes pumpedysfunktion. Hos voksne med hjertesvigt bruges digoksin til at forbedre pumpefunktionen. Men hvis digoksin anvendes til behandling af CHF på grund af venstre-til-højre shunt, virker det primært for sin kolinerge virkning for at nedsætte hjertefrekvensen. Væskebegrænsning bør undgås, da det reducerer kalorieindtaget og forsinker væksten.
iltbehandling bør også undgås, da det er en pulmonal vasodilator og en systemisk vasokonstriktor. Det ville forværre venstre-til-højre shunt og CHF symptomer. Patienter med vedvarende CHF eller dem, der udvikler pulmonal hypertension, kræver kirurgisk lukning af VSD. Hvis en patient ikke er en egnet kandidat til operation, bør lungearteriebånd overvejes, indtil kirurgi kan udføres (normalt inden for det første leveår). For nylig er trans-kateterteknikker blevet brugt til at lukke VSD ‘er (især de muskulære VSD’ er).
Patent Ductus Arteriosus Anatomy
anatomi
ductus arteriosus, dannet fra den embryonale 6.aortabue, forbinder aorta med lungearterien. Det lukker normalt inden for få dage efter fødslen. En høj iltspænding og et fald i endogene prostaglandiner er vigtige faktorer for at inducere duktal lukning. Af samme grund er prostaglandinsyntetasehæmmere, såsom indomethacin, effektive til at inducere duktal lukning og bruges ofte i den nyfødte periode, især hos premature spædbørn.
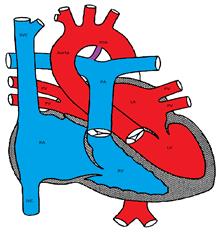
figur, der viser en Patent Ductus Arteriosus
Patofysiologi
svigt i lukning af ductus arteriosus fører til hæmodynamiske ændringer svarende til dem, der ses i VSD. Retningen og omfanget af shunten i PDA ‘en afhænger af størrelsen af PDA’ en og de relative systemiske og pulmonale vaskulære modstande.
kliniske præsentationer
PDA er mere almindelig hos kvinder, premature spædbørn, patienter med nedsat syndrom og medfødt rubella syndrom. Symptomerne ligner dem, der findes i VSD og afhænger af størrelsen på shunten og strømningsretningen. Mens en lille PDA normalt er asymptomatisk, kan en stor PDA med signifikant venstre mod højre shunt føre til CHF og til sidst pulmonal hypertension.
stille diagnosen
- hos ældre børn producerer PDA Klassisk en kontinuerlig eller “maskineri” – murmur på grund af strømning over shunten gennem hjertecyklussen. Hos nyfødte spædbørn, især dem, der er født for tidligt, kan mumlen kun høres under systole, fordi det højere pulmonale arterielle tryk mindsker strømmen under diastol.
- en apikal mid-diastolisk murmur kan høres på grund af øget strømning gennem mitralventilen (relativ mitralstenose). Dette betyder normalt en stor PDA og er ofte forbundet med CHF.
- bredt pulstryk indikerer en stor venstre-til-højre shunt på grund af et pludseligt fald i diastolisk tryk.
- i en lille PDA er EKG normalt normalt. I en stor PDA vil EKG demonstrere højre ventrikulær hypertrofi, venstre ventrikulær og venstre atriel forstørrelse på grund af volumenoverbelastning.
- røntgenbilleder af brystet kan vise øget lungevaskularitet og kardiomegali på grund af forstørrelse af venstre atrium og venstre ventrikel. Hjertestørrelsen kan være normal, hvis shunten er lille.
naturhistorie og ledelse
lille og moderat størrelse PDA lukker ofte spontant, især hos fuldbårne spædbørn. PDA hos premature spædbørn kan have brug for indomethacinbehandling (i de første 2-4 uger af livet) eller kirurgisk ligering. Transcatheter enhed lukning af PDA er almindeligt anvendt i ældre børn.
Atrieseptumdefekter (ASDs)
anatomi
atrieseptumdefekter involverer mange forskellige dele af atrieseptum. Septum secundum defekt er den mest almindelige og udgør 6-10% af alle CHD. Det er placeret i fossa ovalis, i placeringen af foramen ovale. Primum septal defekt betragtes som en delvis form for atrioventrikulær septal defekt. De andre “mindre almindelige” typer af ASD ‘ er er sinus venosus og un-tagdækning af koronar sinus.
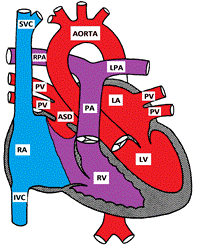
figur, der viser en secundum Atrial Septal defekt
Patofysiologi
da trykforskellen mellem de to atria er lille, genereres der ingen turbulens ved hjælp af en flyde over ASD. I moderate til store ASD ‘ er afhænger retningen og størrelsen af shunten over ASD af den relative højre og venstre ventrikulære overholdelse. I den tidlige barndom er den højre ventrikulære overholdelse lav, og shunten over ASD er lille. Når den højre ventrikulære overholdelse øges, øges venstre-til-højre shunt. Hvis den højre ventrikulære overholdelse falder, falder shunten senere i livet. Shunten kan til sidst vende, hvis patienten udvikler pulmonal hypertension og Eisenmenger syndrom. Dette tager normalt et par årtier at udvikle sig.
klinisk præsentation
ASD er normalt asymptomatisk og præsenterer typisk med et hjertemusling i førskolealderen. CHF udvikler sjældent hos patienter med en stor ASD. Højre atrial strækning kan forårsage atrielle arytmier. Langvarig volumenoverbelastning af lungerne forårsager til sidst pulmonal hypertension, hvilket kan tage 4 til 5 årtier at udvikle sig.
stille diagnosen
- en systolisk udstødningsmusling kan høres i lungeområdet på grund af øget strømning over lungeventilen (relativ lungestenose).
- en mid-diastolisk murmur kan høres ved den nederste venstre brystkant på grund af øget strømning over tricuspidventilen. Denne mumling høres sjældent, fordi tricuspidventilens ring er større end lungeventilens ring. En tricuspid ventil murmur indikerer, at patienten er i CHF på grund af en stor venstre-til-højre shunt.
- ingen murmur udvikler sig på grund af strømmen over ASD, da der kun er en minimal trykgradient mellem de to atria, og der genereres ingen turbulens.
- en bred opdeling af S2 skyldes forsinket lukning af P2 sekundært til øget strømning over lungeventilen.
- opdelingen af S2 er “fast” og varierer ikke med respiration. Dette skyldes formindskede virkninger af åndedrætscyklus på det højre ventrikulære volumen. Som inspiration øges den venøse tilbagevenden til højre atrium og hindrer venstre mod højre shunt over ASD. Ved udløb falder den venøse tilbagevenden til højre atrium, og shunten over ASD øges. I begge tilfælde øges mængden af blod i højre ventrikel og forbliver uændret i både inspiration og udløb.
- EKG kan demonstrere forstørrelse af højre atrium, højre ventrikulær ledningsforsinkelse (ufuldstændig højre bundtgrenblok), højre ventrikulær udvidelse og højre akseafvigelse.røntgenbillede af brystet viser øget lungevaskularitet, forstørrelse af højre atrium og højre ventrikel.
Ledelse
de fleste patienter med ASD er asymptomatiske, og ingen specifik medicinsk behandling er nødvendig. Medicinsk ledelse (som i VSD) kan være nødvendig, hvis CHF er til stede. Trans-kateter lukning er den foretrukne metode til lukning af secundum ASDs. Kirurgisk lukning kan være nødvendig hos patienter med en stor secundum ASD, der ikke kan lukkes trans-kateter eller andre typer ASD, da de sandsynligvis ikke lukker spontant.
atrioventrikulær defekt (AVSD)
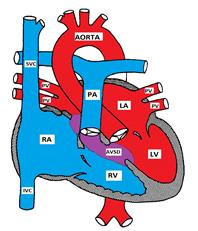
udbredt hos patienter med nedsat syndrom. Fyrre procent af børn med nedsat syndrom har CHD, og 40% af defekterne er former for AVSD
anatomi
atrioventrikulær septumdefekt er også kendt som endokardiel pudedefekt (ECD) og atrioventrikulær kanal (AVC). Den består af en række defekter i de endokardiale puder, der danner den nedre del af atrialseptumet, den øvre del (indløb) af det ventrikulære septum og de mediale dele af AV-ventilerne.
der er 4 mulige typer:
a) delvis AVSD (primum ASD) består af en defekt i den nedre del af atrialseptumet og er normalt forbundet med en kløft i den forreste mitral folder, der forårsager mitral insufficiens. Den ventrikulære septum er normalt intakt.
b) Komplet AVSD har en defekt, der strækker sig fra den nedre del af atrialseptumet til den øvre del (indløb) af ventrikulær septum. Mitral-og tricuspid-ventilerne mister deres ankerpunkter i ventrikulær septum og er i stedet fastgjort til hinanden og danner en fælles AV-ventil, der hænger ud over ventrikulær septum.
c) mellemliggende AVSD svarer til den komplette AVSD, men har 2 AV-ventiler med en primum ASD og en stor indløbs-VSD.
d) Transitional AVSD svarer til den mellemliggende AVSD, men VSD er lille.
Patofysiologi
patofysiologien afhænger af den overvejende læsion (atrial vs ventrikulær). Der er en venstre-til-højre shunt på atrialt niveau på grund af øget relativ højre ventrikulær overholdelse, der fører til forstørrelse af højre atrium. Forstørrelse af venstre atrium opstår på grund af mitral insufficiens sekundært til mitralventilspalten. Der er en varierende grad af pulmonal hypertension, da lungevaskulaturen udsættes for overskydende blodvolumen ved højere tryk. Pulmonal hypertension kan udvikle sig i de første to år hos normale patienter og i det første år hos patienter med nedsat syndrom.
kliniske præsentationer
den kliniske præsentation af AVSD er variabel og afhænger af størrelsen på defekten og graden af venstre mod højre shunt. Patienter med komplet AVSD er normalt til stede med kongestiv hjertesvigt i de første par uger af livet, mens de med delvis AVSD (primum ASD) kan være helt asymptomatiske.
symptomer på CHF inkluderer dårlig fodring, åndenød, diaphorese under fodring og dårlig vægtøgning. Mild cyanose kan sjældent udvikle sig på grund af højre til venstre shunt på grund af øget lungemodstand eller på grund af præferentiel streaming af det venøse blod fra IVC til venstre atrium.
diagnose
- fysiske fund er variable og afhænger af tilstedeværelsen eller fraværet af kongestiv hjertesvigt. Precordium kan være hyperdynamisk, og hjertepunktet kan forskydes ringere og til venstre.
- de auskultatoriske fund er også variable og kan omfatte en systolisk udstødningsmusling på grund af øget strømning gennem lungeventilen med bred og fast opdeling af S2 som i ASD. En høj, enkelt S2 indikerer pulmonal hypertension.
- yderligere auskultatoriske fund inkluderer en mid-diastolisk murmur ved den nederste venstre brystgrænse på grund af øget strømning gennem tricuspidventilen, apikal holosystolisk murmur, der udstråler til venstre aksilla på grund af mitral insufficiens og en holosystolisk murmur af VSD.
- EKG er kendetegnet ved afvigelse fra venstre akse på grund af ringere og posterior forskydning af AV-knuden (anatomisk). Det kan også vise højre ventrikulær hypertrofi (på grund af øget tryk), forstørrelse af højre atrium og LVH. Et forlænget PR-interval (første grads hjerteblok) sandsynligvis på grund af unormal av-knudeledning kan være til stede.
- røntgenbillede af brystet viser forskellige grader af kardiomegali og øget lungevaskularitet.
- ekkokardiografi er nyttig til at demonstrere de anatomiske læsioner og tilhørende abnormiteter. Det er vigtigt at vurdere av-ventilernes integritet.
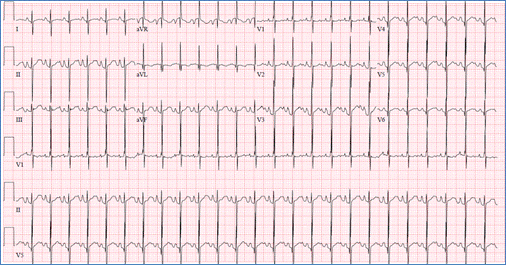
EKG viser overlegen AKSEAFVIGELSE (negativ i avF) og højre ventrikulær
hypertrofi i AVSD
behandling
CHF, hvis til stede, administreres med diuretika, ACE-hæmmere og lejlighedsvis digoksin. En formel med høj kaloritæthed bør anvendes uden væskebegrænsning.
næsten alle patienter med AVSD har brug for operation. Tidspunktet for operationen afhænger af patientens størrelse, tilstedeværelsen af CHF, respons på medicinsk behandling og tilstedeværelsen eller fraværet af pulmonal hypertension. Hos asymptomatiske patienter med delvis AVSD kan kirurgi forsinkes indtil førskolealderen. Korrigerende kirurgi udføres normalt hos symptomatiske patienter med uhåndterlig CHF i de første par måneder af livet. Selv hos patienter, der reagerer på medicinsk behandling, kræver tilstedeværelsen af ned-syndrom tidlig operation for at forhindre udvikling af pulmonal hypertension. Hvis kirurgi ikke kan udføres hos en symptomatisk patient, kan pulmonal arteriel banding hjælpe med at begrænse lungeblodstrømmen, indtil kirurgisk reparation er mulig.