phenanthren
- phenanthren kemiske egenskaber,anvendelser,produktion
- ikke-lineære polycykliske aromatiske carbonhydrider
- molekylær struktur
- kemiske egenskaber
- bruger
- forberedelse
- kemiske egenskaber
- kemiske egenskaber
- fysiske egenskaber
- anvendelser
- anvender
- Definition
- produktionsmetoder
- Syntesereference
- generel beskrivelse
- luft & Vandreaktioner
- Reaktivitetsprofil
- sundhedsfare
- brandfare
- sikkerhedsprofil
- potentiel eksponering
- carcinogenicitet
- kilde
- miljø skæbne
- forsendelse
- oprensningsmetoder
- bortskaffelse af affald
phenanthren kemiske egenskaber,anvendelser,produktion
ikke-lineære polycykliske aromatiske carbonhydrider
phenanthren er den enkleste ikke-lineære polycykliske aromatiske carbonhydrider med tre bensenringstruktur, der er isomeren af anthracen. I 1872 E. Ostermayer et al har identificeret phenanthren i anthracenoliefraktionen i kultjæredestillat, der er et af stenkulstjæreforarbejdningsprodukter. I højtemperaturkulstjære er phenanthrenindholdet sekundært kun til naphthalen, der er omkring 4~6%, hovedsageligt koncentreret i anthracenoliefraktionerne. Den kemiske aktivitet af phenanthren er stærkere end naphthalen, men den er svagere end anthracen, og iltnings-og additionsreaktionerne kan også forekomme i 9 og 10 positioner.
phenanthren er en farveløs krystal med glans, og phenanthren udfældet fra ethanol er en farveløs monoklinisk krystal. Phenanthren er en bladlignende krystal med en relativ densitet på 1.179 (25/4 liter) og et brydningsindeks på 1,6450, smeltepunkt på 101 liter C og kogepunkt på 340 liter C. Det kan underkastes sublimering, idet det er uopløseligt i vand, let opløseligt i ethanol, opløseligt i ether, eddikesyre, chloroform, tetrachlormethan og carbondisulfid. Opløsningen udviser blå fluorescens. 1, 4, 5, 8-positionerne er de samme, kendt som kurposition; 2, 3, 6, 7-positionen er også de samme, kendt som kurposition; 9, 10-positionerne er de samme, kendt som ?-position. Dens kemiske egenskab er mellem naphthalen og anthracen. Det kan også have additionsreaktion i 9, 10-positionen, men ikke så let som anthracen. Iltning forekommer også ved 9, 10-positionen med iltning, der giver phenanthrenekinon. Substitutionsreaktioner kan også forekomme. Det kan også opnås ved adskillelse fra antracenoliefraktionen af kultjæreolie. Phenanthren kan anvendes til fremstilling af pesticider og farvestoffer, men også anvendes som stabilisator af den høje effektivitet & lav toksicitet pesticider og røgfri pulver sprængstoffer.
phenanthren kan bruges til at producere farvestoffer, lægemidler og harpikser efter konverteringsbehandling. 9, 10-dihydro-9-phenathroic acid er et plantevækststimulerende hormon; Perhydrophenanthren fremstillet ved hydrogenering af phenanthren kan anvendes til fremstilling af jetbrændstof; dets sulfonerede produkt, phenanthrensulfonsyre kan anvendes som bindemiddel og garvning.
Den phenanthrenholdige moderlud under produktionen af raffineret anthracen ved anvendelse af opløsningsmiddelmetode efter genvinding af opløsningsmiddel og yderligere krystallisationsfiltrering kan give rå phenanthren indeholdende 40% phenanthren.
den rå phenanthren, efter fjernelse af restopløsningsmidler i smeltekedlen og derefter udbedret i retteringstårnet med 20 teoretiske plader, fraktionerne på 335 til 340 liter C udskæres, efterfulgt af afkøling, krystallisation og filtrering for at opnå den industrielle phenanthren med phenanthrenindholdet på mere end 70%. .
ovenstående oplysninger er udarbejdet af Tongtong fra Chemicalbook.
molekylær struktur
den molekylære struktur af phenanthren og anthracen er ens med hinanden med alle atomer placeret i samme plan, men ikke i samme linje, idet de er et lukket konjugatsystem med aromatisk egenskab. 1, 2, 3, 4, 10 positioner og 5, 6, 7, 8, 9 positioner inde i molekylerne svarer til henholdsvis hinanden, men der var forskelle i aktivitet ved de 5 positioner, blandt hvilke 9 og 10 havde højere aktivitet med substitution, iltning og tilsætning, der forekom i 9 og 10 positioner: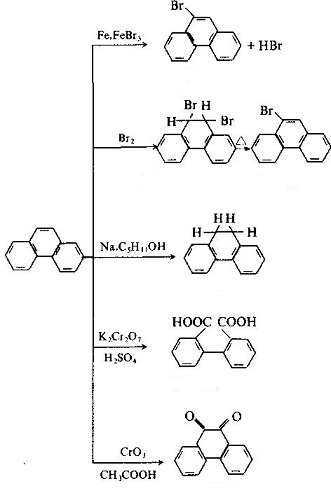
Phenanthrenekinon er et pesticid, der anvendes som bakteriedræbende frøforbinding, der er i stand til at forhindre hvedeskurv, hård smut og sød kartoffel sort plet.
industriel phenanthren er afledt af destillation af anthracenolie afledt af kultjæredestillat. Mange slags naturlige produkter (såsom steroler) indeholder dette ringsystem. Phenanthren anvendes hovedsageligt til fremstilling af farvestoffer, lægemidler, høj effektivitet og lav toksicitet af pesticider og kan bruges som scintillanter, røgfri pulverstabilisator. Mange af phenanthrenderivaterne har kræftfremkaldende fysiologiske virkninger. Såsom: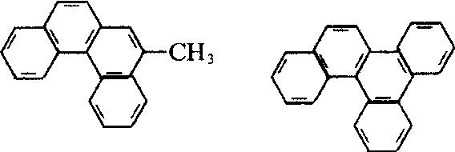
molekylstrukturen af 2-methyl-3, 4-bensophenanthren og 1, 2, 3, 4-dibensophene
kemiske egenskaber
det fremstår som hvid glans og fluorescerende flakekrystaller. Det er ikke opløseligt i vand, let opløseligt i ethanol, opløseligt i ether, eddikesyre, methan, tetrachlormethan og carbondisulfid.
bruger
det kan bruges til fremstilling af phenanthrenekinon, syntetisk harpiks, pesticider og konserveringsmidler og så videre.
phenanthren kan gennem iltning give phenanthrenekinon, der skal bruges til at erstatte de organiske kviksølvpesticider ceresin og gallotoks. Biphenylsyren opnået ved dens iltning kan anvendes til fremstilling af alkydharpiks. Det kan også være forårsaget af en række sygdomme. Chloreringsprodukterne af phenanthren kan bruges til at fremstille ikke-brændbare elektriske isolatorer og imprægneringsmidler. Den sulfonerede phenanthrensulfonsyre kan være lavet af bindemiddel, garvning og så videre. Men faktisk er de fleste af disse applikationer endnu ikke udviklet. I papirindustrien, kan phenanthren anvendes som papirmasse antifogging agent; kan også anvendes til nitroglycerin sprængstoffer og nitrocellulose stabilisator og til fremstilling af røg bombe; den faste ilt af phenanthren kan være fremstillet af fremragende flamme resistente elektriske isoleringsmaterialer og fyldstoffer. I medicin kan phenanthren anvendes til syntetisering af alkaloider-morfin og koffein, dimethylmorphine samt lægemidler med særlige fysiologiske virkninger på mange reproduktive organer. I farvestofindustrien kan phenanthren være lavet af 2-aminophenanthren kinon, bensantron, sulfidreduktionsfarvestof (blå BO, sort BB og brun) og så videre. Derudover kan plastindustrien, syntetiske garvemidler og phenanthren under høj temperatur og højt tryk gennemgå hydrogenering for at få hydrofenanthren, der er brændstof til senior jetfly.
til bestemmelse af molekylvægt og syntese af organiske forbindelser.
forberedelse
phenanthren er et relativt højt indhold af kultjære, der tegner sig for 5% kultjære, kun andet end naphthalenindhold. Antracenolien i fraktionsområdet 300-360 liter af kultjære har det højeste indhold af phenanthren, efterfulgt af anthracen og carbasol og så videre. Phenanthrenekstraktionsmetoden sendes normalt anthracenolie til afkøling, krystallisation og derefter vakuumfiltrering eller centrifugalseparation til olieseparation. Den relativt høje mængde opløselige phenoler i olier kan genvindes ved hjælp af præcisionsdestillationsmetode. Den opnåede krystal kaldes rå anthracen, som indeholder 25-30% anthracen, 22-25% carbasol og 30% phenanthren. Rå anthracen kan udsættes for kraftig ekstraktion, afkøling, filtrering med filtratet dampet ud af opløsningsmiddel før omkrystallisation og filtrering. Tag filtrat til destillation, så vi kan få industriel phenanthren med sulfonering for at få fint phenanthren.
kemiske egenskaber
hvide krystaller
kemiske egenskaber
phenanthren er et hvidt krystallinsk stof. Svag aromatisk lugt. Polycykliske aromatiske carbonhydrider (PAH ‘ ER) er forbindelser, der indeholder flere bencenringe og kaldes også polynukleære aromatiske carbonhydrider.
fysiske egenskaber
farveløse, monokliniske krystaller med en svag, aromatisk lugt
anvendelser
phenanthren er et polycyklisk aromatisk kulbrinte, et miljøforurenende stof.
anvender
mærkede polycykliske aromatiske carbonhydrider som mikroforurenende stoffer.
Definition
ChEBI: Et polycyklisk aromatisk carbonhydrid sammensat af tre smeltede ringe, der tager sit navn fra de to udtryk ‘phenyl’ og ‘anthracen.’
produktionsmetoder
phenanthren forekommer i stenkulstjære og kan isoleres fraflere typer råolie.
Syntesereference
Tidsskrift for heterocyklisk Kemi, 30, s. 291, 1993 DOI: 10.1002/jhet.5570300151
Journal of Organic Chemistry, 18, s. 801, 1953 DOI: 10.1021/jo50013a004
Tetrahedron Letters, 15, s. 495, 1974
generel beskrivelse
farveløse monokliniske krystaller med en svag aromatisk lugt. Opløsninger udviser en blå fluorescens.
luft & Vandreaktioner
uopløseligt i vand.
Reaktivitetsprofil
phenanthren kan reagere med iltningsmaterialer .
sundhedsfare
den akutte orale toksicitet af phenanthren er low.It er mere giftig end anthracen. En oral LD50-værdi hos mus rapporteres ved 700 mg / kg. Det kanforårsage tumor i huden på applikationsstedet.Beviserne for karcinogenicitet hos dyr er imidlertid utilstrækkelige.
brandfare
phenanthren er brændbart.
sikkerhedsprofil
gift intravenøst. Moderat Giftig ved indtagelse. Mutationsdata rapporteret. En human hud fotosensibilisator. Tvivlsom carcinogen med eksperimentelle neoplastigen-og tumorigeniske data ved hudkontakt. Brændbart, når det udsættes for varme eller flamme; kan reagere kraftigt med brandnærende materialer. For at bekæmpe ild skal du bruge vand, skum, CO2, tørkemikalie. Ved opvarmning til nedbrydning udsender den skarp røg og irriterende dampe
potentiel eksponering
støv kan danne eksplosiv blanding med luft. Hvis det er nødvendigt, kan det være nødvendigt at anvende en sådan metode.); kontakt kan forårsage brand eller eksplosioner. Holdes væk fra alkaliske materialer, stærke baser, stærke syrer, oksocider, epoksider.
carcinogenicitet
phenanthren er ineffektivt som initiator. Det kan ikke klassificeres med hensyn til human carcinogenicitet—klasse 3 Efter IARC og klasse D efter IRIS, baseret på ingen humane data og utilstrækkelige data fra en enkelt gavagestudie hos rotter og hudmalings-og injektionsstudier i mus.
kilde
påvist i grundvand under et tidligere kulforgasningsanlæg i Seattle, var ved en koncentration på 130 liter/L (ASTR, 1995). Påvist i 8 dieselbrændstoffer i koncentrationer fra 0,17-110 mg/L med en gennemsnitsværdi på 41,43 mg/L (Vestholm og Li, 1994) og i destillerede vandopløselige fraktioner af ny og brugt motorolie i koncentrationer på henholdsvis 1,9–2,1 og 2,1–2,2 liter (Chen et al., 1994). Lee et al. (1992) rapporterede koncentrationsintervaller på henholdsvis 100 til 300 mg/L og 15 til 25 liter/L i dieselbrændstof og den tilsvarende vandige fase (destilleret vand). Schauer et al. (1999) rapporterede phenanthren i dieselbrændstof i en koncentration på 57 liter/g og i en dieseldrevet Medium-duty lastbiludstødning med en emissionshastighed på 93,1 liter/km.Identificeret i råolier i henholdsvis 26 og 70 ppm (Pancirov og brun, 1975). Dieselolie fra en tankstation i Schlieren indeholdt phenanthren i en anslået koncentration på 327 mg / L (Schluep et al.,2001).
phenanthren blev påvist i asfaltdampe ved en gennemsnitlig koncentration på 57,73 ng/m3., 2001).
Thomas og Delfino (1991) ækvilibreret forureningsfrit grundvand opsamlet fragainesville, FL med individuelle fraktioner af tre individuelle olieprodukter ved 24-25 liter C for24 h. den vandige fase blev analyseret for organiske forbindelser via den amerikanske EPA-godkendte testmetode625. Phenanthren blev kun påvist i den vandopløselige fraktion af dieselbrændstof ved en gennemsnitlig koncentration på 17 liter/L.
baseret på laboratorieanalyse af 7 kultjæreprøver varierede phenanthrenkoncentrationer fra3.100 til 35.000 ppm (EPRI, 1990). Påvist i 1-års alderen kultjærefilm og bulk kultjære ved en anidentisk koncentration på 10.000 mg/kg (Nelson et al., 1996). En højtemperatur stenkulstjæreindeholdt phenanthren i en gennemsnitlig koncentration på 2,66 vægt % (McNeil, 1983). Også identificeret i højtemperaturkulstjærepladser i koncentrationer fra 7.500 til 40.300 mg/kg(Arrendale og Rogers, 1981). Lee et al. (1992a) ækvilibrerede otte kultar med destilleret vand ved25 liter C. Den maksimale koncentration af phenanthren observeret i den vandige fase er 0,4 mg/L.
ni kommercielt tilgængelige creosotprøver indeholdt phenanthren i koncentrationer fra 48.000 til 120.000 mg/kg (Kohler et al., 2000).
typisk koncentration af phenanthren i en tung pyrolyseolie er 2,5 vægt % (Chevron Phillips,maj 2003).
miljø skæbne
biologisk. Catechol er den centrale metabolit i den bakterielle nedbrydning af phenanthren.Mellemprodukter omfatter 1-hydroksy-2-naphthonsyre, 1,2-dihydroksynaphthalen ogsalicylsyre (Chapman, 1972; Hou, 1982). Det blev rapporteret, at Beijerinckia, under aerobicbetingelser, nedbrudt phenanthren til cis-3,4-dihydroksi-3,4-dihydrophenanthracen (Kobayashiand Rittman, 1982).
jord. De rapporterede halveringstider for phenanthren i en Kidman sandy loam og McLaurin sandyloam er henholdsvis 16 og 35 d (Park et al., 1990). Manilal og Aleksander (1991) rapporterede ahalf-life på 11 d i en Kendaia jord.
overfladevand . I en 5 m dyb overfladevandskrop var de beregnede halveringstider for direkte fotokemisk transformation ved 40 liter n breddegrad i midsommeren ved middagstid henholdsvis 59 og 69 d med og uden sediment-vandpartitionering (Sepp og Schlotjauer, 1979).
Fotolytisk. Et kultveilteudbytte på 24,2% blev opnået, når phenanthren adsorberet onsilica-gel blev bestrålet med lys (kur >290 nm) i 17 timer (Freitag et al., 1985). I et 2-ugers eksperiment gav phenanthren på jord-vand-suspensioner under aerobe og anaerobe forhold 14co2-udbytter på 7,2 og 6.3% (Scheunert et al., 1987). Etal. (2001) undersøgte den fotokemiske nedbrydning af fem polycykliske aromatiske carbonhydrider indieselpartikler deponeret på jorden og i forskellige jordkomponenter. Den fotokemiske nedbrydning ved kunstigt sollys blev opnået ved hjælp af en 900-Volt ksenonlampe.Lys fra denne lampe blev ført gennem et glasfilter for at eliminere lys med kortere bølgelængder (LR2. Derudover blev en solsimulatorudstyret med en 300V-lampe brugt til at give den maksimale sollysintensitet, der blev observeret i Tokyo (breddegrad 35,5 liter N). Halveringstiden for phenanthren i dieselpartikler ved anvendelse af 900-og 300V-kilder var henholdsvis 4,29 og 60,63 h. Følgende halveringstider blev bestemt for phenanthren adsorberet på forskellige jordkomponenter ved anvendelse af 900-h apparater: 3,04 h for kvarts,2,90 h for feltspat, 1,15 h for kaolinit, 4,97 h for montmorillonit, 3,26 h for silicagel og 1,17 h for alumina.
kemisk / fysisk. Den vandige chlorering af phenanthren ved pH 8,8), phenanthren-9,10-oksid, phenanthren-9,10-Dion og 9,10-dihydrophenanthrenediol blev identificeret som vigtige produkter (Oyler et al.,1983). Det blev foreslået, at chlorering af phenanthren i ledningsvand tegnede sig forTilstedeværelsen af chlor – og dichlorphenanthrenes (Shiraishi et al., 1985).
forsendelse
UN3077 miljøfarlige stoffer, faste stoffer, n. o.s., fareklasse: 9; etiketter: 9-diverse farligt materiale, teknisk navn påkrævet.
oprensningsmetoder
sandsynlige forurenende stoffer omfatter antracen, fluoren og andre polycykliske carbonhydrider. Rens det ved destillation fra natrium under vakuum, kogning med maleinsyreanhydrid, krystallisation fra eddikesyre, sublimering og områdesmeltning. Det er også blevet omkrystalliseret gentagne gange fra EtOH, *bensene eller pet ether (b 60-70o), med efterfølgende tørring under vakuum over P2O5 i en Abderhalden pistol. Feldman, Pantages og Orchin adskilt det meste af anthracen Urenhed ved tilbagesvaling phenanthren (671g) med maleinsyreanhydrid (194g) i ksylen (1,25 L) under nitrogen i 22 timer, derefter filtreret. Filtratet blev ekstraheret med vandig 10% NaOH, den organiske fase blev adskilt, og opløsningsmidlet blev fordampet. Remanensen, efter omrøring i 2 timer med 7 g natrium, blev destilleret i vakuum, derefter omkrystalliseret to gange fra 30% *bensin i EtOH. Den blev derefter opløst i varm eddikesyre (2,2 mL/g), og til den blev der langsomt tilsat en vandig opløsning af CrO3 (60 g i 72 ml H2O plus 2,2 L eddikesyre) efterfulgt af langsom tilsætning af conc H2SO4 (30 ml). Blandingen blev tilbagesvalet til 15minutter, fortyndet med et lige volumen vand og afkølet. Bundfaldet blev filtreret af, vasket med vand, tørret og destilleret, derefter omkrystalliseret to gange fra EtOH. Yderligere oprensning er mulig ved kromatografi fra en chcl3-opløsning på aktiveret alumina, med * Bensen som eluent og ved områderaffinering. Picraten (1:1) danner gyldne gule nåle med m 146o, og styfnatet (1: 1) har m 138-139o (plader eller nåle fra henholdsvis EtOH eller EtOH/H2O).
bortskaffelse af affald
Rådfør dig med miljøreguleringsorganer for at få vejledning om acceptabel bortskaffelsespraksis. 100 kg/mo) skal overholde EPA-reglerne for opbevaring, transport, behandling og bortskaffelse af affald.