Das universelle Lösungsmittel
Das universelle Lösungsmittel
Dies ist natürlich eine weitere Schlüsseleigenschaft von Wasser, da sich mehr Substanzen in Wasser lösen als in jeder anderen gewöhnlichen Flüssigkeit. Dies liegt daran, dass das polare Wassermolekül die Auflösungskraft erhöht. Bei der Auflösung werden „Salze“ in „Ionen“ zerlegt.“ Zum Beispiel zerfällt NaCl (Kochsalz) in die Ionen Na+ und Cl- weil die Anziehung von Ionen (Atomen oder Gruppen von Atomen mit einer Ladung) zu Wassermolekülen hoch ist.
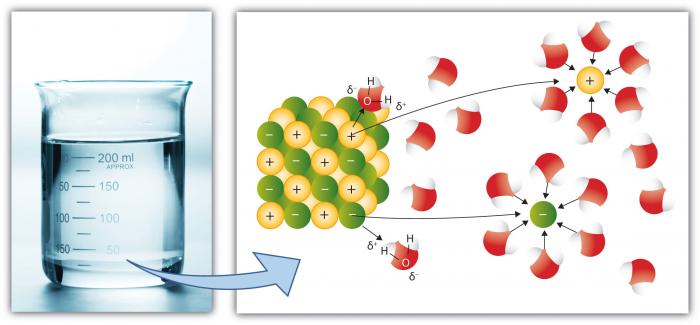
Kationen wie Na (Natrium) haben eine positive Nettoladung, während Anionen (wie Cl, Chlorid) eine negative Nettoladung haben. Es gibt viele einzelne Elemente und Verbindungen, die Ionen bilden. Somit kann Wasser beträchtliche Konzentrationen verschiedener chemischer Spezies enthalten, abhängig von ihren besonderen Eigenschaften. Beachten Sie, wie die Wassermoleküle die einzelnen Ionen umgeben und sie von anderen Ionen in Lösung isoliert halten. An diesem Punkt ist die Lösung mit diesen Ionen „gesättigt“ und kann sich nicht mehr auflösen (Salz beginnt auszufallen — bildet einen Feststoff).