Phenanthren
- Phenanthren Chemische Eigenschaften, Verwendung, Herstellung
- Nichtlineare polyzyklische aromatische Kohlenwasserstoffe
- Molekülstruktur
- Chemische Eigenschaften
- Verwendungen
- Zubereitung
- Chemische Eigenschaften
- Chemische Eigenschaften
- Physikalische Eigenschaften
- Verwendung
- Verwendet
- Begriffsbestimmung
- Herstellungsverfahren
- Synthesereferenz(en)
- Allgemeine Beschreibung
- Luft & Wasserreaktionen
- Reaktivitätsprofil
- Gesundheitsgefahr
- Brandgefahr
- Sicherheitsprofil
- Mögliche Exposition
- Kanzerogenität
- Quelle
- Umweltschicksal
- Versand
- Reinigungsmethoden
- Abfallentsorgung
Phenanthren Chemische Eigenschaften, Verwendung, Herstellung
Nichtlineare polyzyklische aromatische Kohlenwasserstoffe
Phenanthren ist die einfachste nichtlineare polyzyklische aromatische Kohlenwasserstoffe mit drei Benzolringstruktur, wobei das Isomer des Anthracen. Im Jahr 1872 haben E. Ostermayer et al. das Phenanthren in der Anthracenölfraktion im Kohlenteerdestillat als eines der Kohlenteerverarbeitungsprodukte identifiziert. Im Hochtemperatur-Kohlenteer ist der Phenanthrengehalt nur sekundär zu Naphthalin und beträgt etwa 4 bis 6%, hauptsächlich konzentriert in den Anthracenölfraktionen. Die chemische Aktivität von Phenanthren ist stärker als die von Naphthalin, aber schwächer als die von Anthracen, und die Oxidations- und Additionsreaktionen können auch an 9- und 10-Positionen auftreten.
Das Phenanthren ist ein farbloser Kristall mit Glanz, und das aus Ethanol ausgefällte Phenanthren ist ein farbloser monokliner Kristall. Das Phenanthren ist ein blattartiger Kristall mit einer relativen Dichte von 1.179 (25/4 ℃) und ein brechungsindex von 1,6450, schmelzpunkt von 101 °C und siedepunkt von 340 °C. Es kann gegenstand sublimation, unlöslich in wasser, leicht löslich in ethanol, löslich in ether, benzol, essigsäure, chloroform, tetrachlorkohlenstoff und schwefelkohlenstoff. Die Lösung zeigt blaue Fluoreszenz. Die 1, 4, 5, 8-Positionen sind die gleichen, bekannt als α-Position; die 2, 3, 6, 7-Position sind auch die gleichen, bekannt als β-Position; die 9, 10-Positionen sind die gleichen, bekannt als ?-Position. Seine chemische Eigenschaft liegt zwischen Naphthalin und Anthracen. Es kann auch Additionsreaktion in der 9, 10-Position haben, aber nicht so einfach wie Anthracen. Oxidation tritt auch an der 9, 10-Position auf, wobei Oxidation Phenanthrenchinon ergibt. Es können auch Substitutionsreaktionen auftreten. Es kann auch durch Abtrennung von der Anthracenölfraktion von Kohlenteeröl erhalten werden. Phenanthren kann bei der Herstellung von Pestiziden und Farbstoffen verwendet werden, aber auch als Stabilisator der hohen Effizienz & Pestizide mit geringer Toxizität und rauchlose Pulversprengstoffe.
Phenanthren kann zur Herstellung von Farbstoffen, Arzneimitteln und Harzen nach der Konversionsverarbeitung verwendet werden. Die Oxidationsprodukte Phenanthrenchinon können als Farbstoffe, Fungizide und Polymerisationsinhibitoren verwendet werden; 9, 10-Biphenyldicarbonsäure wird zur Herstellung von Polyester und Alkydharz verwendet; 9, 10-Dihydro-9-phenathroinsäure ist ein pflanzenwachstumsstimulierendes Hormon; Perhydrophenanthren, das durch Hydrierung von Phenanthren hergestellt wird, kann zur Herstellung von Düsentreibstoff verwendet werden; sein sulfoniertes Produkt, Phenanthrensulfonsäure, kann als Bindemittel und Gerbung verwendet werden.
Die Phenanthren enthaltende Mutterlauge bei der Herstellung von raffiniertem Anthracen mit Lösungsmittelverfahren, nach Rückgewinnung von Lösungsmittel und weitere Kristallisation Filtration kann roh Phenanthren mit 40% Phenanthren geben.
Das rohe Phenanthren wird nach Entfernen von Lösungsmittelrückständen im Schmelzkessel und anschließender Rektifizierung im Verstärkungsturm mit 20 theoretischen Böden die Fraktionen von 335 bis 340 ° C ausgeschnitten, gefolgt von Kühlung, Kristallisation und Filtration, um das technische Phenanthren mit dem Phenanthrengehalt von mehr als 70% zu erhalten. .
Die obigen Informationen werden von Tongtong von Chemicalbook zusammengestellt.
Molekülstruktur
Die Molekülstruktur von Phenanthren und Anthracen ist einander ähnlich, wobei sich alle Atome in derselben Ebene befinden, jedoch nicht in derselben Linie. Die 1, 2, 3, 4, 10 Positionen und 5, 6, 7, 8, 9 Positionen innerhalb der Moleküle entsprechen einander, aber es gab Unterschiede in der Aktivität an den 5 Positionen, unter denen 9 und 10 eine höhere Aktivität mit Substitution, Oxidation und Addition in 9 und 10 Positionen aufwiesen: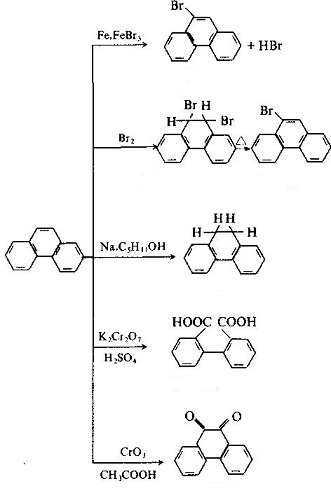
Phenanthrenchinon ist ein Pestizid, das als keimtötende Saatgutbeizung verwendet wird und in der Lage ist, Weizenschorf, harten Schmutz und süßkartoffel schwarzer Fleck.
Industrielles Phenanthren wird aus der Destillation von Anthracenöl gewonnen, das aus Kohlenteerdestillat gewonnen wird. Viele Arten von Naturprodukten (wie Sterole) enthalten dieses Ringsystem. Phenanthren wird hauptsächlich bei der Herstellung von Farbstoffen, Arzneimitteln, hoher Effizienz und geringer Toxizität von Pestiziden verwendet und kann als Szintillantien, rauchloser Pulverstabilisator verwendet werden. Viele der Phenanthrenderivate haben krebserzeugende physiologische Wirkungen. Wie zum Beispiel: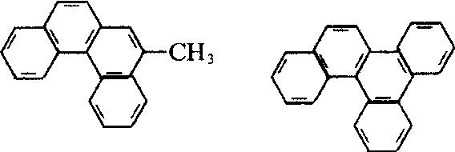
Die Molekülstruktur von 2-Methyl-3, 4-benzophenanthren und 1, 2, 3, 4-dibenzophen
Chemische Eigenschaften
Es erscheint als weißer Glanz und fluoreszierende Flockenkristalle. Es ist nicht löslich in Wasser, leicht löslich in Ethanol, löslich in Ether, Essigsäure, Benzol, Tetrachlorkohlenstoff und Schwefelkohlenstoff.
Verwendungen
Es kann zur Herstellung von Phenanthrenchinon, Kunstharz, Pestiziden und Konservierungsmitteln usw. verwendet werden.
Phenanthren, durch die Oxidation kann Phenanthrenchinon geben, verwendet werden, um die organischen Quecksilber-Pestizide Ceresin und Gallotox zu ersetzen. Die aus ihrer Oxidation erhaltene Biphenylsäure kann zur Herstellung von Alkydharz verwendet werden. Phenanthrenoxidation kann auch Anhydrid, Cyclohexanon und Phenol ergeben. Die Chlorierungsprodukte von Phenanthren können zur Herstellung nicht brennbarer elektrischer Isolatoren und Imprägniermittel verwendet werden. Die sulfonierte Phenanthrensulfonsäure kann aus Bindemittel, Gerbung und so weiter hergestellt werden. Tatsächlich müssen die meisten dieser Anwendungen jedoch noch entwickelt werden. In der Papierindustrie kann das Phenanthren als Zellstoff-Antifog-Mittel verwendet werden; kann auch für Nitroglycerinsprengstoffe und Nitrozellulosestabilisatoren und für die Herstellung von Rauchbomben verwendet werden; Das feste Oxid von Phenanthren kann aus ausgezeichneten flammhemmenden elektrischen Isoliermaterialien und Füllstoffen hergestellt werden. In der Medizin kann Phenanthren zur Synthese von Alkaloiden verwendet werden – Morphin und Koffein, Dimethylmorphin sowie Arzneimittel mit besonderen physiologischen Wirkungen auf viele Fortpflanzungsorgane. In der Farbstoffindustrie kann das Phenanthren aus 2-Aminophenanthrenchinon, Benzanthron, Sulfidreduktionsfarbstoff (blau BO, schwarz BB und braun) und so weiter hergestellt werden. Darüber hinaus können die Kunststoffindustrie, synthetische Gerbstoffe und Phenanthren unter hoher Temperatur und hohem Druck hydriert werden, um Hydrophenanthren zu erhalten, das der Treibstoff für ältere Düsenflugzeuge ist.
Zur Bestimmung des Molekulargewichts und der Synthese organischer Verbindungen.
Zubereitung
Phenanthren ist ein relativ hoher Gehalt an Kohlenteer, der 5% des Kohlenteers ausmacht und nach dem Naphthalingehalt an zweiter Stelle steht. Das Anthracenöl im 300-360 ℃ Bruchbereich von Kohlenteer hat den höchsten Gehalt an Phenanthren, gefolgt von Anthracen und Carbazol und so weiter. Die Phenanthren-Extraktionsmethode besteht normalerweise darin, Anthracenöl zur Kühlung, Kristallisation und dann Vakuumfiltration oder Zentrifugaltrennung zur Öltrennung zu senden. Die relativ hohe Menge an löslichen Phenolen in Ölen kann mit einem Präzisionsdestillationsverfahren zurückgewonnen werden. Der erhaltene Kristall wird rohes Anthracen genannt, das 25-30% Anthracen, 22-25% Carbazol und 30% Phenanthren enthält. Rohes Anthracen kann vor der Umkristallisation und Filtration einer starken Benzolextraktion, Kühlung, Filtration mit dem aus dem Lösungsmittel gedämpften Filtrat unterzogen werden. Nehmen Sie Filtrat zur Destillation, damit wir industrielles Phenanthren mit Sulfonierung erhalten können, um feines Phenanthren zu erhalten.
Chemische Eigenschaften
weiße Kristalle
Chemische Eigenschaften
Phenanthren ist eine weiße kristalline Substanz. Schwacher aromatischer Geruch. Polyzyklische aromatische Kohlenwasserstoffe (PAK) sind Verbindungen mit mehreren Benzolringen und werden auch als mehrkernige aromatische Kohlenwasserstoffe bezeichnet.
Physikalische Eigenschaften
Farblose, monokline Kristalle mit schwachem, aromatischem Geruch
Verwendung
Phenanthren ist ein polyzyklischer aromatischer Kohlenwasserstoff, ein Umweltschadstoff.
Verwendet
Markierte polyzyklische aromatische Kohlenwasserstoffe als Mikroverunreinigungen.
Begriffsbestimmung
Tschebi: Ein polyzyklischer aromatischer Kohlenwasserstoff, der aus drei kondensierten Benzolringen besteht und seinen Namen von den beiden Begriffen Phenyl und Anthracen hat.
Herstellungsverfahren
Phenanthren kommt in Kohlenteer vor und kann aus verschiedenen Erdölsorten isoliert werden.
Synthesereferenz(en)
Zeitschrift für heterocyclische Chemie, 30, p. 291, 1993 DOI: 10.1002/jhet.5570300151
The Journal of Organic Chemistry, 18, S. 801, 1953 DOI: 10.1021/jo50013a004
Tetrahedron Letters, 15, S. 495, 1974
Allgemeine Beschreibung
Farblose monokline Kristalle mit schwach aromatischem Geruch. Lösungen zeigen eine blaue Fluoreszenz.
Luft & Wasserreaktionen
Unlöslich in Wasser.
Reaktivitätsprofil
Phenanthren kann mit oxidierenden Stoffen reagieren.
Gesundheitsgefahr
Die akute orale Toxizität von Phenanthren ist low.It ist giftiger als Anthracen. Ein oraler LD50-Wert bei Mäusen wird bei 700 mg / kg berichtet. Es maycause Tumor in der Haut an der Stelle der Anwendung.Der Nachweis der Kanzerogenität bei Tieren ist jedoch unzureichend.
Brandgefahr
Phenanthren ist brennbar.
Sicherheitsprofil
Intravenöse Verabreichung. Mäßig giftig durch Verschlucken. Mutationsdaten gemeldet. Ein Photosensibilisator der menschlichen Haut. Fragwürdiges Karzinogen mit experimentellen neoplastischen und tumorigenen Daten durch Hautkontakt. Brennbar bei Hitze oder Flamme; kann heftig mit oxidierenden Materialien reagieren. Verwenden Sie zur Brandbekämpfung Wasser, Schaum, CO2 und Trockenchemikalien. Wenn es zur Zersetzung erhitzt wird, emittiert es beißenden Rauch und reizende Dämpfe
Mögliche Exposition
Staub kann mit Luft ein explosives Gemisch bilden. Unverträglich mit Oxidationsmitteln (Chlorate, Nitrate, Peroxide, Permanganate, Perchlorate, Chlor, Brom, Fluor usw.); kontakt kann Brände oder Explosionen verursachen. Von alkalischen Materialien, starken Basen, starken Säuren, Oxosäuren und Epoxiden fernhalten.
Kanzerogenität
Phenanthren ist als Initiator unwirksam. Es ist nicht in Bezug auf die Kanzerogenität beim Menschen —Klasse 3 nach IARC und Klasse D nach IRIS – klassifizierbar, basierend aufkeinen Humandaten und unzureichenden Daten aus einer einzigen Gava-Studie an Ratten und Hautbemalungs- und Injektionsstudien an Maus.
Quelle
Nachgewiesen im Grundwasser unterhalb einer ehemaligen Kohlevergasungsanlage in Seattle, WA bei einer Konzentration von 130 µg/l (ASTR, 1995). Nachgewiesen in 8 Dieselkraftstoffen in Konzentrationen von 0,17- 110 mg / l mit einem Mittelwert von 41,43 mg / l (Westerholm und Li, 1994) und in destillierten wasserlöslichen Fraktionen von neuem und gebrauchtem Motoröl in Konzentrationen von 1,9-2,1 bzw. 2,1–2,2 µg / l (Chen et al., 1994). In: Lee et al. (1992) berichteten Konzentrationsbereiche von 100 bis 300 mg / l und 15 bis 25 µg / l in Dieselkraftstoff bzw. der entsprechenden wässrigen Phase (destilliertes Wasser). Schauer et al. (1999) berichteten über Phenanthren in Dieselkraftstoff mit einer Konzentration von 57 µg / g und in einem dieselbetriebenen mittelschweren LKW-Auspuff mit einer Emissionsrate von 93,1 µg / km.Identifiziert in Kuwait und South Louisiana Rohöle bei Konzentrationen von 26 bzw. 70 ppm (Pancirov und Brown, 1975). Dieselkraftstoff aus einer Tankstelle in Schlieren, Schweiz, enthielt Phenanthren in einer geschätzten Konzentration von 327 mg / l (Schluep et al.,2001).
Phenanthren wurde in Asphaltdämpfen bei einer durchschnittlichen Konzentration von 57,73 ng/m3 nachgewiesen (Wanget al., 2001).
Thomas und Delfino (1991) äquilibrierten kontaminationsfreies Grundwasser aus Gainesville, FL, mit einzelnen Fraktionen von drei einzelnen Erdölprodukten bei 24-25 ° C für 24 h. Die wässrige Phase wurde mit der von der US-amerikanischen EPA zugelassenen Testmethode auf organische Verbindungen analysiert625. Phenanthren wurde nur in der wasserlöslichen Fraktion von Dieselkraftstoff bei einer durchschnittlichen Konzentration von 17 µg / l nachgewiesen.
Basierend auf einer Laboranalyse von 7 Kohlenteerproben lagen die Phenanthrenkonzentrationen zwischen 3.100 und 35.000 ppm (EPRI, 1990). Nachgewiesen in 1-jährigem gealtertem Kohlenteerfilm und Massenkohlenteer bei einer identischen Konzentration von 10.000 mg / kg (Nelson et al., 1996). Ein Hochtemperatur-Kohlenteer enthielt Phenanthren in einer durchschnittlichen Konzentration von 2,66 Gew.-% (McNeil, 1983). Auch identifiziert in Hochtemperatur-Kohlenteerpech bei Konzentrationen im Bereich von 7.500 bis 40.300 mg / kg (Arrendale und Rogers, 1981). In: Lee et al. (1992a) äquilibrierte acht Kohlenteer mit destilliertem Wasser bei25 ° C. Die maximale Konzentration von Phenanthren in der wässrigen Phase beträgt 0,4 mg / L.Neun kommerziell erhältliche Kreosotproben enthielten Phenanthren in Konzentrationen von 48.000 bis 120.000 mg/kg (Kohler et al., 2000).Eine typische Konzentration von Phenanthren in einem schweren Pyrolyseöl beträgt 2,5 Gew.-% (Chevron Phillips, Mai 2003).
Umweltschicksal
Biologisch. Catechol ist der zentrale Metabolit beim bakteriellen Abbau von Phenanthren.Zwischenprodukte umfassen 1-Hydroxy-2-Naphthoesäure, 1,2-dihydroxynaphthalin undsalicylsäure (Chapman, 1972; Hou, 1982). Es wurde berichtet, dass Beijerinckia unter aeroben Bedingungen Phenanthren zu cis-3,4-Dihydroxy-3,4-dihydrophenanthracen abbaute (Kobayashi und Rittman, 1982).
Boden. Die berichteten Halbwertszeiten für Phenanthren in einem Kidman Sandy Loam und McLaurin Sandyloam sind 16 bzw. 35 d (Park et al., 1990). Manilal und Alexander (1991) berichteten über eine Halbwertszeit von 11 d in einem Kendaia-Boden.
Oberflächenwasser. In einem 5 m tiefen Oberflächenwasserkörper betrugen die berechneten Halbwertszeiten für die direkte photochemische Transformation bei 40 ° N Breite im Hochsommer während der Mittagszeit 59 bzw. 69 d mit und ohne Sediment-Wasser-Verteilung (Zepp und Schlotzhauer, 1979).
Photolytisch. Eine Kohlendioxid-Ausbeute von 24,2% wurde erreicht, wenn auf Silica-Gel adsorbiertes Phenanthren 17 h lang mit Licht (λ >290 nm) bestrahlt wurde (Freitag et al., 1985). In einem 2-Wkexperiment ergab die Anwendung von Phenanthren auf Boden-Wasser-Suspensionen unter aeroben und anaeroben Bedingungen 14CO 2-Ausbeuten von 7,2 und 6.3% (Scheunert et al., 1987). Matsuzawa etal. (2001) untersuchten den photochemischen Abbau von fünf polyzyklischen aromatischen Kohlenwasserstoffen Indieselpartikeln, die sich auf dem Boden und in verschiedenen Bodenkomponenten ablagern. Der photochemische Abbau durch künstliches Sonnenlicht erfolgte mit einer 900-W-Xenonlampe.Das Licht dieser Lampe wurde durch einen Glasfilter geleitet, um Licht kürzerer Wellenlängen zu eliminieren (λ2. Zusätzlich wurde ein mit einer 300-W-Xenonlampe ausgestatteter Sonnensimulator verwendet, um die in Tokio beobachtete maximale Sonnenlichtintensität (35,5 °nördlicher Breite) zu ermitteln. Die Halbwertszeiten von Phenanthren in Dieselpartikeln mit 900- und 300-W-Quellen betrugen 4,29 bzw. 60,63 h. Die folgenden Halbwertszeiten wurden für Phenanthren bestimmt, das an verschiedenen Bodenkomponenten mit 900-W-Apparaten adsorbiert wurde: 3,04 h für Quarz, 2,90 h für Feldspat, 1,15 h für Kaolinit, 4,97 h für Montmorillonit, 3,26 h für Kieselgel und 1,17 h für Aluminiumoxid.
Chemisch/Physikalisch. Die wässrige Chlorierung von Phenanthren bei pH 8,8), Phenanthren-9,10-oxid, Phenanthren-9,10-dion und 9,10-dihydrophenanthrendiol wurden als Hauptprodukte identifiziert (Oyler et al.,1983). Es wurde vorgeschlagen, dass die Chlorierung von Phenanthren in Leitungswasser für das Vorhandensein von Chlor- und Dichlorphenanthrenen verantwortlich ist (Shiraishi et al., 1985).
Versand
UN3077 Umweltgefährdende Stoffe, fest, n.a.g., Gefahrenklasse: 9; Etiketten: 9-Verschiedenes Gefahrgut, Technische Bezeichnung erforderlich.
Reinigungsmethoden
Zu den wahrscheinlichen Verunreinigungen gehören Anthracen, Carbazol, Fluoren und andere polyzyklische Kohlenwasserstoffe. Reinigen Sie es durch Destillation von Natrium im Vakuum, Kochen mit Maleinsäureanhydrid in Xylol, Kristallisation aus Essigsäure, Sublimation und Zonenschmelzen. Es wurde auch mehrfach aus EtOH, *Benzol oder PET-Ether (b 60-70o) umkristallisiert und anschließend im Vakuum über P 2 O 5 in einer Abderhaldenpistole getrocknet. Feldman, Pantages und Orchin trennten den größten Teil der Anthracenverunreinigung durch Rückfluss von Phenanthren (671 g) mit Maleinsäureanhydrid (194 g) in Xylol (1,25 l) unter Stickstoff für 22 Stunden, dann filtriert. Das Filtrat wurde mit wässriger 10%iger NaOH extrahiert, die organische Phase abgetrennt und das Lösungsmittel eingedampft. Der Rückstand wurde nach 2stündigem Rühren mit 7g Natrium im Vakuum destilliert und anschließend zweimal aus 30%igem Benzol in EtOH umkristallisiert. Es wurde dann in heißer Essigsäure (2,2 ml / g) gelöst und langsam mit einer wässrigen Lösung von CrO3 (60 g in 72 ml H2O plus 2,2 l Essigsäure) versetzt, gefolgt von einer langsamen Zugabe von conc H2SO4 (30 ml). Die Mischung wurde 15 Minuten unter Rückfluss gekocht, mit einem gleichen Volumen Wasser verdünnt und abgekühlt. Der Niederschlag wurde abfiltriert, mit Wasser gewaschen, getrocknet, destilliert und anschließend zweimal aus EtOH umkristallisiert. Eine weitere Reinigung ist durch Chromatographie aus einer CHCl 3-Lösung auf aktiviertem Aluminiumoxid mit *Benzol als Laufmittel und durch Zonenraffination möglich. Das Picrat (1:1) bildet mit m 146o goldgelbe Nadeln, und das Styphnate (1:1) hat m 138-139o (Platten oder Nadeln aus EtOH bzw. EtOH/H2O).
Abfallentsorgung
Wenden Sie sich an die Umweltaufsichtsbehörden, um Hinweise zu akzeptablen Entsorgungspraktiken zu erhalten. Die Erzeugung von Abfällen, die diese Verunreinigung enthalten (≥100 kg / mo), muss den EPA-Vorschriften für Lagerung, Transport, Behandlung und Entsorgung entsprechen.