Vicodin ES
Generischer Name: Acetaminophen und Hydrocodonbitartrat
Darreichungsform: Tablette
Medizinisch überprüft von Drugs.com . Zuletzt aktualisiert am Jul 22, 2020.
- Nebenwirkungen
- Dosierung
- Professional
- Wechselwirkungen
- Schwangerschaft
- Bewertungen
- Mehr
Der Markenname Vicodin ES wurde in den USA eingestellt Wenn generische Versionen dieses Produkts von der FDA zugelassen wurden, sind möglicherweise generische Äquivalente verfügbar.
- Warnung
- Vicodin ES Beschreibung
- Vicodin ES – Klinische Pharmakologie
- Pharmakokinetik
- Indikationen und Verwendung für Vicodin ES
- Kontraindikationen
- Warnhinweise
- Hepatotoxizität
- Überempfindlichkeit/Anaphylaxie
- Atemdepression
- Kopfverletzung und erhöhter intrakranieller Druck
- Akute abdominale Zustände
- Vorsichtsmaßnahmen
- Allgemein
- Informationen für Patienten/Pflegepersonal
- Labortests
- Arzneimittelwechselwirkungen
- Arzneimittel- /Labortest-Wechselwirkungen
- Karzinogenese, Mutagenese, Beeinträchtigung der Fertilität
- Schwangerschaft
- Wehen und Entbindung
- Stillende Mütter
- Pädiatrische Anwendung
- Geriatrische Anwendung
- Nebenwirkungen
- Zentralnervensystem
- Magen-Darm-System
- Urogenitalsystem
- Atemdepression
- Special Senses
- Dermatologisch
- Drogenmissbrauch und -abhängigkeit
- Kontrollierte Substanz
- Missbrauch und Abhängigkeit
- Überdosierung
- Anzeichen und Symptome
- Behandlung
- Vicodin ES Dosierung und Verabreichung
- Wie wird Vicodin ES geliefert
- LAGERUNG
- More about Vicodin ES (acetaminophen / hydrocodone)
- Professional resources
- Verwandte Behandlungsleitfäden
Warnung
PARACETAMOL WURDE MIT FÄLLEN VON AKUTEM LEBERVERSAGEN IN VERBINDUNG GEBRACHT, DAS MANCHMAL ZU LEBERTRANSPLANTATION UND TOD FÜHRTE. DIE MEISTEN FÄLLE VON LEBERSCHÄDEN SIND MIT DER VERWENDUNG VON PARACETAMOL IN DOSEN VON MEHR ALS 4000 MILLIGRAMM PRO TAG VERBUNDEN UND BETREFFEN HÄUFIG MEHR ALS EIN PARACETAMOLHALTIGES PRODUKT.
Vicodin ES Beschreibung
Hydrocodonbitartrat und Paracetamol werden in Tablettenform zur oralen Verabreichung geliefert.
WARNUNG: Kann gewohnheitsbildend sein (siehe VORSICHTSMAßNAHMEN, Informationen für Patienten / Betreuer und DROGENMISSBRAUCH UND -ABHÄNGIGKEIT).
Hydrocodonbitartrat ist ein Opioid-Analgetikum und Antitussivum und kommt als feine, weiße Kristalle oder als kristallines Pulver vor. Es wird durch Licht beeinflusst. Der chemische Name ist 4,5α-Epoxy-3-methoxy-17-methylmorphinan-6-on tartrat (1:1) Hydrat (2:5). Es hat die folgende Strukturformel:
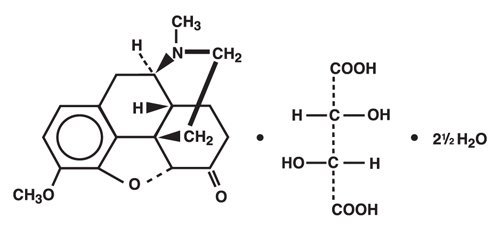 C18H21NO3·C4H6O6·2½H2O M.W. = 494.490
C18H21NO3·C4H6O6·2½H2O M.W. = 494.490
Acetaminophen, 4′-Hydroxyacetanilid, ein leicht bitteres, weißes, geruchloses, kristallines Pulver, ist ein Nicht-Opiat, Nicht-Salicylat Analgetikum und Antipyretikum. Es hat die folgende Strukturformel:
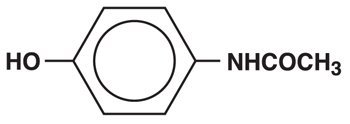 C8H9NO2 M.W. = 151.16
C8H9NO2 M.W. = 151.16
Hydrocodonbitartrat und Acetaminophentabletten, USP ist in den folgenden Stärken erhältlich:
VICODIN®: Hydrocodonbitartrat….. 5 mg
WARNUNG: Kann zur Gewohnheit werden.
Paracetamol….. 300 mg
Vicodin ES®: Hydrocodonbitartrat….. 7,5 mg
WARNUNG: Kann zur Gewohnheit werden.
Paracetamol….. 300 mg
VICODIN HP®: Hydrocodonbitartrat….. 10 mg
WARNUNG: Kann zur Gewohnheit werden.
Paracetamol….. 300 mg
Zusätzlich enthält jede Tablette die folgenden inaktiven Bestandteile: kolloidales Siliciumdioxid, Crospovidon, Magnesiumstearat, mikrokristalline Cellulose, Povidon, vorgelatinierte Stärke und Stearinsäure.
Dieses Produkt entspricht dem USP Dissolution Test 2.
Vicodin ES – Klinische Pharmakologie
Hydrocodon ist ein halbsynthetisches narkotisches Analgetikum und Antitussivum mit mehreren Wirkungen, die denen von Codein qualitativ ähnlich sind. Die meisten davon betreffen das zentrale Nervensystem und die glatte Muskulatur. Der genaue Wirkungsmechanismus von Hydrocodon und anderen Opiaten ist nicht bekannt, obwohl angenommen wird, dass er sich auf die Existenz von Opiatrezeptoren im Zentralnervensystem bezieht. Zusätzlich zur Analgesie können Betäubungsmittel Schläfrigkeit, Stimmungsschwankungen und geistige Trübung hervorrufen.
Die analgetische Wirkung von Paracetamol beinhaltet periphere Einflüsse, aber der spezifische Mechanismus ist noch unbestimmt. Die antipyretische Aktivität wird durch hypothalamische Wärmeregulierungszentren vermittelt. Acetaminophen hemmt die Prostaglandinsynthetase. Therapeutische Dosen von Paracetamol haben vernachlässigbare Auswirkungen auf das Herz-Kreislauf- oder Atmungssystem; toxische Dosen können jedoch zu Kreislaufversagen und schneller, flacher Atmung führen.
Pharmakokinetik
Das Verhalten der einzelnen Komponenten wird nachfolgend beschrieben.
Hydrocodon
Nach einer oralen Dosis von 10 mg Hydrocodon, die fünf erwachsenen männlichen Probanden verabreicht wurde, betrug die mittlere Spitzenkonzentration 23,6 ± 5,2 ng/ml. Die maximalen Serumspiegel wurden nach 1,3 ± 0,3 Stunden erreicht und die Halbwertszeit wurde mit 3,8 ± 0,3 Stunden bestimmt. Hydrocodon zeigt ein komplexes Muster des Metabolismus einschließlich O-Demethylierung, N-Demethylierung und 6-Keto-Reduktion zu den entsprechenden 6-α- und 6-β-Hydroxy-Metaboliten. Siehe ÜBERDOSIERUNG für Toxizitätsinformationen.
Paracetamol
Paracetamol wird schnell aus dem Magen-Darm-Trakt resorbiert und in den meisten Körpergeweben verteilt. Die Plasmahalbwertszeit beträgt 1,25 bis 3 Stunden, kann aber durch Leberschäden und nach Überdosierung erhöht werden. Die Elimination von Paracetamol erfolgt hauptsächlich durch Lebermetabolismus (Konjugation) und anschließende renale Ausscheidung von Metaboliten. Etwa 85% einer oralen Dosis erscheint im Urin innerhalb von 24 Stunden nach der Verabreichung, die meisten als Glucuronid-Konjugat, mit geringen Mengen anderer Konjugate und unveränderter Arzneimittel. Siehe ÜBERDOSIERUNG für Toxizitätsinformationen.
Indikationen und Verwendung für Vicodin ES
Hydrocodonbitartrat- und Acetaminophentabletten sind zur Linderung von mittelschweren bis mittelschweren Schmerzen indiziert.
Kontraindikationen
Dieses Produkt sollte nicht bei Patienten angewendet werden, die zuvor eine Überempfindlichkeit gegen Hydrocodon oder Paracetamol gezeigt haben.
Patienten, von denen bekannt ist, dass sie gegenüber anderen Opioiden überempfindlich sind, können eine Kreuzempfindlichkeit gegenüber Hydrocodon aufweisen.
Warnhinweise
Hepatotoxizität
Paracetamol wurde mit Fällen von akutem Leberversagen in Verbindung gebracht, das manchmal zu Lebertransplantation und Tod führte. Die meisten Fälle von Leberschäden sind mit der Verwendung von Paracetamol in Dosen von mehr als 4000 Milligramm pro Tag verbunden und betreffen häufig mehr als ein paracetamolhaltiges Produkt. Die übermäßige Einnahme von Paracetamol kann absichtlich sein, um Selbstverletzung oder unbeabsichtigt zu verursachen, wenn Patienten versuchen, mehr Schmerzlinderung zu erhalten oder unwissentlich andere paracetamolhaltige Produkte einzunehmen.
Das Risiko eines akuten Leberversagens ist bei Personen mit zugrunde liegender Lebererkrankung und bei Personen, die während der Einnahme von Paracetamol Alkohol zu sich nehmen, höher.Weisen Sie die Patienten an, auf den Packungsetiketten nach Paracetamol oder APAP zu suchen und nicht mehr als ein Produkt zu verwenden, das Paracetamol enthält. Weisen Sie die Patienten an, sofort nach Einnahme von mehr als 4000 Milligramm Paracetamol pro Tag einen Arzt aufzusuchen, auch wenn sie sich gut fühlen.
Schwerwiegende Hautreaktionen
In seltenen Fällen kann Paracetamol schwerwiegende Hautreaktionen wie akute generalisierte exanthematöse Pustulose (AGEP), Stevens-Johnson-Syndrom (SJS) und toxische epidermale Nekrolyse (TEN) verursachen, die tödlich sein können. Die Patienten sollten über die Anzeichen schwerwiegender Hautreaktionen informiert werden, und die Anwendung des Arzneimittels sollte beim ersten Auftreten von Hautausschlag oder anderen Anzeichen einer Überempfindlichkeit abgebrochen werden.
Überempfindlichkeit/Anaphylaxie
Nach Markteinführung gab es Berichte über Überempfindlichkeit und Anaphylaxie im Zusammenhang mit der Anwendung von Paracetamol. Zu den klinischen Symptomen gehörten Schwellungen von Gesicht, Mund und Rachen, Atemnot, Urtikaria, Hautausschlag, Pruritus und Erbrechen. Es gab selten Berichte über lebensbedrohliche Anaphylaxie, die eine medizinische Notfallversorgung erforderten. Weisen Sie die Patienten an, Hydrocodonbitartrat- und Paracetamol-Tabletten sofort abzusetzen und bei Auftreten dieser Symptome einen Arzt aufzusuchen. Verschreiben Sie keine Hydrocodonbitartrat- und Paracetamol-Tabletten für Patienten mit Paracetamolallergie.
Atemdepression
Bei hohen Dosen oder bei empfindlichen Patienten kann Hydrocodon eine dosisabhängige Atemdepression hervorrufen, indem es direkt auf das Atemzentrum des Hirnstamms einwirkt. Hydrocodon beeinflusst auch das Zentrum, das den Atemrhythmus steuert, und kann unregelmäßige und periodische Atmung erzeugen.
Kopfverletzung und erhöhter intrakranieller Druck
Die respiratorische dämpfende Wirkung von Betäubungsmitteln und ihre Fähigkeit, den zerebrospinalen Flüssigkeitsdruck zu erhöhen, können bei Kopfverletzungen, anderen intrakraniellen Läsionen oder einem bereits bestehenden Anstieg des intrakraniellen Drucks deutlich übertrieben sein. Darüber hinaus verursachen Narkotika Nebenwirkungen, die den klinischen Verlauf von Patienten mit Kopfverletzungen verschleiern können.
Akute abdominale Zustände
Die Verabreichung von Betäubungsmitteln kann die Diagnose oder den klinischen Verlauf von Patienten mit akuten abdominalen Zuständen verdecken.
Vorsichtsmaßnahmen
Allgemein
Patienten mit besonderem Risiko
Wie bei jedem narkotischen Analgetikum sollten Hydrocodonbitartrat- und Paracetamol-Tabletten bei älteren oder geschwächten Patienten und Patienten mit schwerer Leber- oder Nierenfunktionsstörung, Hypothyreose, Morbus Addison, Prostatahypertrophie oder Harnröhrenstriktur mit Vorsicht angewendet werden. Die üblichen Vorsichtsmaßnahmen sollten beachtet und die Möglichkeit einer Atemdepression berücksichtigt werden.
Hustenreflex
Hydrocodon unterdrückt den Hustenreflex; wie bei allen Betäubungsmitteln ist Vorsicht geboten, wenn Hydrocodonbitartrat- und Paracetamol-Tabletten postoperativ und bei Patienten mit Lungenerkrankungen angewendet werden.
Informationen für Patienten/Pflegepersonal
- Nehmen Sie keine Hydrocodonbitartrat- und Paracetamol-Tabletten ein, wenn Sie gegen einen der Bestandteile allergisch sind.
- Wenn Sie Anzeichen einer Allergie wie Hautausschlag oder Atembeschwerden entwickeln, beenden Sie die Einnahme von Hydrocodonbitartrat und Paracetamol-Tabletten und wenden Sie sich sofort an Ihren Arzt.
- Nehmen Sie nicht mehr als 4000 Milligramm Paracetamol pro Tag ein. Rufen Sie Ihren Arzt, wenn Sie mehr als die empfohlene Dosis eingenommen haben.
Hydrocodon kann wie alle Betäubungsmittel die geistigen und/ oder körperlichen Fähigkeiten beeinträchtigen, die für die Ausführung potenziell gefährlicher Aufgaben wie Autofahren oder Bedienen von Maschinen erforderlich sind.
Alkohol und andere ZNS-Depressiva können bei Einnahme mit diesem Kombinationspräparat eine additive ZNS-Depression hervorrufen und sollten vermieden werden.
Hydrocodon kann Gewohnheit bilden. Patienten sollten das Medikament nur so lange einnehmen, wie es verschrieben wird, in den vorgeschriebenen Mengen und nicht häufiger als vorgeschrieben.
Labortests
Bei Patienten mit schwerer Leber- oder Nierenerkrankung sollten die Auswirkungen der Therapie mit seriellen Leber- und/ oder Nierenfunktionstests überwacht werden.
Arzneimittelwechselwirkungen
Patienten, die andere Betäubungsmittel, Antihistaminika, Antipsychotika, Antiangstmittel oder andere ZNS-Depressiva (einschließlich Alkohol) gleichzeitig mit Hydrocodonbitartrat und Paracetamol-Tabletten erhalten, können eine additive ZNS-Depression aufweisen. Wenn eine Kombinationstherapie in Betracht gezogen wird, sollte die Dosis eines oder beider Wirkstoffe reduziert werden.
Die Verwendung von MAO-Hemmern oder trizyklischen Antidepressiva mit Hydrocodonpräparaten kann die Wirkung von Antidepressiva oder Hydrocodon verstärken.
Arzneimittel- /Labortest-Wechselwirkungen
Paracetamol kann zu falsch positiven Testergebnissen für 5-Hydroxyindolessigsäure im Urin führen.
Karzinogenese, Mutagenese, Beeinträchtigung der Fertilität
Es wurden keine ausreichenden Studien an Tieren durchgeführt, um festzustellen, ob Hydrocodon oder Paracetamol ein Potenzial für Karzinogenese, Mutagenese oder Beeinträchtigung der Fertilität haben.
Schwangerschaft
Teratogene Wirkungen
Schwangerschaftskategorie C
Es liegen keine ausreichenden und gut kontrollierten Studien bei Schwangeren vor. Hydrocodonbitartrat und Paracetamol-Tabletten sollten während der Schwangerschaft nur angewendet werden, wenn der potenzielle Nutzen das potenzielle Risiko für den Fötus rechtfertigt.
Nicht-teratogene Wirkungen
Babys von Müttern, die vor der Entbindung regelmäßig Opioide eingenommen haben, sind körperlich abhängig. Zu den Entzugserscheinungen gehören Reizbarkeit und übermäßiges Weinen, Zittern, hyperaktive Reflexe, erhöhte Atemfrequenz, vermehrter Stuhlgang, Niesen, Gähnen, Erbrechen und Fieber. Die Intensität des Syndroms korreliert nicht immer mit der Dauer des Opioidkonsums oder der Dosis der Mutter. Es besteht kein Konsens über die beste Methode zur Verwaltung des Entzugs.
Wehen und Entbindung
Wie bei allen Betäubungsmitteln kann die Verabreichung dieses Produkts an die Mutter kurz vor der Entbindung zu einem gewissen Grad an Atemdepression beim Neugeborenen führen, insbesondere wenn höhere Dosen verwendet werden.
Stillende Mütter
Paracetamol wird in geringen Mengen in die Muttermilch ausgeschieden, aber die Bedeutung seiner Auswirkungen auf stillende Säuglinge ist nicht bekannt. Es ist nicht bekannt, ob Hydrocodon in die Muttermilch übergeht. Da viele Arzneimittel in die Muttermilch übergehen und aufgrund des Potenzials schwerwiegender Nebenwirkungen bei stillenden Säuglingen durch Hydrocodon und Paracetamol eine Entscheidung getroffen werden sollte, ob das Stillen abgebrochen oder das Arzneimittel abgesetzt werden soll, wobei die Bedeutung des Arzneimittels für die Mutter zu berücksichtigen ist.
Pädiatrische Anwendung
Sicherheit und Wirksamkeit bei pädiatrischen Patienten wurden nicht nachgewiesen.
Geriatrische Anwendung
Klinische Studien mit Hydrocodonbitartrat und Paracetamol-Tabletten umfassten keine ausreichende Anzahl von Probanden ab 65 Jahren, um festzustellen, ob sie anders reagieren als jüngere Probanden. Andere berichtete klinische Erfahrungen haben keine Unterschiede in den Reaktionen zwischen älteren und jüngeren Patienten festgestellt. Im Allgemeinen sollte die Dosisauswahl für einen älteren Patienten vorsichtig sein und normalerweise am unteren Ende des Dosierungsbereichs beginnen, was die größere Häufigkeit einer verminderten Leber-, Nieren- oder Herzfunktion sowie einer Begleiterkrankung oder einer anderen medikamentösen Therapie widerspiegelt.
Es ist bekannt, dass Hydrocodon und die Hauptmetaboliten von Paracetamol im Wesentlichen über die Niere ausgeschieden werden. Daher kann das Risiko toxischer Reaktionen bei Patienten mit eingeschränkter Nierenfunktion aufgrund der Akkumulation der Ausgangsverbindung und / oder Metaboliten im Plasma größer sein. Da ältere Patienten eher eine verminderte Nierenfunktion haben, sollte bei der Dosisauswahl Vorsicht walten gelassen werden, und es kann nützlich sein, die Nierenfunktion zu überwachen.Ältere Patienten sollten im Allgemeinen mit niedrigen Dosen von Hydrocodonbitartrat- und Paracetamol-Tabletten begonnen und engmaschig beobachtet werden.
Nebenwirkungen
Die am häufigsten berichteten Nebenwirkungen sind Benommenheit, Schwindel, Sedierung, Übelkeit und Erbrechen. Diese Effekte scheinen bei ambulanten Patienten ausgeprägter zu sein als bei nichtambulatorischen Patienten, und einige dieser Nebenwirkungen können gelindert werden, wenn sich der Patient hinlegt.
Andere Nebenwirkungen sind:
Zentralnervensystem
Schläfrigkeit, geistige Trübung, Lethargie, Beeinträchtigung der geistigen und körperlichen Leistungsfähigkeit, Angstzustände, Angstzustände, Dysphorie, psychische Abhängigkeit, Stimmungsschwankungen.
Magen-Darm-System
Eine längere Verabreichung von Hydrocodonbitartrat und Paracetamol-Tabletten kann zu Verstopfung führen.
Urogenitalsystem
Bei Opiaten wurde über Ureterspasmus, Spasmus der vesikalen Schließmuskeln und Harnverhalt berichtet.
Atemdepression
Hydrocodonbitartrat kann eine dosisabhängige Atemdepression hervorrufen, indem es direkt auf die Atemzentren des Hirnstamms einwirkt (siehe ÜBERDOSIERUNG).
Special Senses
Fälle von Schwerhörigkeit oder dauerhaftem Verlust wurden vorwiegend bei Patienten mit chronischer Überdosierung berichtet.
Dermatologisch
Hautausschlag, Pruritus.
Die folgenden unerwünschten Arzneimittelwirkungen können als mögliche Auswirkungen von Paracetamol berücksichtigt werden: allergische Reaktionen, Hautausschlag, Thrombozytopenie, Agranulozytose.
Mögliche Auswirkungen einer hohen Dosierung sind im Abschnitt ÜBERDOSIERUNG aufgeführt.
Drogenmissbrauch und -abhängigkeit
Kontrollierte Substanz
Hydrocone bitartrate and acetaminophen tablets is classified as a Schedule III controlled substance.
Missbrauch und Abhängigkeit
Psychische Abhängigkeit, körperliche Abhängigkeit und Toleranz können sich bei wiederholter Verabreichung von Betäubungsmitteln entwickeln; daher sollte dieses Produkt mit Vorsicht verschrieben und verabreicht werden. Es ist jedoch unwahrscheinlich, dass sich eine psychische Abhängigkeit entwickelt, wenn Hydrocodonbitartrat- und Paracetamol-Tabletten für kurze Zeit zur Behandlung von Schmerzen verwendet werden.
Körperliche Abhängigkeit, der Zustand, in dem die fortgesetzte Verabreichung des Arzneimittels erforderlich ist, um das Auftreten eines Entzugssyndroms zu verhindern, nimmt klinisch signifikante Anteile erst nach mehreren Wochen fortgesetzten Drogenkonsums an, obwohl sich nach einigen Tagen narkotischer Therapie ein leichter Grad an körperlicher Abhängigkeit entwickeln kann. Die Toleranz, bei der immer größere Dosen erforderlich sind, um den gleichen Grad an Analgesie zu erzeugen, äußert sich zunächst in einer verkürzten Dauer der analgetischen Wirkung und anschließend in einer Abnahme der Intensität der Analgesie. Die Rate der Toleranzentwicklung variiert zwischen den Patienten.
Überdosierung
Nach einer akuten Überdosierung kann die Toxizität von Hydrocodon oder Paracetamol resultieren.
Anzeichen und Symptome
Hydrocodon: Eine schwere Überdosierung mit Hydrocodon ist gekennzeichnet durch Atemdepression (Abnahme der Atemfrequenz und / oder des Atemzugvolumens, Cheyne-Stokes-Atmung, Zyanose), extreme Schläfrigkeit, die zu Stupor oder Koma führt, Schlaffheit der Skelettmuskulatur, kalte und feuchte Haut und manchmal Bradykardie und Hypotonie. Bei schwerer Überdosierung können Apnoe, Kreislaufkollaps, Herzstillstand und Tod auftreten.
Paracetamol: Bei Paracetamol-Überdosierung: Dosisabhängige, potenziell tödliche Lebernekrose ist die schwerwiegendste Nebenwirkung. Renale tubuläre Nekrose, hypoglykämisches Koma und Gerinnungsdefekte können ebenfalls auftreten.Frühe Symptome nach einer potenziell hepatotoxischen Überdosierung können sein: Übelkeit, Erbrechen, Diaphorese und allgemeines Unwohlsein. Klinische und laboratorische Hinweise auf eine Lebertoxizität sind möglicherweise erst 48 bis 72 Stunden nach der Einnahme ersichtlich.
Behandlung
Eine Einzel- oder Mehrfachüberdosis mit Hydrocodon und Paracetamol ist eine potenziell tödliche Polydrug-Überdosis, und die Konsultation eines regionalen Giftkontrollzentrums wird empfohlen.
Die sofortige Behandlung umfasst die Unterstützung der kardiorespiratorischen Funktion und Maßnahmen zur Verringerung der Arzneimittelabsorption.
Sauerstoff, intravenöse Flüssigkeiten, Vasopressoren und andere unterstützende Maßnahmen sollten wie angegeben angewendet werden. Eine assistierte oder kontrollierte Beatmung sollte ebenfalls in Betracht gezogen werden.
Bei einer Hydrocodon-Überdosierung sollte der Wiederherstellung eines angemessenen Atemaustauschs durch Bereitstellung eines patentierten Atemwegs und der Einrichtung einer unterstützten oder kontrollierten Beatmung besondere Aufmerksamkeit gewidmet werden. Der narkotische Antagonist Naloxonhydrochlorid ist ein spezifisches Gegenmittel gegen Atemdepression, die von Überdosierung oder ungewöhnliche Empfindlichkeit gegenüber Betäubungsmitteln, einschließlich Hydrocodon führen kann. Da die Wirkungsdauer von Hydrocodon die des Antagonisten überschreiten kann, sollte der Patient kontinuierlich überwacht werden, und wiederholte Dosen des Antagonisten sollten nach Bedarf verabreicht werden, um eine ausreichende Atmung aufrechtzuerhalten. Ein narkotischer Antagonist sollte nicht in Abwesenheit einer klinisch signifikanten respiratorischen oder kardiovaskulären Depression verabreicht werden.
Magen-Dekontamination mit Aktivkohle sollte kurz vor N-Acetylcystein (NAC) verabreicht werden, um die systemische Resorption zu verringern, wenn bekannt ist oder vermutet wird, dass die Einnahme von Paracetamol innerhalb weniger Stunden nach der Präsentation stattgefunden hat. Serum-Paracetamolspiegel sollten sofort erhalten werden, wenn der Patient 4 Stunden oder länger nach der Einnahme auftritt, um das potenzielle Risiko einer Hepatotoxizität zu beurteilen; Paracetamolspiegel, die weniger als 4 Stunden nach der Einnahme gezogen werden, können irreführend sein. Um das bestmögliche Ergebnis zu erzielen, sollte NAC so bald wie möglich verabreicht werden, wenn eine drohende oder sich entwickelnde Leberschädigung vermutet wird. Intravenöse NAC kann verabreicht werden, wenn die Umstände eine orale Verabreichung ausschließen.
Bei schwerer Intoxikation ist eine kräftige unterstützende Therapie erforderlich. Verfahren zur Begrenzung der anhaltenden Resorption des Arzneimittels müssen leicht durchgeführt werden, da die Leberverletzung dosisabhängig ist und früh im Verlauf der Intoxikation auftritt.
Vicodin ES Dosierung und Verabreichung
Die Dosierung sollte entsprechend der Schwere der Schmerzen und der Reaktion des Patienten angepasst werden. Es sollte jedoch beachtet werden, dass sich bei fortgesetzter Anwendung eine Toleranz gegenüber Hydrocodon entwickeln kann und dass das Auftreten unerwünschter Wirkungen dosisabhängig ist.
VICODIN® (Hydrocodonbitartrat- und Acetaminophentabletten, USP 5 mg / 300 mg): Die übliche Dosierung für Erwachsene beträgt eine oder zwei Tabletten alle vier bis sechs Stunden, je nach Bedarf bei Schmerzen. Die tägliche Gesamtdosis sollte 8 Tabletten nicht überschreiten.
Vicodin ES® (Hydrocodonbitartrat- und Acetaminophentabletten, USP 7,5 mg / 300 mg): Die übliche Dosierung für Erwachsene beträgt eine Tablette alle vier bis sechs Stunden, je nach Bedarf bei Schmerzen. Die tägliche Gesamtdosis sollte 6 Tabletten nicht überschreiten.
VICODIN HP® (Hydrocodonbitartrat- und Acetaminophentabletten, USP 10 mg / 300 mg): Die übliche Dosierung für Erwachsene beträgt eine Tablette alle vier bis sechs Stunden, je nach Bedarf bei Schmerzen. Die tägliche Gesamtdosis sollte 6 Tabletten nicht überschreiten.
Wie wird Vicodin ES geliefert
VICODIN®, Vicodin ES® und VICODIN HP® (Hydrocodonbitartrat und Acetaminophen) Tabletten, USP werden wie folgt geliefert:
VICODIN® 5 mg / 300 mg
Weiße, kapselförmige, halbierte Tabletten mit der Prägung „5“ / „300“auf einer Seite und „VICODIN“ auf der anderen Seite in Flaschen mit 100 und 500 Tabletten:
Flaschen mit 100 – NDC 0074-3041-13
Flaschen mit 500 – NDC 0074-3041-53
Vicodin ES® 7,5 mg/300 mg
Weiße, kapselförmige, halbierte Tabletten mit der Prägung „7.5“ score „300“ auf der einen Seite und „Vicodin ES“ auf der anderen Seite in Flaschen mit 100 und 500 Tabletten:
Flaschen mit 100 – NDC 0074-3043-13
Flaschen mit 500 – NDC 0074-3043-53
VICODIN HP® 10 mg/300 mg
Weiße, kapselförmige, halbierte Tabletten, Prägung „10“ und „300“ auf der einen Seite und „VICODIN HP“ auf der anderen Seite in Flaschen mit 100 und 500 Tabletten:
Flaschen mit 100 – NDC 0074-3054-13
Flaschen mit 500 – NDC 0074-3054-53
LAGERUNG
Bei 20 ° bis 25 ° C (68 ° bis 77°F). .
APOTHEKER: In einen dichten, lichtbeständigen Behälter mit kindersicherem Verschluss geben.
Ein Narkotikum gemäß Anhang III
© AbbVie Inc. 2014
Hergestellt für
AbbVie Inc.
North Chicago, IL 60064 U.S.A.
Hergestellt von:
Mikart, Inc.
Atlanta, GA 30318
1122F00 Rev. 06/14 June, 2014
NDC 0074–3054–53
Vicodin HP® (Hydrocodone Bitartrate and Acetaminophen) Tablets, USP
CIII
10 mg / 300 mg
500 Tablets
Rx only abbvie

NDC 0074–3043–13
Vicodin ES® (Hydrocodone Bitartrate and Acetaminophen) Tablets, USP
CIII
7.5 mg / 300 mg
100 Tablets
Rx only abbvie

NDC 0074–3041–13
Vicodin® (Hydrocodone Bitartrate and Acetaminophen) Tablets, USP
CIII
5 mg / 300 mg
100 Tablets
Rx only abbvie

| VICODIN HP hydrocodone bitartrate and acetaminophen tablet |
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
| Vicodin ES hydrocodone bitartrate and acetaminophen tablet |
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
| VICODIN hydrocodone bitartrate and acetaminophen tablet |
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
Labeler – AbbVie Inc. (078458370)
More about Vicodin ES (acetaminophen / hydrocodone)
- Side Effects
- During Pregnancy
- Dosage Information
- Drug Images
- Drug Interactions
- 15 Reviews
- Drug class: narcotic analgesic combinations
- FDA Alerts (11)
Professional resources
- Prescribing Information
Other brands Norco, Vicodin, Lortab, Hycet, … +13 mehr
Verwandte Behandlungsleitfäden
- Rückenschmerzen
- Husten
- Schmerzen
- Rheumatoide Arthritis
Medizinischer Haftungsausschluss