Vitamin C: Ein Antioxidans
Redoxstoffwechsel und antioxidative Eigenschaften von Vitamin C
Freie Radikale und Oxidationsmittel spielen eine doppelte Rolle als toxische und nützliche Verbindungen, in Stoffwechselprozessen und als Reaktion auf exogene Stimulationen. Sie entstehen entweder durch normale Stoffwechselaktivitäten oder durch Umweltfaktoren (Umweltverschmutzung, Zigarettenrauch und Strahlung). Wenn eine Überlastung freier Radikale nicht abgefangen werden kann, erzeugt ihre Ansammlung im Körper oxidativen Stress . Oxidativer Stress tritt auf, wenn die Bildung freier Radikale die Fähigkeit des Schutzes gegen sie übersteigt. Dieser Prozess führt zur Entwicklung chronischer und degenerativer Erkrankungen wie Krebs, Autoimmunerkrankungen, Alterung, Katarakt, rheumatoider Arthritis, Herz-Kreislauf- und neurodegenerativen Erkrankungen . Ein Antioxidans ist ein Molekül, das die Oxidation anderer Moleküle verhindert. Oxidationsprozess ist eine chemische Reaktion, die freie Radikale erzeugt, was zu Kettenreaktionen führt, die Zellen schädigen können. Die antioxidative Wirkung von Vitamin C ist gut dokumentiert . Vitamin C ist ein starkes Antioxidans mit der Fähigkeit, ein Wasserstoffatom zu spenden und ein relativ stabiles Ascorbyl-freies Radikal zu bilden. Vitamin E, Vitamin C und β-Carotin sind als antioxidative Vitamine bekannt, die oxidative Schäden verringern und das Risiko bestimmter chronischer Krankheiten senken sollen. Krankheiten wie Herz-Kreislauf-Erkrankungen sind in epidemiologischen Studien mit unzureichenden Konzentrationen von l-Ascorbinsäure, Tocopherol und β-Carotin verbunden. Vitamin C verbessert auch die Eisenaufnahme, indem es Fe3 + zu Fe2 + aus Nicht-Häm-Eisenquellen reduziert. In Gegenwart von redoxaktiven Ionen (Eisen, Kupfer) wirkt Vitamin C als Prooxidans und trägt zur Bildung von Hydroxylradikalen bei, die zu einer Oxidation von Lipiden, DNA oder Proteinen führen können . Es gibt verschiedene Mechanismen, um oxidativen Stress abzubauen und beschädigte Makromoleküle zu reparieren. Enzymatische und nichtenzymatische Antioxidantien spielen eine wichtige Rolle beim Abfangen freier Radikale und reaktiver Sauerstoffspezies (ROS). Es wurde gezeigt, dass die antioxidativen Enzyme Katalase (CAT), Superoxiddismutase (SOD), Glutathionreduktase (GR), Glutathionperoxidase (GSHpx) und in Pflanzen Ascorbatperoxidase (AA-px) und die nichtenzymatischen Antioxidantien, einschließlich Glutathion (GSH) und Ascorbat (ASC), signifikant durch oxidativen Stress beeinflusst werden . Antioxidative Verbindungen können die unkontrollierte Bildung von freien Radikalen verhindern oder ihre Reaktion mit biologischen Stellen hemmen; Die Zerstörung der meisten freien Radikale hängt auch von der Oxidation endogener Antioxidantien ab, hauptsächlich durch Auffangen und Reduzieren von Molekülen . Es wird angenommen, dass Vitamin C ein wichtiges wasserlösliches Antioxidans ist, von dem berichtet wird, dass es ROS neutralisiert und oxidativen Stress reduziert .
Vitamin C ist ein starkes Reduktionsmittel und Fänger von freien Radikalen in biologischen Systemen . Es ist an der ersten Linie der antioxidativen Abwehr beteiligt und schützt Lipidmembranen und Proteine vor oxidativen Schäden. Als wasserlösliches Molekül kann Vitamin C sowohl innerhalb als auch außerhalb der Zellen wirken und freie Radikale neutralisieren und Schäden durch freie Radikale verhindern. Vitamin C ist eine ausgezeichnete Elektronenquelle für freie Radikale, die ein Elektron suchen, um ihre Stabilität wiederzugewinnen. Vitamin C kann Elektronen an freie Radikale abgeben und deren Reaktivität stillen .
Vitamin C hat sich als wirksamer Fänger gegen Sauerstoff- und Stickoxidspezies wie Superoxidradikali, Wasserstoffperoxid, Hydroxylradikal und Singulettsauerstoff erwiesen. Diese Eigenschaft von Vitamin C hat lebenswichtige Prozesse zum Schutz der zellulären Komponenten vor Schäden durch freie Radikale. Darüber hinaus regeneriert Vitamin C wirksam die antioxidative Form von Vitamin E, indem es Tocopheroxylradikale reduziert. Dieser Prozess schützt Membranen und andere Kompartimente der Zelle vor Schäden durch freie Radikale (Abbildung 2). Ascorbatperoxidase (APX) ist ein Enzym, das H2O2 zu Wasser reduziert, indem Ascorbat als Elektronendonor verwendet wird. Monodehydroascorbat ist ein oxidiertes Ascorbat, das durch Monodehydroascorbatreduktase (MDAR) regeneriert wird. Monodehydroascorbatradikal disproportioniert schnell in Ascorbat und Dehydroascorbat. Dehydroascorbate is reduced to ascorbate by dehydroascorbate reductase in the presence of GSH, yielding oxidized glutathione (GSSG). It is reduced by glutathione reductase (GR) using nicotinamide adenine dinucleotide phosphate hydrogen (NADPH) as an electron donor. Dehydroascorbate may be reduced nonenzymatically or catalyzed by proteins with dehydroascorbate reductase (DHAR) activity.
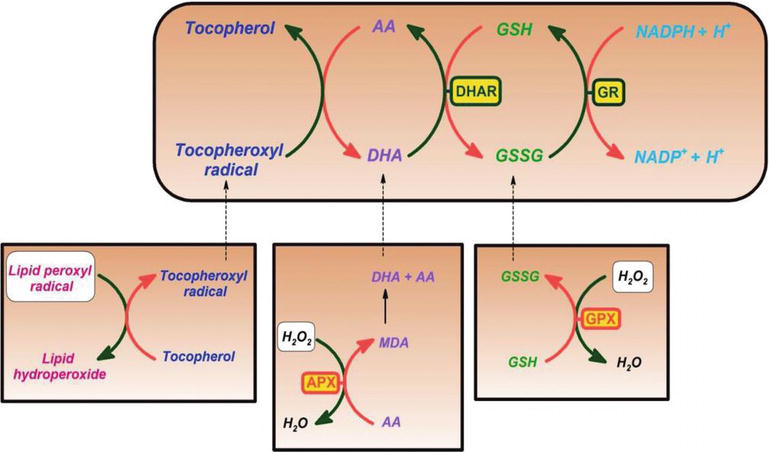
Figure 2.
xmlns:mml=“http://www.w3.org/1998/Math/MathML“ xmlns:xlink=“http://www.w3.org/1999/xlink“ xmlns:xsi=“http://www.w3.org/2001/XMLSchema-instanceAscorbate and redox cycling antioxidants. AA, ascorbate; DHA, dehydroascorbate; DHAR, semidehydroascorbate reductase; GSH, glutathione; GSSG, semi-glutathione reductase; GR, glutathione reductase; APX, ascorbate peroxidase; and GPX, glutathione peroxidase .
Glutathione-ascorbate cycle operates in the cytosol, mitochondria, plastids, and peroxisomes in plants . Es wird vermutet, dass der Glutathion-Ascorbat-Zyklus aufgrund der hohen Konzentrationen von Glutathion, Ascorbat und NADPH in Pflanzenzellen eine Schlüsselrolle für die H2O2-Entgiftung spielt. Andere Enzyme wie Ascorbat- und Glutathionperoxidasen, die Thioredoxine oder Glutaredoxine als reduzierende Substrate verwenden, spielen ebenfalls eine Rolle bei der Entfernung von H2O2 in Pflanzen (Abbildung 2).
Vitamin C bildet auch das Semidehydroascorbylradikal, ein relativ langlebiges Radikal, bei der Regeneration von Vitamin E aus seiner Radikalform sowie beim Radikalfänger. Pflanzliche und tierische Zellen enthalten ein NADH-abhängiges Semidehydroascorbat-Reduktase-Enzym (EC 1.6.5.4), das das Radikal zurück zu Vitamin C reduziert, indem NADH als Quelle für Reduktionsmittel verwendet wird (Abbildung 2). Es kann sowohl enzymatisch als auch nichtenzymatisch irreversibel in Diketogluconsäure zerfallen oder in einer glutathionabhängigen Reaktion in Ascorbat umgewandelt werden .Als reduzierende Substanz und Elektronendonor spendet Vitamin C beim Radikalfänger hochenergetische Elektronen, um freie Radikale zu neutralisieren, und es wird zu Dehydroascorbinsäure oxidiert. Dehydroascorbinsäure kann zur Wiederverwendung wieder in Ascorbinsäure umgewandelt oder metabolisiert werden, wodurch weitere Elektronen freigesetzt werden. Obwohl Vitamin C über einen natriumabhängigen Vitamin-C-Transporter aus dem Darm aufgenommen wird, transportieren die meisten Zellen Vitamin C in oxidierter Form (Dehydroascorbinsäure) über den Glucosetransporter 1. Dehydroascorbinsäure wird reduziert, um Ascorbinsäure in der Zelle zu erzeugen und die Mitochondrien vor oxidativen Schäden durch freie Radikale zu schützen (Abbildungen 2 und 3). Hochreaktive freie Radikale (z.B., RO-, RO2-, OH-,, NO2) werden durch Ascorbat reduziert, und der neu erzeugte Ascorbylrest ist schlecht reaktiv. Ascorbat kann auch nichtradikale reaktive Spezies abfangen, die von Peroxynitrit abgeleitet sind, wie hypochlorige Säure, Ozon und Nitriermittel. Vitamin C ist ein Monosaccharid-Oxidations-Reduktions-Katalysator (Redox-Katalysator), der sowohl in Tieren als auch in Pflanzen vorkommt. Die antioxidative Wirkung von Vitamin C beruht auf seiner Fähigkeit, Elektronen sowohl aus dem zweiten als auch aus dem dritten Kohlenstoff abzugeben. Während der Primatenevolution ist eines der Enzyme, die zur Herstellung von Ascorbinsäure benötigt werden, durch Mutation verloren gegangen, Menschen müssen es aus der Nahrung beziehen ; Die meisten Tiere können dieses Vitamin in ihrem Körper synthetisieren und benötigen es nicht in ihrer Ernährung . Vitamin C wird bei der Umwandlung des Prokollagens in Kollagen durch Oxidation von Prolinresten zu Hydroxyprolin benötigt. In anderen Zellen wird es durch Reaktion mit Glutathion in seiner reduzierten Form erhalten . Wie in den Abbildungen 2 und 3 gezeigt, ist Ascorbinsäure ein Redoxkatalysator, der ROS wie Wasserstoffperoxid (H2O2) reduzieren und dadurch neutralisieren kann (Abbildungen 2 und 3).
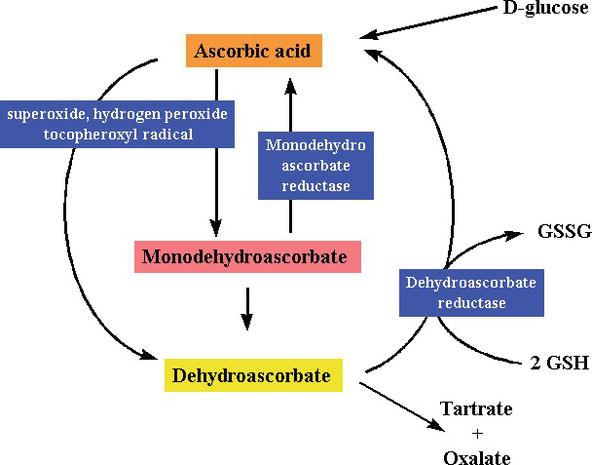
Figure 3.
xmlns:mml=“http://www.w3.org/1998/Math/MathML“ xmlns:xlink=“http://www.w3.org/1999/xlink“ xmlns:xsi=“http://www.w3.org/2001/XMLSchema-instanceSynthesis and degradation ofl-ascorbic acid in plant tissues .
Ascorbic acid has direct antioxidant effects, and also it is a substrate for the redox enzyme ascorbate peroxidase, that is particularly important in stress resistance in plants. Ascorbinsäure ist in allen Pflanzenteilen in hohen Konzentrationen vorhanden, insbesondere in Chloroplasten, die dort Konzentrationen von 20 mm erreichen . Dehydroascorbat (DHA) und freies Ascorbatradikal (AFR), als Zwischenprodukt, das freie Ascorbatradikal (AFR), die reversible Ein-Elektronen-Oxidationen sind, werden aus Ascorbat erzeugt (Abbildung 4). Gemäß dem allgemein angenommenen Modell der enzymatischen Entfernung von ROS katalysiert SOD Superoxidanion zu H2O2 und Sauerstoff; dann wird H2O2 durch CAT zu Wasser und molekularem Sauerstoff reduziert. CAT turnover number is very high, but its affinity for H2O2 is relatively low, and consequently a certain amount of H2O2 remains in the cell.
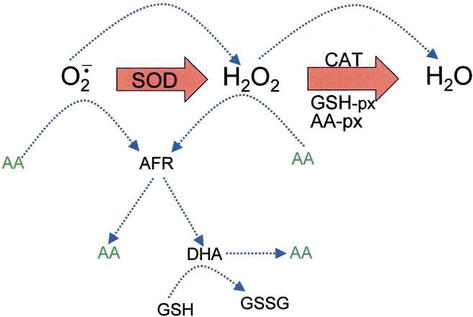
Figure 4.
xmlns:mml=“http://www.w3.org/1998/Math/MathML“ xmlns:xlink=“http://www.w3.org/1999/xlink“ xmlns:xsi=“http://www.w3.org/2001/XMLSchema-instanceThe role of AA in the detoxification of ROS. Blue dotted lines indicate nonenzymatic reactions.
H2O2 can react with superoxide anion formed in oxidative metabolism generating the highly reactive hydroxyl radical. GSH peroxidases (GSH-px) and AA peroxidases (AA-px) are capable of scavenging H2O2 due to their high affinity for H2O2. The cooperativity of SOD, CAT, and peroxidases ensures low amounts of superoxide anion and H2O2 and limiting the risk of hydroxyl radical formation (Figure 5).

Figure 5.
xmlns:mml=“http://www.w3.org/1998/Math/MathML“ xmlns:xlink=“http://www.w3.org/1999/xlink“ xmlns:xsi=“http://www.w3.org/2001/XMLSchema-instanceFoyer-Halliwell-Asada cycle .