L’Osimertinib Améliore la survie dans le Cancer du Poumon Avancé avec Mutations EGFR
12 décembre 2019 par le personnel du NCI
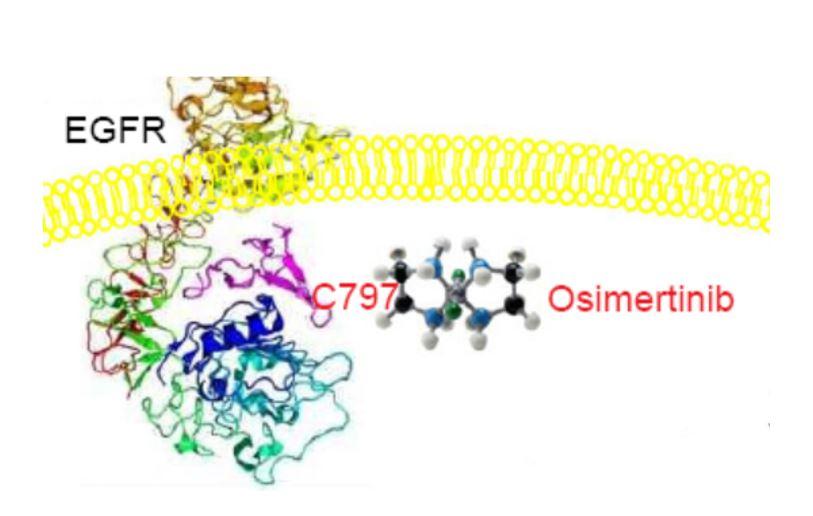
L’Osimertinib se lie à des formes mutées spécifiques de protéines EGFR, dont une appelée T790M qui est liée à une résistance à d’autres médicaments ciblés par l’EGFR.
Les premiers traitements ciblant les formes mutées de la protéine EGFR ont été approuvés pour une utilisation chez les personnes atteintes d’un cancer du poumon non à petites cellules (CPNPC) il y a plus de 15 ans. Les résultats mis à jour d’un vaste essai clinique montrent maintenant que l’un des médicaments les plus récents ciblant l’EGFR, l’osimertinib (Tagrisso), est plus efficace que les thérapies antérieures ciblant l’EGFR chez les personnes dont les tumeurs du CPNPC présentent des altérations spécifiques du gène EGFR.
Dans l’essai baptisé FLAURA, les patients atteints d’un CPNPC avancé ayant reçu l’osimertinib en tant que traitement initial ont vécu environ 7 mois de plus que les patients traités par erlotinib (Tarceva) ou gefinitib (Iressa). Et l’amélioration de la survie ne s’est pas faite au prix de la sécurité; les enquêteurs n’ont constaté aucune augmentation des effets secondaires graves chez les personnes traitées avec de l’osimertinib.
Les résultats de survie globale de l’essai ont été initialement présentés fin septembre lors de la réunion annuelle de la Société Européenne d’Oncologie médicale (ESMO) à Barcelone et ont été publiés le 21 novembre dans le New England Journal of Medicine.
L’Osimertinib a été approuvé par la Food and Drug Administration (FDA) en 2018 en tant que traitement initial ou de première intention pour les personnes atteintes d’un CPNPC avancé présentant des mutations spécifiques de l’EGFR. L’approbation était basée sur des résultats antérieurs de l’essai FLAURA montrant que le médicament améliorait la durée de vie des personnes sans que leur cancer ne s’aggrave (survie sans progression).
La conclusion selon laquelle l’osimertinib améliore également la durée de vie globale des patients renforce encore son rôle dans le traitement, a déclaré le chercheur principal de l’essai FLAURA, Suresh Ramalingam, MD, de l’Institut du cancer Winship de l’Université Emory à Atlanta.
Chez les patients atteints d’un CPNPC avancé dont les tumeurs présentent des mutations de l’EGFR, le Dr Ramalingam a déclaré: « L’osimertinib est maintenant la norme de soins pour le traitement de première intention. »
Leora Horn, MD, directrice clinique du programme d’oncologie thoracique au Vanderbilt-Ingram Cancer Center dans le Tennessee, est d’accord. Les résultats de FLAURA « nous disent que c’est certainement le médicament que vous devriez utiliser en premier » pour ces patients, a déclaré le Dr Horn.
Amélioration par rapport à la génération précédente de médicaments ciblés par l’EGFR
Le cancer du poumon non à petites cellules est le type de cancer du poumon le plus courant. Bien que les mutations EGFR soient relativement courantes dans le CPNPC avancé, leur fréquence varie considérablement selon l’ethnicité et la région géographique, a expliqué Pilar Garrido, MD, Ph.D., qui se spécialise dans le traitement du cancer du poumon à l’Université d’Alcalá en Espagne.
Dans les populations européennes et caucasiennes, les mutations surviennent chez 10% à 15% des patients atteints d’un CPNPC avancé. Mais ils sont présents chez près de 40% des patients dans certains pays asiatiques, a déclaré le Dr Garrido lors d’un point de presse sur les résultats de FLAURA lors de la réunion de l’ESMO.
Le gefitinib et l’erlotinib ont été les deux premiers traitements ciblés par l’EGFR à être approuvés par la FDA pour traiter le cancer du poumon. Peu de temps après ces approbations, une série d’études ont montré que les médicaments n’étaient efficaces que chez les patients dont les tumeurs présentaient des mutations « activatrices » spécifiques du gène EGFR, c’est—à-dire des mutations qui peuvent maintenir le gène constamment activé, alimentant la croissance du cancer.
L’Osimertinib agit contre les tumeurs présentant les mêmes mutations activant l’EGFR (appelées délétions de l’exon 19 et exon 21 L858R) ciblées par les autres médicaments ciblés par l’EGFR. Cependant, il a également été conçu pour cibler spécifiquement les cellules tumorales avec une mutation EGFR connue sous le nom de T790M, qui a été démontrée pour provoquer une résistance aux thérapies ciblées par EGFR de génération précédente.
Il est important, a expliqué le Dr Horn, que l’osimertinib semble également être plus efficace que les autres inhibiteurs de l’EGFR dans le cancer du poumon qui s’est propagé au système nerveux central (SNC), principalement au cerveau. « Pour de nombreux patients, le premier site de progression peut être le SNC », a-t-elle déclaré.
Premier essai à Montrer une Meilleure Survie globale
L’approbation de l’osimertinib par la FDA en 2018 n’en était pas la première. Il a été initialement approuvé en 2015 pour une utilisation chez certaines personnes atteintes d’un CPNPC dont le cancer est revenu après avoir reçu l’une des autres thérapies ciblées par l’EGFR. L’essai FLAURA a été lancé pour déterminer si l’osimertinib était plus efficace en tant que traitement initial que les inhibiteurs de l’EGFR de génération antérieure.
Plus de 550 patients ont été inscrits à l’essai, financé par AstraZeneca, le fabricant de l’osimertinib. Tous les patients de l’essai avaient récemment diagnostiqué un CPNPC avancé avec des mutations activant l’EGFR et ont été assignés au hasard pour recevoir l’osimertinib ou le choix de leur médecin, soit le gefitinib, soit l’erlotinib.
Chez les participants du groupe traité par l’osimertinib, la survie globale médiane était de 38,6 mois, comparativement à 31,8 mois dans le groupe erlotinib/gefitinib. Trois ans après le début du traitement, 28% des patients affectés à l’osimertinib prenaient toujours le médicament — ce qui signifie que leur cancer y répondait toujours — contre environ 9% des patients du groupe gefitinib / erlotinib.
Reflétant l’agressivité du CPNPC avancé, 30% des patients de l’essai dont le cancer a progressé n’ont pas subi de traitement supplémentaire avec un autre traitement, le plus souvent parce qu’ils sont décédés rapidement après la progression de leur cancer.
Cependant, pour les personnes du groupe témoin qui pourraient recevoir un autre traitement après la progression de leur cancer, près de la moitié ont reçu de l’osimertinib, souvent appelé traitement « croisé ». »
La survie médiane de près de 32 mois dans le groupe erlotinib / gefitinib « est parmi les plus rapportées » chez les patients initialement traités par l’un ou l’autre de ces médicaments, a noté le Dr Ramalingam, ce qu’il a attribué au grand nombre de ces patients qui ont ensuite reçu de l’osimertinib.
Compte tenu du taux de croisement élevé, il est particulièrement remarquable que l’osimertinib ait pu améliorer la survie globale, a-t-il déclaré.
Les taux d’effets secondaires graves étaient similaires entre les deux groupes de traitement. Un plus grand nombre de patients traités par l’osimertinib ont présenté des problèmes cardiaques, y compris un problème appelé allongement de l’intervalle QT qui peut causer des problèmes de rythme cardiaque. Une inflammation des poumons, ou pneumopathie, un problème observé dans des essais antérieurs avec l’osimertinib, n’est survenue que chez quelques patients.
Au total, 15% des patients du groupe osimertinib ont cessé de prendre le médicament en raison d’effets secondaires, contre 18% dans le groupe erlotinib / gefitinib.
Dans les soins de tous les jours, a déclaré le Dr Horn, les patients tolèrent assez bien l’osimertinib et sont moins susceptibles de ressentir des effets secondaires tels que des éruptions cutanées sévères et des diarrhées couramment observées avec les autres médicaments ciblés par l’EGFR.
L’importance des tests moléculaires
L’amélioration de la survie observée avec l’osimertinib, combinée à sa sécurité relative, « est une bonne nouvelle pour les patients », a déclaré le Dr Garrido.
Elle a cependant souligné que l’utilisation par les cliniciens des tests moléculaires pour identifier les patients candidats à une thérapie ciblée fait toujours défaut. Ces tests ont été entravés en partie par ce que l’on appelle souvent le nihilisme thérapeutique, c’est—à-dire la conviction que les tests ne produiront aucun bénéfice pour les patients.
Bien que ce nihilisme ait quelque peu diminué chez les cliniciens qui traitent le cancer du poumon, a déclaré le Dr Ramalingam, il existe toujours. « Seul un sous-ensemble de patients subit des tests. »
Dans les cas où des tests sont effectués mais qu’il y a un retard dans l’obtention des résultats, les cliniciens commenceront souvent à administrer d’autres traitements, a déclaré le Dr Horn. De plus en plus, ce traitement est une chimiothérapie associée à des inhibiteurs de points de contrôle immunitaires.
Bien que ces médicaments d’immunothérapie puissent être efficaces chez les personnes atteintes d’un cancer du poumon avancé, a-t-elle ajouté, ils agissent rarement dans les tumeurs présentant des mutations de l’EGFR. Les inhibiteurs de point de contrôle augmentent également considérablement le risque de pneumopathie, a-t-elle poursuivi, de sorte qu’une fois qu’ils sont administrés, la possibilité d’utiliser l’osimertinib peut être perdue.
« Donc, si vous sentez que vous devez commencer le traitement, commencez par la chimio et laissez de côté l’immunothérapie jusqu’à ce que vous connaissiez l’état moléculaire du patient », a-t-elle déclaré.
Un message essentiel pour les cliniciens traitant des patients atteints d’un cancer du poumon avancé, a-t-elle souligné, est qu’ils doivent commander des tests moléculaires, « et attendre le résultat jusqu’à ce que vous commenciez le traitement. »