7.18: vinil-halogenidek és Aril-halogenidek
nukleofil szubsztitúció az aril-halogenidekben
részletesen megvizsgáljuk a klórbenzol szerkezetét. A bróm-benzol és a jodobenzol ugyanaz. A klórbenzol szerkezetének legegyszerűbb módja:
a klórbenzol megfelelő megértéséhez meg kell ásni a klórbenzolt egy kicsit mélyebbre, mint ez. Kölcsönhatás van a benzolgyűrű delokalizált elektronjai és a klóratom egyik magányos párja között. Ez átfedésben van a delokalizált gyűrűelektron rendszerrel . . .
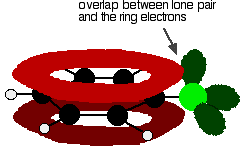
hogy egy ilyen struktúrát adjunk meg:
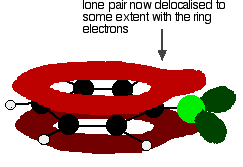
ez a delokalizáció korántsem teljes, de jelentős hatással van mind a szén-klór tulajdonságaira a kötés és a molekula polaritása. A delokalizáció némi extra kötést hoz létre a szén és a klór között, ami erősebbé teszi a kötést. Ez jelentős hatással van a vegyületek, például a klórbenzol reakcióira.
az elektronok is elmozdulnak a klórtól a gyűrű felé. A klór meglehetősen elektronegatív, és általában magához vonzza a szén-klór kötésben lévő elektronokat. Ebben az esetben ezt bizonyos mértékben ellensúlyozza az elektronok mozgása a delokalizáció során a gyűrű felé. A molekula kevésbé poláris, mint amire egyébként számíthatott volna.
az egyszerű aril-halogenidek, mint például a klórbenzol, nagyon rezisztensek a nukleofil szubsztitúcióval szemben. A klórt-OH-val lehet helyettesíteni, de csak nagyon súlyos ipari körülmények között – például 200 C és 200 atmoszféra esetén. A laborban ezek a reakciók nem fordulnak elő. Ennek két oka van – attól függően, hogy a fenti mechanizmusok közül melyikről beszél.
- a szén-halogén kötés extra szilárdsága az aril-halogenidekben: a szén-klór kötés a klórbenzolban erősebb, mint amire számíthat. Kölcsönhatás van a klóratom egyik magányos párja és a delokalizált gyűrűelektronok között, és ez erősíti a kötést. Mindkét fenti mechanizmus magában foglalja a szén-halogén kötés megszakítását egy bizonyos szakaszban. Minél nehezebb megtörni, annál lassabb lesz a reakció.
- A gyűrűelektronok taszítása: ez csak akkor érvényes, ha a hidroxidion a fent leírt első mechanizmushoz hasonló mechanizmussal támadta meg a klórbenzolt. Ebben a mechanizmusban a hidroxidion megtámadja azt a kissé pozitív szenet, amelyhez a halogénatom kapcsolódik.Ha a halogénatom egy benzolgyűrűhöz kapcsolódik, akkor a bejövő hidroxidion a szénatom felett és alatt lévő delokalizált gyűrűelektronokkal szembesül. A negatív hidroxid-ion egyszerűen visszaszorul. Ez a bizonyos mechanizmus egyszerűen nem indító!