határok a Cardiovascular Medicine-ben
Bevezetés
a különböző biológiai entitásokra alkalmazható koordináta-rendszerek vizsgálatakor figyelembe kell venni a sajátos jellemzőket. Például a kromoszómaszám és a bázispár pozíciója egy lineáris koordináta-rendszert alkot, amely elegendő a referencia genomban való hely meghatározásához (1). Azonban egy koordináta-rendszer az egész emberi test számára, amely képes kiszolgálni a hubmap, HCA, HPA és más feltérképezési erőfeszítések igényeit, több okból is sokkal összetettebb (2-5). Először is, a sejtek három dimenzióban élnek; és további információkra van szükség az adatok előállításához használt szövetminták méretének és forgásorientációjának leírásához. Másodszor, míg a genom bázispár pozíciója nem függ attól, hogy a DNS hogyan van hajtva és csomagolva a magba, az egyes elemek helyzete (pl., sejtek, szervek) a testen belül dinamikusak, mivel megváltozhatnak a csontváz és az izommozgások, a gravitáció, a légzés, a szívverés és más funkciók és erők, amelyek torzítják a szöveteket. Harmadszor, bár a DNS variabilitása az emberek között <1%, az emberi test geometriája a magasságok, súlyok és formák széles skáláját öleli fel, amelyek nemenként és fajonként változnak, és jelentősen megváltoznak az ember élettartama alatt.
az egyik lehetőség egy 3D derékszögű koordinátarendszer használata a testen belüli helyzet leírására. A derékszögű koordináta-rendszerek előnye, hogy ismerősek és könnyen érthetők. A test normál anatómiai helyzetében a bal-jobb, a caudalis-cranialis és a hátsó-elülső három merőleges (x-y-z) tengelyt képez. Kisebb léptékű elemzéseknél az eredet anatómiai iránypontra való összpontosítása lehet a leghasznosabb és potenciálisan kevésbé változó a különböző emberek között. Például könnyebb lenne megmérni a szövetminta távolságát a vesétől a vese felső pólusáig, mint az ember fejének tetejéig. A derékszögű koordináták hátránya, hogy tengelyei nem követik a test természetes alakját. Ennek eredményeként egy referenciatest-térkép létrehozása a különböző méretű emberektől gyűjtött szövetminták digitális “összefűzésével” összetett folyamatot igényelne az adatok vetemedésével, forgatásával és összehangolásával. Rendkívül nehéz lenne ezt úgy megtenni, hogy az egész testre kiterjedjen, miközben megőrzi a sejtszintű pontosságot.
Egyéb 3D koordináta-rendszereket fejlesztettek ki különböző alkalmazásokhoz. Például a gömb alakú koordináták, amelyek tengelyei a szélességet, a hosszúságot és a magasságot képviselik, kényelmesen leírják a Föld felszínén lévő helyet. A gömb alakú koordináták egyszerű útját, például az “1 km-re keletre”, sokkal nehezebb kommunikálni derékszögű koordinátákkal. Hasonlóképpen, az emberi test koordináta-rendszereinek ideális esetben olyan tengelyekkel kell rendelkezniük, amelyek anatómiai struktúrákat, genetikai expressziós mintákat, kémiai gradienseket és/vagy más biológiailag releváns útvonalakat követnek. Számos szervspecifikus koordináta-rendszert fejlesztettek ki, például a talairach koordinátákat a funkcionális agyi képalkotáshoz, de ezek nem terjednek ki az egész testre (6).
vaszkuláris alapú koordináta-rendszer
2017-ben közös koordináta-keret (CCF) találkozót szervezett a Nemzeti Egészségügyi Intézetek, a Broad Intézet, a Sanger Intézet és a Chan Zuckerberg kezdeményezés. A találkozó résztvevői, köztük anatómusok, patológusok, klinikusok és technológiai szakértők a világ minden tájáról, számos megközelítést javasoltak az emberi test sejtjeinek feltérképezésére, beleértve az anatómiai alapú koordináta-rendszereket (7). Ezek egyikét, amely az érrendszert használja, tovább tárgyalták egy 2019-es CCF Műhelyben, kifejezetten a vesesejtek lokalizálására (8). Ebben a kéziratban ennek a vaszkuláris alapú koordináta-rendszernek a fogalmi áttekintését mutatjuk be, és ismertetjük annak előnyeit és korlátait (1.ábra).
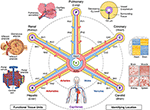
1. ábra. Az érrendszer koordináta-rendszerének hub-and-spoke szerkezete. A vaszkuláris koordináta-rendszer reprezentatív érhurkokból áll, amelyek a szív kamráiban kezdődnek és végződnek, és kiterjednek az egyes szervek funkcionális egységeire (az óramutató járásával ellentétes irányban a bal felsőtől: alveolusok, glomerulusok és máj lobulák). A sejt ” címe “tartalmazza a hurok nevét (pl.” r “a vesére és” H “a májra) és a legközelebbi ér elágazási szintjét (pl.” RA1 ” az afferens arteriolák esetében a vese hurokban). Megjegyezzük, hogy a szív falai a szívkoszorúér (“C”) vaszkuláris hurok mentén fekszenek, és a szív belsejében lévő egyes struktúrák sejtjei valójában a koordináta-rendszer perifériáján helyezkednek el, a kapillárisok közelében, amelyek vérrel látják el őket. Többféle módon lehet még pontosabb “GPS-szerű” pozíciót meghatározni, beleértve a jobb felső óramutató járásával megegyező irányba haladva a “hipoxia ujjlenyomatot”, amely az értől távolabb eső oxigénszint csökkenéséből származik, az egyedi” szövettani ujjlenyomatot “és a” gén expressziós ujjlenyomatot “a különböző típusú vaszkuláris endothel sejtekben, valamint a különböző típusú szövetekben található jellegzetes” vaszkuláris architektúra ujjlenyomatot”. Az érrendszer kiterjed a test minden részére (alul), és minden szervet keretez. Forrás Fájlok: A máj lobuláinak, glomerulusainak, alveolusainak, génexpressziós hőtérképének és az egész test érrendszerének képei a Wikimedia Commons-ból származnak: https://commons.wikimedia.org/wiki/File:2423_Microscopic_Anatomy_of_Liver.jpg (Public Domain); https://commons.wikimedia.org/wiki/File:Juxtaglomerular_Apparatus_and_Glomerulus.jpg (CC BY 3.0 license); https://commons.wikimedia.org/wiki/File:Alveolus_diagram.svg (Public Domain); https://commons.wikimedia.org/wiki/File:Iris_dendrogram.png (CC BY-SA 4.0 licenc); és https://commons.wikimedia.org/wiki/File:Circulatory_System_en.svg (public domain). A génexpressziós hőtérkép Guo et al. (9) szimulált adatok felhasználásával. Vaszkuláris architektúra alapján Bosetti et al. (10) (CC BY 4.0 licenc).
a vaszkuláris koordináta-rendszer célja nem az érrendszer térképének felépítése. Inkább az az elképzelés, hogy a testen keresztül ismert vaszkuláris útvonalakat tengelyként használják egy koordinátarendszerben, amely leírhatja az anatómiai elemek, például a sejtek helyzetét az érrendszert körülvevő szövetben. Ebben a javasolt keretben a szív kamrái tekinthetők az egész test térképének eredetének. A vaszkuláris tengely tartalmaz vaszkuláris hurkok (hasonló “utak” a Google Map metafora), hogy nyúlik ki az aorta vagy a pulmonalis artéria, fokozatosan kúpos le egyetlen sejt méretét, ahogy közeledik minden más sejt minden szerv a szervezetben, és visszatér a szív. Ezen utak mentén az érrendszer a különböző szervek és szövetek egyedi biológiáját követi, és hasonlóképpen a test szervei és szövetei sem létezhetnek szorosan integrált érrendszerük egyedi tulajdonságai nélkül.
ahogy a genomtérkép lineáris szekvenciává bontja a DNS-t, el tudjuk képzelni, hogy az érrendszer tengelyének komplex 3D-s fordulatait egy egyszerűbb 2D-s “hub-and-spoke” alakra bontjuk, a szív kamráival a központban. Az érrendszer ezen sematikus ábrázolása megkönnyíti (1) a testben való hely leírását; (2) igazítsa az érrendszeri útvonalakat különböző 3D alakzatokkal, de egyenértékű funkcióval a különböző emberektől; (3)azonosítsa a mintákat, például a sejttípus és a génexpresszió változásait, amikor az egyik nagyobbról kisebbre változik hajók egy szerven belül (küllő mentén); és (4) hasonlítsa össze a szöveteket ugyanazon a szinten (például kapillárisok) a különböző szervekben (a küllőkön keresztül).
egy szerv, például a vese, több tízezer érrendszerrel rendelkezik, ha minden kapillárisot egyértelműen figyelembe veszünk. Annak érdekében azonban, hogy a CCF felépítése megvalósítható legyen, további egyszerűsítő feltételezést fogunk tenni, hogy ezen utak közül sok nem különböztethető meg egymástól. Különösen a legkisebb erek (kapillárisok) állnak az egyes szervek kis speciális funkcionális egységeinek középpontjában (pl., máj lobulák a májban, glomerulusok a vesében, alveolusok a tüdőben). Egy egész szervnek sok ilyen érközpontú funkcionális egységre van szüksége, amelyek anatómiailag és fiziológiailag hasonlóak (11). Ez a hasonlóság felhasználható arra, hogy számos vaszkuláris utat néhány reprezentatívvá összeomoljon (2.ábra). A jövőben, amint többet megtudunk ezeknek az utaknak a biomolekuláris profiljairól, finomíthatjuk a CCF-et azáltal, hogy az utakat felosztjuk bármely felfedezett altípusra.

2. ábra. A vese vaszkuláris útvonalának kibontása az egysejtes szintre. A reprezentatív vaszkuláris útvonal a vese artérián keresztül jut be a vesébe, áthalad a glomeruluson, visszatér a vese vénájába. A makroszkálában (balra) és a mezoszkálában (középen) a sárga dobozokban lévő címkék anatómiai struktúrák, amelyek megfelelnek a hurok mentén lévő különböző edényeknek. A mikroszkópnál (jobbra) a sárga dobozokban lévő címkék különböző típusú sejtek, amelyek rövid távolságra vannak a glomerulus közeli edényétől. Az egyes cellák helyzete a legközelebbi hajó címével írható le (pl., “RA0” a glomerulus kapilláris esetében), az ér endotheliumától mért távolság mikrométerben vagy sejtszámban, valamint az ér hosszára merőleges szög (pl. “RA0-10 6-135 XNUMX” vagy “RA0-1C-135 XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX). A jobb szélen minden edényt és a környező szöveteket kivonták az eredeti képből, és függőlegesen igazították, hogy megkönnyítsék a sejttípusok és az eloszlás változását az érrendszer mentén. Ebben a példában az igazított képeket is elforgattuk úgy, hogy a glomerulus középpontja mindig a jobb oldalon legyen. Forrás Fájlok: A vese és a glomerulus képeit a Wikimedia Commons adaptálta:https://commons.wikimedia.org/wiki/File:KidneyStructures_PioM.svg (CC BY 3.0 licenc); éshttps://commons.wikimedia.org/wiki/File:Renal_corpuscle-en.svg (CC BY-SA 4.0 licenc).
az érrendszeri koordináta-rendszer egyes sejtjeinek “címe” négy összetevőből áll. (1) az első a legközelebbi anatómiailag megnevezett ér, amely a legpontosabban azonosítja az érhurkot (az érterületet vagy a “vízválasztót”), például a jobb veseartériát. (2) a következő komponens az edény elágazási szintjét képviseli. A vesében a proximálistól a disztálisig terjedő példák közé tartoznak az interlobar artériák, a kortikális sugárzó artériák, az afferens arteriolák és a glomeruláris kapillárisok. Az elágazási szint numerikusan is meghatározható, a kapillárisok nulla szinten, a magasabb szintek pedig nagyobb számokkal. (3) a harmadik komponens a merőleges távolság mikrométerben vagy a sejtek száma az edény endoteliális rétegétől. (4) választható negyedik komponens lehet az edény hosszára merőleges forgási szög. A nulla fok az alkalmazástól függően sokféleképpen definiálható. Például viszonyulhat a szövetmintán lévő markerhez, vagy anatómiai szerkezet felé mutathat, például a vese legközelebbi glomerulusának középpontja felé. Ezeknek az összetevőknek a hasznosságát és szükségességét kísérleti teszteléssel kell megerősíteni.
egy másik megközelítés az endothel sejtek használata “lehorgonyzó sejtekként” a többi sejt relatív helyzetének GPS-szerű azonosítására. Az Endothelium az egész érrendszert lefedi. Az érrendszer különböző részein különböző endothelsejt (EC) típusok jelennek meg, amelyek szövettanilag kimutathatók az egyedi sejtjellemzők és a szomszédos sejtek révén (a “szövettani ujjlenyomat”), valamint specifikus génprofiljaik elemzésével (a “génexpressziós ujjlenyomat”, 1.ábra hőtérkép) (9, 12, 13). Vaszkuláris szervezeti minta, elágazási komplexitás, átmérő stb. adjon meg további felismerhető jellemzőket, amelyek minden szövethez “vaszkuláris architektúra ujjlenyomatot” képeznek (1.ábra hamis színű fluoreszcens érrendszer képek) (10, 14). Minden szövetnek specifikus oxigéngradiensei vannak, amelyek felhasználhatók az edénytől való távolság meghatározására. Ha a PO2 nem mérhető közvetlenül, akkor következtetni lehet a sejt távolságára a hipoxia által indukálható gének indukciós/expressziós gradienseitől különböző típusú sejtekben (a “hipoxia ujjlenyomat”, 1.ábra egy ér keresztirányú nézete) (15-17).
A vaszkuláris CCF előnyei
az érrendszer koordináta-rendszerének biológiailag van értelme. Minden élő sejtnek a legközelebbi véredény kis sugarú körzetében kell lennie (a szövettől függően 100-1 mm), hogy oxigént kapjon (18); és minden edényt ugyanaz a folytonos endotéliumréteg szegélyez (19). Így az érrendszer töretlen utat képez, amely eléri a test minden részét, zökkenőmentesen lefelé haladva a mérlegeken, a makroszkálától (egész test/klinikai) a mezoszkálától a mikroszkáláig (egysejtes méretű kapilláris erek). Ennek részeként kezeli a fokozatos átmenetet a nagy artériáktól és vénáktól, amelyek a legtöbb emberben konzerválódnak, egészen a mikroszkopikus erek milliójáig, amelyek kategóriánként felismerhetők (pl. glomerulus kapilláris), de nem egyedi nevekkel. Az érrendszer alkalmazkodik az egyéni testmérethez és alakhoz, figyelembe véve az egyének közötti variációkat (20, 21). Meghatározza a funkcionális egységek alakját különböző szervekben, például máj lobulákban, vese glomerulusokban és tüdő alveolusokban. Az új szövetek normális fejlődése az érképződéssel kezdődik, mielőtt további sejttípusok növekedhetnek körülötte (22).
az érrendszer az összes szervet, szövetet és sejtet is összefüggő módon éri el. Úgy tűnik, hogy más anatómiai struktúrák nem rendelkeznek hasonló sokoldalúsággal. Például a csontrendszer kiterjed az egész testre; azonban a szerven belüli sejttől a legközelebbi csontig terjedő távolság több centiméter is lehet, és ez a csont valószínűleg nem része a szervnek, és még kevésbé valószínű, hogy része egy szövetmintának. Az idegrendszer ugyanazokat az utakat követi, mint a kontraktilis tulajdonságokkal rendelkező nagyobb erek, de nem ismert, hogy kiterjednek-e az összes szövetsejtet elérő kisebb erek követésére. Így, ellentétben a sejtek oxigénfüggőségével, nincs garancia arra, hogy minden sejt egy ideg közvetlen közelében van. A szervspecifikus referenciarendszerek olyan egyedi szerkezeti jellemzőkön alapulnak, amelyek csak az adott szervben léteznek (pl. az agy meghatározott régióiban), és nem valószínű, hogy hasznosak lennének a test más részein található sejthelyek ábrázolásához.
az érrendszeri koordináta-rendszernek számos gyakorlati előnye van. A vaszkuláris útvonalakat minden szervben alaposan tanulmányozták, és részletesen leírják a szakirodalomban. Ezek hasznosak, jól ismertek, és számos speciális területen szabványosított nevekkel rendelkeznek. A szöveti vaszkularizációs mintákat klinikailag használják a betegség diagnosztizálására; és a hajókat a műtétekben és a biopsziákban használják, mint a fő anatómiai tereptárgyakat, és meghatározzák az” érrendszeri területeket ” (23, 24). Bár a pontos helyzet a 3D derékszögű térben nehéz lehet meghatározni egy reszektált szövetmintát, a sebész általában képes lesz jelezni, hogy melyik érrendszeri vízválasztó tartalmazza a mintát.
A vaszkuláris CCF korlátai
csak a genomszekvencia bázispárjainak ismerete nem nyújt elegendő információt annak meghatározásához, hogy a DNS hogyan van hajtva egy adott sejtben. Hasonlóképpen, bár a kibontott vaszkuláris koordináta-rendszer képes leírni a közeli sejtek 3D térbeli kapcsolatát a mikroszkálában, az edények kanyargós útjai és a sejtek közötti relatív távolság nagyobb léptékben elvész. A nagyobb léptékű struktúrákra vonatkozó információk a klinikai képalkotás, valamint a szövettani és molekuláris mintázatok integrálásával nyerhetők.
néhány további helyzeti információ elvész az érrendszeri utak összeomlásával. Például egy érrendszeri koordináta-rendszer kezdetben a vese összes glomerulus kapillárisát azonos szerkezetként kezelheti, potenciálisan elfedve a glomerulusok különbségeit a felső és az alsó vese pólusaiban. Bár, ahogy többet megtudunk ezeknek az utaknak a biomolekuláris profiljairól, iteratív módon finomíthatjuk az érrendszeri CCF-et idővel azáltal, hogy az utakat felosztjuk bármely felfedezett altípusra.
Ezen korlátozások ellenére a vaszkuláris koordináta-rendszer elegendő pozicionális információt tárol a sokféle kutatási kérdés megválaszolásához, lehetővé téve a kutatók számára, hogy pontosan lokalizálják az egyes sejteket funkcionális egységeken, szöveteken és szerveken belül, vagy összehasonlítsák a kontextus különböző sejttípusokra gyakorolt hatásait az egész testben a makro – és mezo – skálán.
következő lépések és jövőbeli irányok
az 1.ábrán a vaszkuláris CCF erősen leegyszerűsített és stilizált ábrázolását mutatjuk be az általános koncepció bevezetése érdekében. A tényleges vaszkuláris utak sokkal összetettebbek, a teljes vaszkuláris CCF végül több száz vagy ezer struktúrából, valamint elágazási mintákból áll, amelyek nem követik a szigorú hub-and-spoke elrendezést. Például a máj portálrendszerének vénái, amelyek több szervből vért szállítanak a májba, és a keringési anasztomózisok, mint például Willis köre az agyban, merőlegesek lennének az 1.ábrán látható “küllőkre”, és kereszteznék azokat.
a vaszkuláris CCF-nek szintén be kell építenie az érrendszer normál anatómiai variánsait, például a thyroidea ima-t és a kettős cisztás artériákat, ugyanúgy, mint az egy nukleotid polimorfizmusok (SNP-k) a genom normális variációit írják le. Ahogy kibővítjük és kitöltjük a vaszkuláris CCF részleteit, előfordulhat, hogy hópehely vagy web-szerű megjelenést kap, különböző részekhez rendelt valószínűségekkel, hogy jelezzék annak valószínűségét, hogy megtalálják őket egy adott személyben.
a tényleges vaszkuláris CCF-nek kifinomultabb kódolási sémára van szüksége az edények elnevezéséhez, mint amit az 1. ábra mutat, annak komplexitásának pontosabb ábrázolása érdekében, és szoftveres algoritmusokkal “kiszámíthatóvá” teszi. Az egyik megközelítés a meglévő anatómiai ontológiákra épül, mint például az UBERON, amely már számos edény számára tartalmaz egyedi egységes erőforrás-azonosítókat (Uri-kat), és különféle kapcsolattípusokat határoz meg, mint például a “branching_part_of”, annak leírására, hogy az edények hogyan kapcsolódnak egymáshoz (25).
egy cella egynél több edény közelében lehet, ebben az esetben külön címet lehet hozzárendelni az egyes edényekhez képest. Jövőbeli kutatásokra van szükség annak meghatározásához, hogy mi legyen a megfelelő “vágási” távolság. Kívánatos lehet, hogy több címet tároljon a cellák számára, hogy segítsen háromszögelni helyzetüket a 3D térben.
bár a vaszkuláris CCF kezdeti motivációja egy koordinátarendszer meghatározása a sejtek helyének meghatározására, az emberi test új radiális elrendezése az ér körül, amint azt az 1. ábra mutatja, más tudományos alkalmazásokkal is rendelkezhet. Például a helyzetinformáció ezen a kereten belül analógiát mutat az embriológiai fejlődéssel, és betekintést nyújthat olyan mechanizmusokba, amelyek betegségeket vagy diszregulációkat okoznak, amelyek egy sejtcsoportból származnak. Például a vaszkuláris CCF-ben a 2-es típusú cukorbetegséghez kapcsolódó makrovaszkuláris betegségek (például ischaemiás szívbetegség, perifériás érrendszeri betegség és cerebrovascularis betegség) a központ közelében csoportosulnak, míg a mikrovaszkuláris betegségek (például retinopathia, nephropathia és neuropathia) gyűrűt képeznek a külső körül (26).
összefoglaló
az érrendszernek számos olyan tulajdonsága van, amelyek reagálnak a CCF számára korábban kívánatosnak tartott jellemzőkre, hogy lehetővé tegyék az emberi test összes sejtjének feltérképezését (7). (1) több skálán működik. A folyamatos endothelium révén zökkenőmentes átmenetet biztosít a nagy anatómiai struktúrákról a sejtek szintjére. (2) minden testszövetre alkalmazható. Mivel a szervek az erek körül fejlődnek, az érrendszer minden skálán keretezi a szerv architektúráját. Az érrendszeri minták annyira megkülönböztető jellegűek, hogy az erek képei önmagukban, az összes többi sejt eltávolításával könnyen felhasználhatók a szerv azonosítására. (3) figyelembe veszi az adományozók közötti különbségeket. A vaszkularizáció természetesen alkalmazkodik a szövetek, a testméret és az alak egyedi variációihoz. Ahelyett, hogy fel kellene térképeznie az egyes glomerulusok 3D koordinátáit egy személyben egy másik személy koordinátáival, az érrendszeri CCF minden sejtet egy reprezentatív glomerulus kapillárison belül helyezne el minden embertől. (4) az érrendszer jól ismert a különböző klinikai specialitások gyakorlói számára, segítve mind a betegség diagnosztizálását, mind a műtétek irányítását, és a patológusok, radiológusok és más klinikusok tereptárgyaként használják. Ez megkönnyítené a szövetminták testben történő elhelyezését és az egyes sejtek helyének regisztrálását. Bár egyetlen CCF sem ideális minden felhasználási esetre, a vaszkuláris CCF meghatároz egy természetes koordináta-rendszert, amely megkönnyíti a több ember biomolekuláris adatainak kombinálását és biológiailag releváns kutatási kérdések feltevését.
Adatelérhetőségi nyilatkozat
nyilvánosan elérhető adatkészleteket elemeztünk ebben a tanulmányban. Ezek az adatok itt találhatók: https://www.proteinatlas.org.
szerzői hozzájárulások
a GW ezt a tanulmányt a CCF 2017.évi találkozójának és a CCF 2019. évi műhelyének jelentései alapján fogalmazta meg. A KB és az YJ kritikus visszajelzéseket adott. A GW megírta az eredeti tervezetet, további szöveget átírva a CCFWS-01 diabemutatóból. Minden szerző hozzájárult a kézirat szerkesztéséhez.
finanszírozás
ezt a kutatást a Nemzeti Egészségügyi Intézetek (NIH) OT2OD026671 díja támogatta. Ez a munka nem képviseli az NIH vagy a Nemzeti Szív -, Tüdő-és Vérintézet (NHLBI) véleményét.
összeférhetetlenség
a szerzők kijelentik, hogy a kutatást olyan kereskedelmi vagy pénzügyi kapcsolatok hiányában végezték, amelyek potenciális összeférhetetlenségnek tekinthetők.
Köszönetnyilvánítás
köszönjük Dr. Zorina S. Galis a National Institutes of Health-től a 2017-es CCF találkozón és a 2019-es CCF workshopon az érrendszer alapú koordináta-rendszer ötletének kidolgozásában nyújtott segítséget, előadásokat adott nekünk ezekről az eseményekről, és részt vett számos beszélgetésben, amelyek a kézirat alapját képezték. Az értékelők szakértői észrevételei segítettek tisztázni és részletezni a javasolt vaszkuláris alapú közös koordináta-rendszert.
3. Uhl O. O., B. O. O., Agaton C., Szigyarto CA, Amini B., Andersen E., et al. Egy humán fehérje atlasz a normál és a rákos szövetek számára, antitest proteomikán alapulva. Mol Sejt Proteomika. (2005) 4:1920–32. doi: 10.1074 / mcp.M500279-MCP200
PubMed absztrakt | CrossRef teljes szöveg | Google Tudós
12. Vanlandewijck M, He L, M Initibe MA, Andrae J, Ando K, Del Gaudio F, et al. Az agyi érrendszer sejttípusainak és zónáinak molekuláris atlasza. Természet. (2018) 554:475–80. doi: 10.1038/nature25739
PubMed Abstract | CrossRef Full Text | Google Scholar
14. Johnson C, Sung HJ, Lessner SM, Fini ME, Galis ZS. Matrix metalloproteinase-9 is required for adequate angiogenic revascularization of ischemic tissues: potential role in capillary branching. Circ Res. (2004) 94:262–8. doi: 10.1161/01.RES.0000111527.42357.62
PubMed Abstract | CrossRef Full Text | Google Scholar
15. De Santis V, Singer M. a szerv perfúziójának szöveti oxigénfeszültségének monitorozása: indoklás, módszertanok és irodalmi áttekintés. Br J Anaesth. (2015) 115:357–65. doi: 10.1093 / bja/aev162
PubMed absztrakt | CrossRef teljes szöveg | Google Tudós
17. Koch CJ. A sejtek és szövetek abszolút oxigénszintjének mérése oxigénérzékelők és 2-nitroimidazol EF5 alkalmazásával. Módszerek Enzimol. (2002) 352:3–31. doi: 10.1016/S0076-6879(02)52003-6
PubMed Abstract | CrossRef Full Text | Google Scholar
20. Paruchuri V, Salhab KF, Kuzmik G, Gubernikoff G, Fang H, Rizzo JA, et al. Aortic size distribution in the general population: explaining the size paradox in aortic dissection. Cardiology. (2015) 131:265–72. doi: 10.1159/000381281
PubMed Abstract | CrossRef Full Text | Google Scholar
21. Abadi E, Segars WP, Sturgeon GM, Roos JE, Ravin CE, Samei E. a tüdő architektúrájának modellezése az XCAT Phantoms sorozatában: fiziológiailag megalapozott légutak, artériák és vénák. IEEE Trans med Imaging. (2018) 37:693–702. doi: 10.1109 / TMI.2017.2769640
PubMed absztrakt | CrossRef teljes szöveg | Google Tudós
24. Majno P, Mentha G, Toso C, Morel P, Peitgen HO, Fasel JH. A máj anatómiája: vázlat három komplexitási szinttel–további lépés a személyre szabott területi májrezekció felé. J Hepatol. (2014) 60:654–62. doi: 10.1016/j.jhep.2013.10.026
PubMed Abstract | CrossRef Full Text | Google Scholar
26. Cade WT. Diabetes-related microvascular and macrovascular diseases in the physical therapy setting. Phys Ther. (2008) 88:1322–35. doi: 10.2522/ptj.20080008
PubMed Abstract | CrossRef Full Text | Google Scholar