目次
要約
背景
歯原性ケラトサイト(OKC)は、治療後の再発率が高い局所的に攻撃的な歯原性嚢胞である。 いくつかの保守的な手術は、ケラトシストの治療に示唆されているが、練習の概要での作業は、より良い結果をレンダリングすることができます。
メソッド
我々は、データベースMEDLINE、Web of Science、Scopus、コクランライブラリとGoogle Scholarだけでなく、OKCの病因、臨床提示、イメージング、診断と治療モダリティに報告する研究のためのグレーの文献(書籍や論文)で文献レビューを行った。
結果
OKCの特徴は、診断、治療計画と治療自体に最適なプロトコルを確立するために、文献に照らして議論されている。
結論
OKCのは、他の定期的な、普通の、歯原性嚢胞上の特別な注意に値します。 OKCの評価におけるx線写真およびCTスキャン,術前の組織学的診断およびOKCの核除去に続いてカルノイの適用および口腔粘膜の嚢胞への付着領域の上にある粘膜の切除は,通常OKCの治療における適切なプロトコールである。
キーワード
歯原性ケラトサイト、角嚢胞性歯原性腫瘍、歯原性嚢胞、カルノイ溶液、治療、再発
はじめに
頭頸部腫瘍の最新の世界保健機関分類(2017)は、角嚢胞性歯原性腫瘍(KCOT)の臨床的、放射線学的および生物学的特徴に関する概念を再評価し、決定した。この病変を再び歯原性ケラトサイト(okc)に名前を変更する。 しかし、この政策変更の動機は欠けている。 OKCは潜在的に非常に攻撃的な病変であり(図1)、この名前の変更は外科医の間で混乱をもたらす可能性があり、この病変を適切に治療するために外科医の間で注意力を低下させる傾向がある。
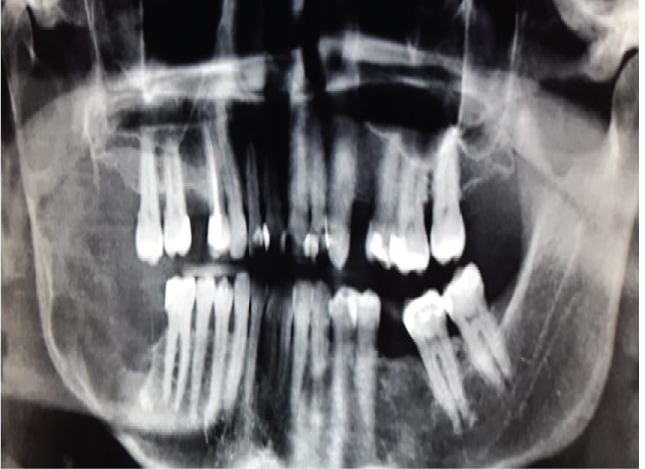 図1:その攻撃性を示す下顎骨の右後部領域に大きなOKC。 図1を見る
図1:その攻撃性を示す下顎骨の右後部領域に大きなOKC。 図1を見る
治療後の高い再発率とは別に、Emerson,et al. 首を介して縦隔に二つの再発OKCの拡張を説明しました。 他の著者らは、頭蓋骨の基部に三つのOKCの拡張、二つのOKCの側頭筋に浸透し、二つのOKCの咬筋にすでに報告しています。 骨移植片における再発OKCを示す四つの症例報告が発表されている。 通常の、普通の、歯原性嚢胞はこのように動作しません。
OKCの攻撃性は、通常の歯原性嚢胞と比較して、上皮嚢胞ライニングの高い有糸分裂指数に起因する可能性がある。 これは、嚢胞壁の一部が残されている間に、嚢胞の断片的な脱核後の再発するOKCを説明するであろう。 OKCは歯板の残骸に由来すると考えられているが,しばしば歯槽隆起部に重なる口腔粘膜に位置する上皮細胞巣および微小嚢胞も原発性および再発性OKCの重要な供給源である可能性がある。 これは、特に顎の後部領域の場合である。
これらの上皮細胞巣および/または微小嚢胞は、口腔粘膜の基底層に由来し、hamartiasであると考えることができる。
これらの上皮細胞巣および/または 組織学的には、脱落現象がいくつかのケースで見られることができる。 口腔粘膜の基底層から生じる骨内OKCの場合、骨穿孔はコンピュータ断層撮影(CTスキャン)で容易に検出することができ、口腔粘膜のそのような領域はOKC
OKCの起源とその可能性のある再発パターンに関する上記の理論は、外科的治療計画において役割を果たすべきである。 OKCには,脱核単独,脱核後の補助療法(Carnoy溶液の適用,凍結療法,末梢骨切除術),上にある粘膜の除去を含む補助療法の有無にかかわらず脱核,有袋化単独および有袋化後の遅延脱核などのいくつかの主に保存的アプローチが提案されている。
一般に、症候群OKC(Nevoid基底細胞癌症候群)の治療モダリティは、非症候群OKCと同じである。 しかし、症候群患者におけるOKC発症のパターンは、腫瘍抑制遺伝子であるPTCH1の不活性化などの分子/遺伝子変化によって広く影響され、症候群患者が顎骨に複数のOKCを有することが多い理由の一つを説明するものである。 したがって、再発OKCは、実際には、新しい、プライマリOKCである可能性があります。
本研究の目的は、臨床的洞察を与え、文献に照らして、非syndromic OKCの治療の主な特徴およびモダリティを議論することである。
材料と方法
私たちは、データベースMEDLINE、Web of Science、Scopus、コクランライブラリとGoogle Scholarだけでなく、灰色の文献(書籍や論文)で文献レビューを行い、英語やポルトガル語で書かれたKCOTまたはOKCに関する研究を検索しました。 合理的な治療方針に基づいて信頼性の高いデータを考え出すために、検索された研究から、OKCの病因、臨床提示、イメージング、診断および治療モダリティに関
結果と議論
OKCは、主に歯の支持領域(すなわち、切歯、犬歯、小臼歯および第1/第2大臼歯領域)における、未歯に関連するかどうかに関連する骨内病変 それらはまた、しばしば口腔粘膜の基底層に位置する上皮細胞巣および微小嚢胞から生じる可能性があり、主に顎の後部領域(すなわち、下顎の第3大臼歯、角度および枝および上顎の第3大臼歯/上顎結節)に位置する。 Nonsyndromic OKCはまたshhシグナル伝達経路を活動化させ、嚢胞性の上皮の増悪された拡散で起因するPTCH1遺伝子の突然変異か不活性化に苦しむかもしれません。 OKCは可能性としては非常に積極的であり、腫瘍または嚢胞であることのコンセンサスはまだ達していない。
OKCの臨床的提示
OKCは、皮質骨の拡張がないか、またはほとんどない下顎または上顎の髄腔内で成長する。 したがって、初期の小さな病変は、感染しない限り、通常無症候性である。 しかし、嚢胞が皮質骨のより薄い領域を内側から外側に穿孔すると、局所的な腫脹が起こることがあります(図2)。 これは規則的な、通常の、odontogenic包嚢、例えばradicularまたはdentigerous包嚢と頻繁に起こります。 突然、患者は下顎の枝のより大きいOKCの場合にはtrismusを開発するかもしれません(図1)。 上顎の大きなOKCは、上顎洞に拡大し(図3)、同じ側に鼻閉塞を引き起こす可能性があります。 一方,成長の遅い嚢胞は骨膜骨の同相を刺激し,皮質穿孔なしに骨拡張を引き起こす可能性がある。 OKCのは、人生の第二から第三十年の男性の下顎骨の後部領域で最も一般的に、広い患者の年齢範囲にわたって発生します。
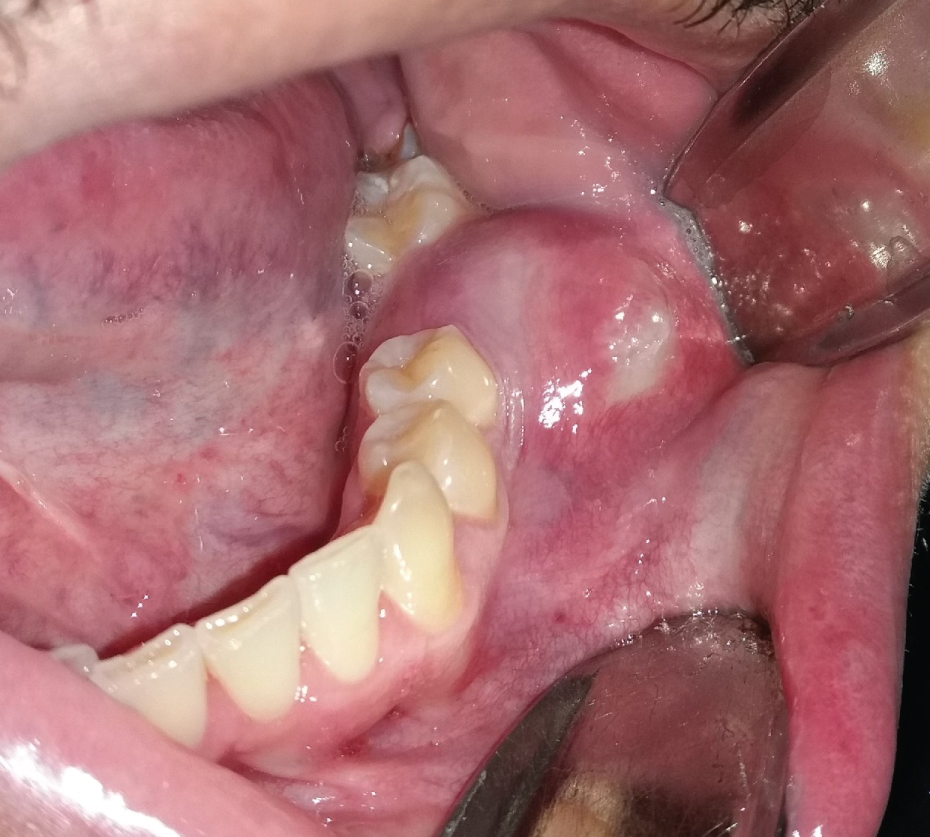 図2:感染したOKCは、欠けている歯の領域に痛みや腫れを引き起こします36。 図2を見る
図2:感染したOKCは、欠けている歯の領域に痛みや腫れを引き起こします36。 図2を見る
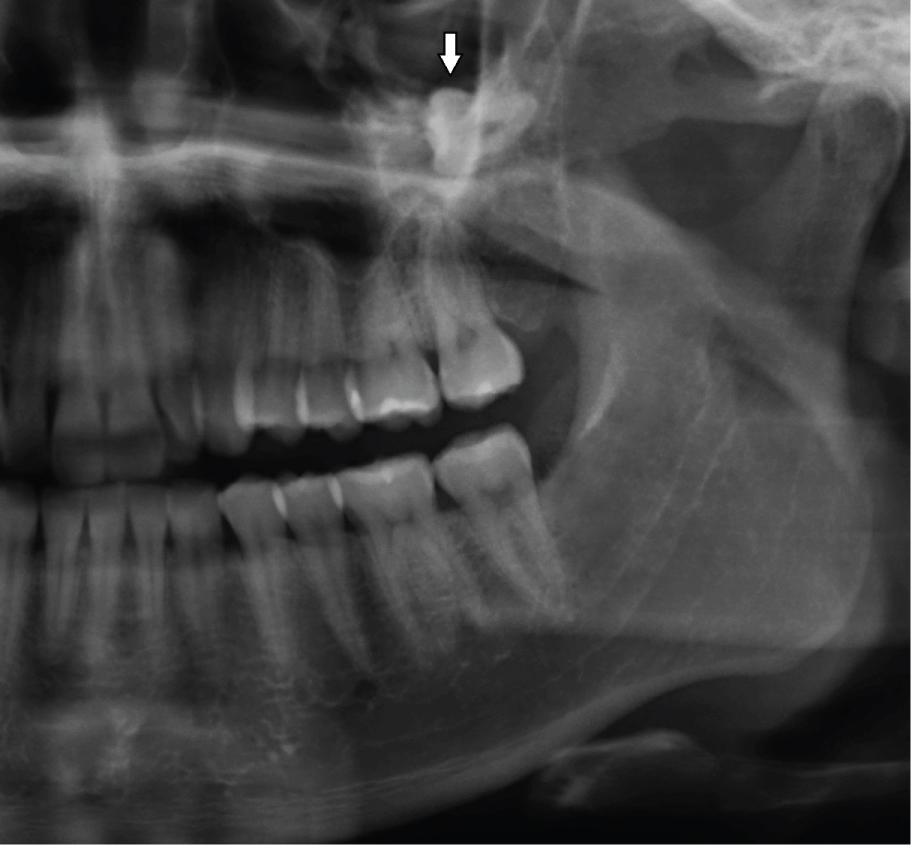 図3:左上顎洞の大きなOKC、歯28を上に変位させる(矢印)。 View Figure3
図3:左上顎洞の大きなOKC、歯28を上に変位させる(矢印)。 View Figure3
OKCのイメージング
OKCのX線写真は、一般的にスカラップマージンの有無にかかわらず明確に定義された境界を有する単房嚢胞性病変とし しばしば、それらは通常の歯原性嚢胞と容易に区別できない(図4)。 OKCは歯とは関係がないかもしれませんし、クラウンは嚢胞の中に完全にあるかもしれません。 それらは、側歯周嚢胞に類似した歯根の側方側面に隣接して配置されてもよい。 再発性および症候群性OKCを含むいくつかの研究で報告された1138OKCのx線写真の側面のレビューでは、672は単眼(59%)、342多眼(30%)、202は滑らかなまたは明確に定義された境界(18%)、70はスカラップ境界(6%)を持っていたことがわかった。 多くの場合、放射線学的側面は報告されなかった。
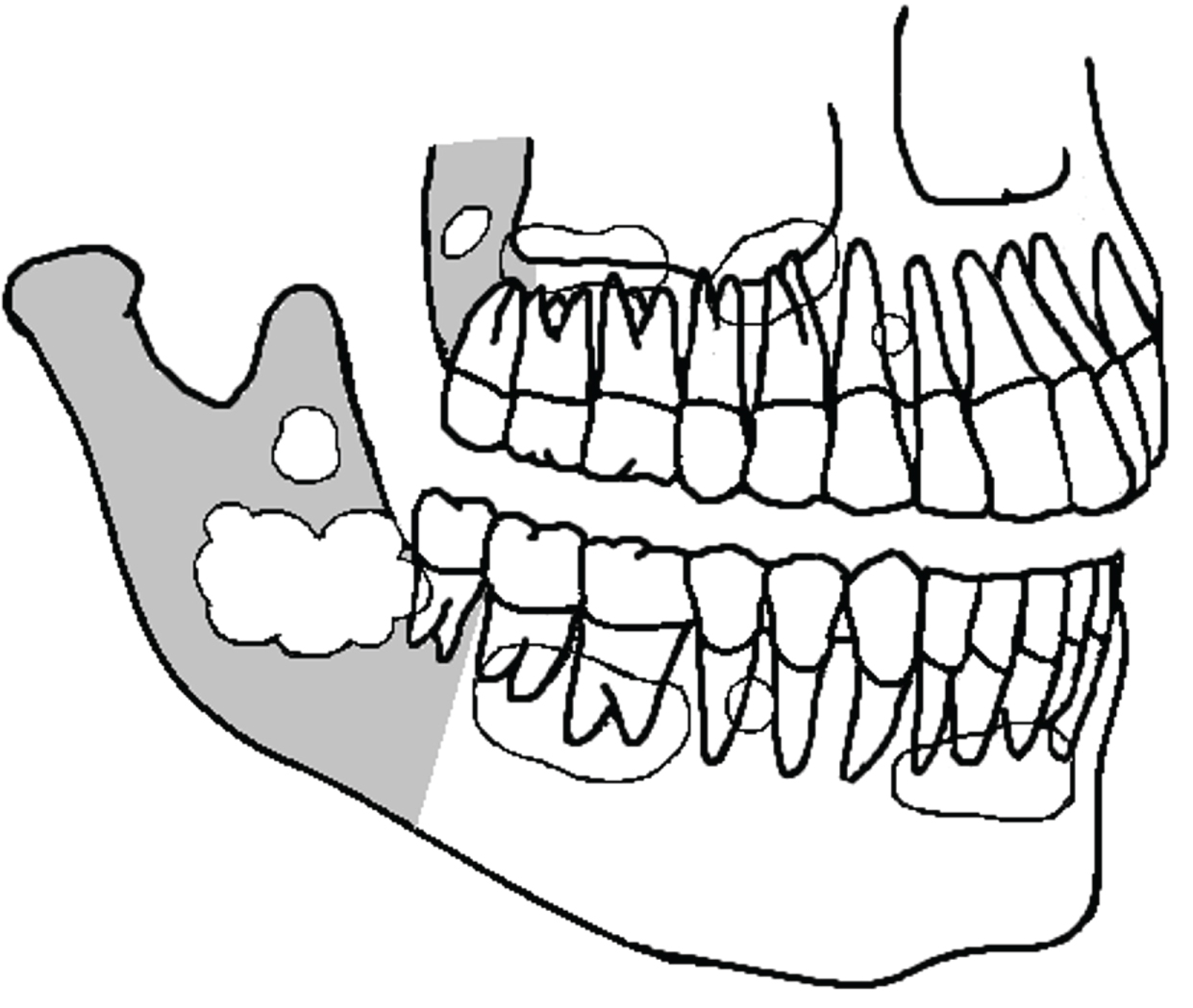 図4:下顎と上顎におけるOKCの提示のいくつかの可能性のいくつか(模式図)。 それらは通常規則的なodontogenic包嚢と混同されます。 灰色の領域は、顎骨の後部領域である。 ビュー図4
図4:下顎と上顎におけるOKCの提示のいくつかの可能性のいくつか(模式図)。 それらは通常規則的なodontogenic包嚢と混同されます。 灰色の領域は、顎骨の後部領域である。 ビュー図4
コンピュータ断層撮影は、下歯槽神経(IAN)、上顎洞、鼻腔などの解剖学的構造のより良い定義でOKCのすべての寸法を検出する上で貴重なツー CTスキャンは皮層のパーホレーションの精密な検出を可能にする(特に下顎の角度/ramusまたは上顎のtuberosityで)、もしあれば。 皮質穿孔はおそらくOKCに上にある口腔粘膜が付着している領域であり,そのような領域は外科的切除に含まれなければならない。 特に歯の支持領域におけるより小さな単房嚢胞は、通常の歯原性嚢胞、特に歯周側嚢胞と容易に混同される可能性がある。
臨床診療では、磁気共鳴画像法(MRI)は限られた値を有するが、特により大きなOKCの軟部組織関与の場合には、放射線学的評価を補完する可能性がある。 MRIはまた顎のameloblastomasおよび他の包嚢および腫瘍からOKCを区別するのを助けます。 MRIは、局所性および固体塊の存在を検出する。 また、管腔内液の信号強度によって嚢胞壁の厚さおよび嚢胞の含有量を示すことになる。 我々は、二つの研究で報告された39OKCのコントラスト強化されたMRIのイメージングデータをプールし、24が単眼(62%)であり、15が多眼(38%)であったことがわかった。 嚢胞壁の厚さは26OKCの(67%)で薄く、11(28%)で厚かった。 しかし、2つの嚢胞のカプセルの厚さの情報は入手できなかった。 流体の信号強度に関しては、21OKCの嚢胞性(54%)であった。 サーティーンは混合された(33%)、すなわち固体と嚢胞性であり、5は固体(13%)であった。 しかし,固形分は嚢胞内の角化デブリの沈着に起因するものであり,嚢胞壁の管腔内増殖に起因するものではない。 (主に非固体病変における)管腔内液の信号強度は、主に異種(30OKCの-77%)ではなく、均質(9OKCの-23%)であった、この機能は、エナメル芽細胞腫からOKCの区別に特に関
OKCの診断
切開生検による組織病理学的評価は、臨床的および放射線的提示から疑いが生じた場合、手術前にOKCを診断する最良の方法である。 切開生検はOKCに炎症を引き起こし,術後標本の病理組織学的分析を妨げる可能性がある。 嚢胞壁は繊維状であり、折り畳まれた、薄く、規則的な無角化上皮5-8細胞層の厚さで裏打ちされ、rete尾根はない。 パラケラチン表面は典型的には波状であり、基底層は明確に定義され、しばしばpalisadedであり、hyperchromatic核および逆の核極性を示す焦点領域である。 しかし、前に述べたように、嚢胞の炎症は、嚢胞壁の化生に二次的な偽陰性の結果をもたらす可能性がある。 非角化上皮および基底層の特徴は完全に消失している可能性がある。
吸引液中のタンパク質レベルおよびケラチンフレークの研究への吸引生検は、診断を助け、病理組織学的結果の問題を克服するのに役立つ可能性が
治療モダリティ
全体的な勧告
OKCに近い非歯は歯内治療および維持される可能性があります(図5aおよび図5b)が、嚢胞が根状表面に付着しているか、またはOKCによる根状再吸収を有するものは除去されるべきである。 OKCを完全に除去した後、患者は最初の五年と隔年それを超えて毎年放射線フォローアップを受けるべきである。 再発は、25年の長い期間にわたって発生する可能性があります。
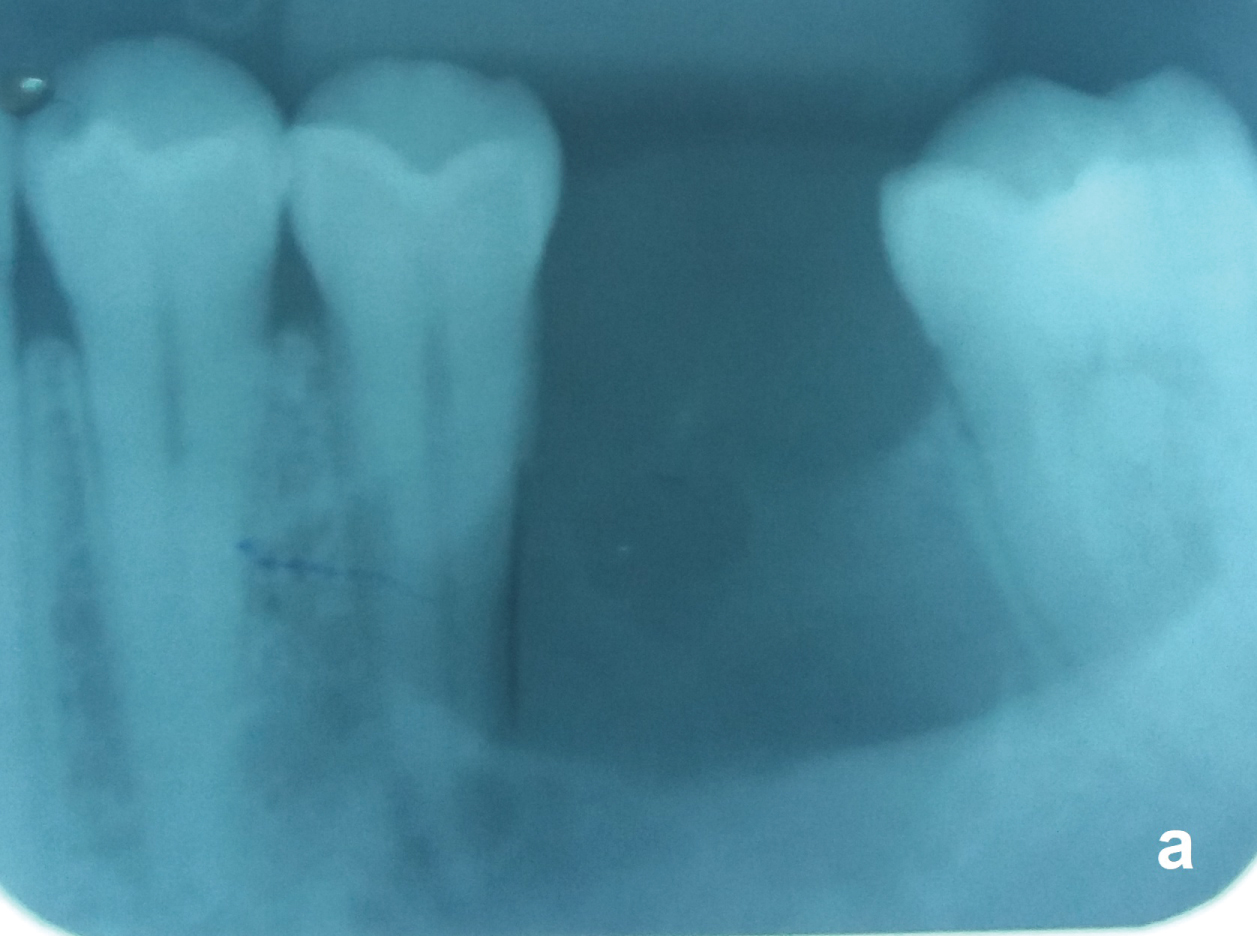 図5A:図2と同じケース。 非生命歯3 5と生命歯3 7との間に明確に定義された境界を有する単眼OKC。 両方の歯の歯周靭帯が保存されていることを観察してください。 図5Aを見る
図5A:図2と同じケース。 非生命歯3 5と生命歯3 7との間に明確に定義された境界を有する単眼OKC。 両方の歯の歯周靭帯が保存されていることを観察してください。 図5Aを見る
 図5B:歯35は手術前に歯内治療を受けました。 図5Bを見る
図5B:歯35は手術前に歯内治療を受けました。 図5Bを見る
OKCの脱核
脱核は、嚢胞の完全な除去で構成されていますが、この作業は、OKCの脆弱な壁のために達成することは非常に困難で 摘出または掻爬後に骨腔に残された嚢胞内層は、再発のリスクを高める。 したがって、手術前にOKCが診断された場合、脱核単独では推奨されません。
脱核後に診断された小さなOKC(直径約1cm以下、一般的には歯の支持領域)にはそれ以上の治療は必要ありませんが、患者は厳格な放射線学的フォローア これらの領域での再発は、患者に多くの害を与えることなく容易に対処することができる。
上にある粘膜の切除
CTスキャンで皮質穿孔が示された場合、上にある口腔粘膜およびOKCへの付着は、この領域に位置する上皮細胞巣および/または微小嚢胞を除去するために、常に安全マージンで切除されるべきである。
OKCの脱核に続いてカルノイ溶液(CS)の適用
CSの適用は、おそらく補助療法の最良の選択肢であり、OKCの再発率を低下させる最も効果的な保 それは安全で低コストの手順です。 この溶液は、60%の絶対アルコール、30%のクロロホルム、10%の氷酢酸および1グラムの塩化第二鉄によって構成される。 CSは、脱核後に残された可能性のある残りの上皮細胞の即時固定/不活性化を引き起こし、また、存在する場合、皮質穿孔の領域に位置する上皮細胞巣または CSを浸したガーゼ片を湾曲したケリークランプで骨腔に1分間塗布する。 これらの構造に回復不能な損傷を与える可能性があるため、イアン、隣接する重要な歯の歯周および洞の薄い骨壁にCSを塗布しないでください。
Carnoy’s Solution(CS)が歯原性角質嚢胞の再発率を低下させる有益な結果を得たにもかかわらず、骨壊死や骨新生の質の悪さなどの手術分野で暴露された構造に対する仮説的に有害な影響に関する組織学的情報の欠如は、多くの外科医がこの補完的な治療法を疑問視し、放棄することを導いた。
OKCの摘出に続いて末梢ostectomy
末梢ostectomyは、OKCの再発率の制御における補助療法の第二のより良い選択肢である可能性があります。 それは残りの上皮細胞および上皮細胞の巣/microcystsの機械取り外しによって再発率の減少でよい結果を示す安全で、低価格のプロシージャです。 大きな丸いバールで、豊富な生理食塩水の灌漑の下で、骨腔に沿って1.5mmの深さまで骨組織を除去する。
OKCの脱核に続いて凍結療法
脱核後、液体窒素のスプレー(-196。6℃)は、骨腔に1分間一度適用され、残りの上皮細胞および上皮細胞巣/マイクロシストを凍結させ、病理細胞の物理的死を1.5mmの深さまで引き起こすが、再発率を低下させるためのこの技術の使用は議論の余地がある。 壊れやすい下顎骨に液体窒素の噴霧を適用すると、術後の病理学的骨折のリスクが増加する。
有袋類化単独および有袋類化および遅延脱核
有袋類化は、OKCを口腔の積分腔に変換することである。 それは決定的(有袋類化単独)または一時的(有袋類化および遅延脱核)であり得る。 嚢胞が口腔環境に曝されると、上皮嚢胞ライニングは化生を受けて口腔粘膜の上皮と区別できなくなり、嚢胞腔は減圧のためにサイズが縮小し、x線写真またはCT缶で監視することができる。 OKCは化生後にはあまり積極的ではなくなりますが、依然として高い再発率を示しています。 一方、有袋類化は、有袋類化された断片が存在する場合、皮質穿孔の領域で除去されれば、再発率に関するより良い結果を示す(Paul JW Stoelinga,Emeritus Professor of Radboud University,personal communication. “上にある粘膜の切除”のセクションを参照してください)。 有袋類化は、患者のためにやや面倒なことがあります。 従って、それは大型OKCの高齢者か悪い危険の患者でもっと示されます。
最終的な考慮事項
歯原性角化嚢胞は、診断、治療計画および治療自体に関する他の通常の歯原性嚢胞よりも特別な注意が必要である。 この損害の名前の現在の変更にもかかわらず、OKCは腫瘍としてし、臨床練習に混乱を持って来るかもしれません。
要するに、OKCの評価には通常、x線写真とCTスキャンで十分です。 健康な患者では,OKCの脱核に続いてカルノイを適用し,OKCへの付着領域の上にある粘膜を切除することが選択されるべきである。 顎の後部の地域の大きいOKCの場合では、主に、限定的な処置の前の12-18か月間marsupializationは外科的処置の危険をdecraseために損害のサイズの減少のよい選択です。
最終的には、OKCの実践の概要は、固体/多嚢胞性エナメル芽細胞腫などの他の積極的な歯原性病変の治療に適用することができる。
謝辞
著者は、利益相反がないことを宣言します。
- Speight P、Devilliers P、Li TJ、Odell EW、Wright JM(2017)歯原性ケラトサイト。 In:El-Naggar AK,Chan JKC,Grandis JR,Takata T,Slootweg PJ,who頭頸部腫瘍の分類. (第4edn)、Iarc、リヨン、フランス、235-236。
- Stoelinga PJW(2018)Keratocystic odontogenic tumour(KCOT)は再びodontogenic keratocyst(OKC)と改名されました。 30313-30318.
- Shear M,Speight PM(2007)Odontogenic keratocyst. で: Shear M、Speight PM、口腔および顎顔面領域の嚢胞。 (第4回edn)、ブラックウェル出版社、6-58。
- Emerson TG,Whitlock RI,Jones JH(1972)歯原性角質嚢胞(原始嚢胞)による軟部組織の関与。 Br J経口Surg9:181-185.
- Jackson IT,Potparic Z,Fasching M,Schievink WI,Tidstrom K,et al. (1993)角質細胞を切開することによる頭蓋骨基部の浸透。 J Craniomaxillofac Surg21:319-325.
- Franc C,Cresseaux P,Richard L,Breton P,Freidel M(1996)ケラトサイトまたは類表皮嚢胞: 頭蓋内病変を有する症例のアプロポスを理解する現状。 97:270-282.
- Soost F,Stoll C,Gerhardt O,Neumann HJ(1999)頭蓋底への拡張を伴う顎の角化嚢胞。 ゼントラーレ60章11-14節を参照のこと。
- Worral SF(1992)側頭筋内の再発性歯原性角化細胞。 Br J経口Surg30:59-62.
- Abé T,Maruyama S,Yamazaki M,Essa A,Babkair H,et al. (2014)角嚢胞性歯原性腫瘍の軟部組織対応物としての筋肉内角化球: 免疫組織化学による鑑別診断。 ハムパトル45:110-118。
- Makarla S,Bavle RM,Muniswamappa S,Narasimhamurthy S(2015)大きな診断外角膜嚢胞性歯原性腫瘍。 2015年には日本代表に選出されている。
- 山本K,松末Y,栗原M,高橋Y,桐田T(2013)角膜嚢胞性歯原性腫瘍の特徴を有する頬粘膜における角膜嚢胞。 7:152-156
- Schofield JJ(1971)歯原性ケラトサイトの異常な再発。 Br Dent J130:487-489.
- Persson G(1973)骨移植における角化細胞の顕著な再発。 Int J経口Surg2:69-76.
- Attenborough NR(1974)骨移植における歯原性角化細胞の再発:症例の報告。 Br J経口Surg12:33-39.
- DeGould MD,Goldberg JS(1991)骨移植における歯原性角化細胞の再発。 事件の報告。 Int J口腔顎顔面Surg20:9-11.
- Toller P(1967)顎の嚢胞の起源と成長。 Ann R Coll Surg Engl40:306-336.
- Stoelinga PJW,Peters JH(1973)顎の角質嚢胞の起源に関するメモ。 Int J経口Surg2:37-44.
- Stoelinga PJ(2001)定義されたプロトコルに従って処理された角化嚢胞の長期フォローアップ。 Int J口腔顎顔面Surg30:14-25.
- Stoelinga PJW(2003)角化嚢胞の病因および病因。 口腔顎顔面Surg Clin北午前15:317-324.
- Stoelinga PJW、Peters JH、van de Staak Wj、Cohen MM Jr(1973)基底細胞母斑症候群におけるいくつかの新しい知見。 Oral Surg Oral Med Oral Pathol36:686-692.
- Stoelinga PJ(2003)嚢胞の脱核およびカルノイ溶液による骨欠損の治療と併せて、上にある付着した粘膜の切除。 口腔顎顔面Surg Clin北午前15:407-414.
- Al-Moraissi EA、Pogrel MA、Ellis E(2016)上にある口腔粘膜の切除は、角嚢胞性歯原性腫瘍の治療における再発率を低下させるか? 体系的なレビューとメタ分析。 J口腔顎顔面Surg74:1974-1982.
- Blanas N,Freund B,Schwartz M,Furst IM(2000)歯原性ケラトサイトの治療および予後の系統的レビュー。 Oral Surg Oral Med Oral Pathol Oral Radiol Endod90:553-558.
- Al-Moraissi EA,Dahan AA,Alwadeai MS,Oginni FO,Al-Jamali JM,et al. (2017)角膜嚢胞性歯原性腫瘍の管理後の再発率が最も低い外科的治療は何ですか? 大規模な体系的レビューとメタ分析。 J Craniomaxillofac Surg45:131-144.
- de Castro MS,Caixeta CA,de Carli ML,Ribeiro Júnior NV,Miyazawa M,et al. (2018)Conservative surgical treatments for nonsyndromic odontogenic keratocysts:a systematic review and meta-analysis. Clin口頭Investig22:2089-2101.
- Philipsen HP(2005)角嚢胞性歯原性腫瘍。 で: Barnes L、Eveson JW、Reichart P、Sidransky、世界保健機関腫瘍の分類。 頭頸部腫瘍の病理学および遺伝学、IARCプレス、リヨン、フランス、306-307。
- Ribeiro Junior O,Borba AM,Alves C,De Gouveia M,Coracin FL,et al. ら(2 0 1 8)Keratocystic odontogenic tumors and carnoy’s solution:Results and complications assessment. 口頭Dis18:548-557.
- Vedtofte P,Praetorius F(1979)臨床的および組織学的特徴に関連した歯原性角質細胞の再発。 72人の患者の20年のフォローアップの調査。 Int J経口Surg8:412-420.
- Bataineh AB,al Qudah M(1998)下顎歯原性角化嚢胞の治療. Oral Surg Oral Med Oral Pathol Oral Radiol Endod86:42-47.
- Berge TI,Helland SB,Sælen A,Øren M,Johannessen AC,et al. ら(2 0 1 6)非症候性角嚢胞性歯原性腫瘍の再発のパターン。 口頭Surg口頭Med口頭Pathol口頭Radiol122:10-16。
- Boffano P,Ruga E,Gallesio C(2010)Keratocystic odontogenic tumor(odontogenic keratocyst):トリノ大学からの261病変の疫学的、臨床的、および放射線学的特徴の予備的レトロスペクティブレビュー。 J口腔顎顔面Surg68:2994-2999.
- Deepthi PV、Beena VT、Padmakumar SK、Rajeev R、Sivakumar R(2016)南ケララ州の人口における1177の歯原性病変の研究。 20:202-207.
- Leung YY,Lau SL,Tsoi KY,Ma HL,Ng CL(2016)脱核を用いた角嚢胞性歯原性腫瘍の治療およびカルノイ溶液による残存骨欠損の治療の結果。 Int J Oral Maxillofac Surg45:1154-1158.
- MacDonald D,Gu Y,Zhang L,Poh C(2013)臨床的および放射線学的特徴は、孤立性角嚢胞性歯原性腫瘍における再発を予測することができるか? Oral Surg Oral Med Oral Pathol Oral Radiol115:263-271.
- Mamabolo M,Noffke C,Raubenheimer E(2011)アフリカの農村部の人口サンプルにおける人生の最初の二十年に現れる歯原性腫瘍:26年の遡及分析。 Dentomaxillofac Radiol40:331-337.
- McIvor J(1972)歯原性ケラトシストの放射線学的特徴。 Br J経口Surg10:116-125.
- Ong ST,Siar CH(1995)malaysian populationにおける歯原性角化嚢胞:臨床的、放射線学的および組織学的考察。 年代記2:9-14.
- Park TW,Kim SR(1985)歯原性ケラトサイトの臨床および放射線学的研究。 1:43-53
- Simiyu BN,Butt F,Dimba EA,Wagaiyu EG,Awange DO,et al. (2013)顎の角嚢胞性歯原性腫瘍および関連病理:ケニアの紹介教育病院における10年間の臨床病理学的監査。 J Craniomaxillofac Surg41:230-234.
- Tabrizi R,Omidi M,Dehbozorgi M,Hekmat M(2014)下顎骨の歯原性角質嚢胞における再発の頻度と放射線学的特徴および治療の相関。 J25:e413-e417。
- Urs AB、Arora S、Singh H(2014)小児患者における骨内顎病変:レトロスペクティブ研究。 J Clin Diagn Res8:216-220.
- Brondum N,Jensen VJ(1991)角質嚢胞の再発と減圧治療. 四十から四例の長期フォローアップ。 口頭Surg口頭Med口頭Pathol72:265-269。
- 中村N、T光康、Y光康、竹富T、樋口Y、et al. (2002)歯原性ケラトシストの有袋類化:成長特性の影響および変化の長期フォローアップ分析。 Oral Surg Oral Med Oral Pathol Oral Radiol Endod94:543-553.
- Cunha JF,Gomes CC,De Mesquita RA,Goulart EMA,De Castro WH,et al. ら(2 0 1 6)歯原性角球の再発に関連する臨床病理学的特徴:コホートレトロスペクティブ分析。 Oral Surg Oral Med Oral Pathol Oral Radiol121:629-635.
- Irvine GH,Bowerman JE(1985)下顎角化嚢胞: 外科的管理。 Br J口腔顎顔面Surg23:204-209.
- 南M、金田T、小澤K、山本H、板井Y、et al. ら(1 9 9 6)cystic loses o f the maxillomandibular region:MR imaging disting o f odontogenic keratocyst and ameloblastomas from other cist. AJR Am J Roentgenol166:943-949.
- Probst FA,Probst M,Pautke Ch,Kaltsi E,Otto S,et al. ら(2 0 1 5)Magnetic resonance imaging:角嚢胞性歯原性腫瘍と歯原性嚢胞とを区別するための有用なツール。 Br J経口Maxillofac Surg53:217-222.
- Rodu B,Tate AL,Martinez MG(1987)歯原性角化嚢胞における炎症の影響。 J経口Pathol16:518-521.
- Haring JI,van Dis ML(1988)Odontogenic keratocysts:a clinical,x線写真および組織学的研究。 口頭Surg口頭Med口頭Pathol66:145-153。
- Voorsmit RACA(1984)the incredible keratocyst. ナイメーヘン大学出身。
- Johnson NR,Batstone MD,Savage NW(2013)角膜嚢胞性歯原性腫瘍の管理と再発:系統的レビュー。 Oral Surg Oral Med Oral Pathol Oral Radiol116:271-276.
- Slusarenko da Silva Y(2016)wistarラットの顎で行われた単皮質欠損に対するcarnoy溶液の効果の組織学的分析。 サンパウロ大学出身。
引用
Slusarenko da Silva Y,Naclério-Homem MG(2018)原発性および非Syndromic歯原性ケラトサイトの保存的治療:実践の概要。 Int Jの口頭凹みの健康4:070。 doi.org/10.23937/2469-5734/1510070
div