19.11:ラセミ化
光学活性ビフェニル誘導体(セクション13-5A)は、いつでも二つの芳香族環が中心結合の周りの回転によって同一平面配置を通過する場合にラセミ化される。 これは、2,2′-オルト置換基が非常に大きくない限り、熱によって多かれ少なかれ容易にもたらすことができる。不斉炭素原子を有する化合物がラセミ化される方法はより複雑である。
不斉炭素原子を有する化合物がラセミ化される方法はより複雑である。 一つの可能性は、四つの基に結合した四面体のキラル炭素が、結合を壊すことなく平面的でアキラルになることであろう。 理論的な計算は、これがキラル四価炭素の可能性の高いプロセスではないことを示していますが、我々が見るように、それはキラル炭素と三つの基に結合している他のキラル原子で発生しません:
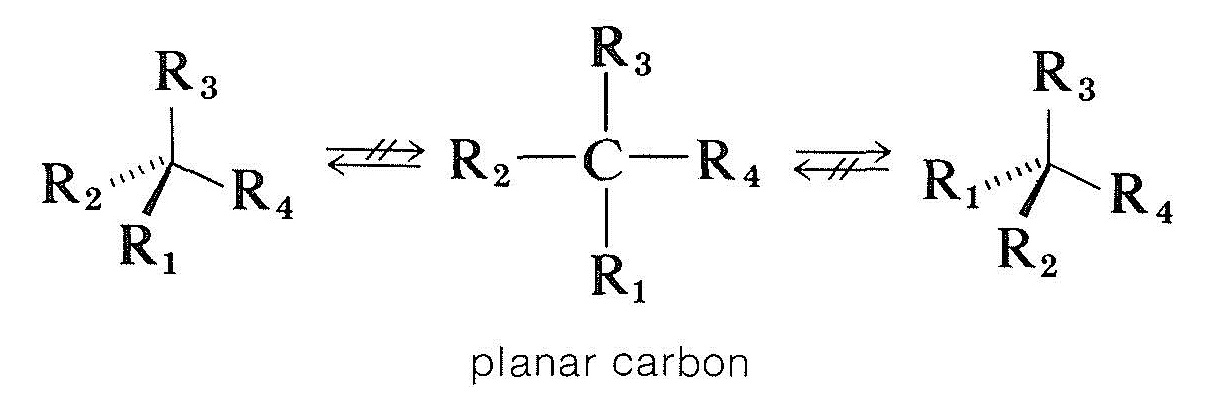
Α炭素が不斉であるタイプ\(\ce{-CHC=O}\)の光学活性カルボニル化合物は、酸と塩基の両方によってラセミ化され、セクション17-1から我々は、キラル炭素と他のキラル原子の両方によってラセミ化されています。これがenolizationに関連していることを確認してください。 エノールまたはエノラート陰イオンのいずれかの形成は、エノールの微量のみが任意の時点で存在している場合でも、最終的にはすべての化合物がラセミ化されるように、\(\アルファ\)炭素の非対称性を破壊する。 しかし、この機構は、\(\alpha\)水素が存在することと、対称中心がこの\(\alpha\)炭素に位置することの両方を必要とする。 それ以外の場合、酸および塩基はラセミ化を触媒するのに効果がない。
.jpg?revision=1)
光学活性な二次ハロゲン化物とハロゲンを担持するキラル炭素とのラセミ化(例えば、ハロゲンを担持するキラル炭素とのラセミ化)
.jpg?revision=1)
光学活性な二次ハロゲン化物,2-クロロブタン)ih溶液が発生することがあり、通常、溶媒がより極性であり、より良好にイオン化するほど、物質はラセミ化される。 おそらく\(S_\text{N}1\)プロセスによるハロゲン化物のイオン化が原因であり、これは確かに極性溶媒によって促進されるであろう(Section8-6)。 このようなイオンがアニオンと再結合すると、\(D\)と\(L\)の鏡像異性体を形成する確率が等しくなります。\(D\)と\(L\)の鏡像異性体を形成する確率が等しくなります。\(D\)と\(L\)の鏡像異性体を形成する確率が等しくなります。\(D\)と\(L\)の鏡像異性体:光学活性なハロゲン化物は\(s_\text{N}2\)機構によってラセミ化することもできます。
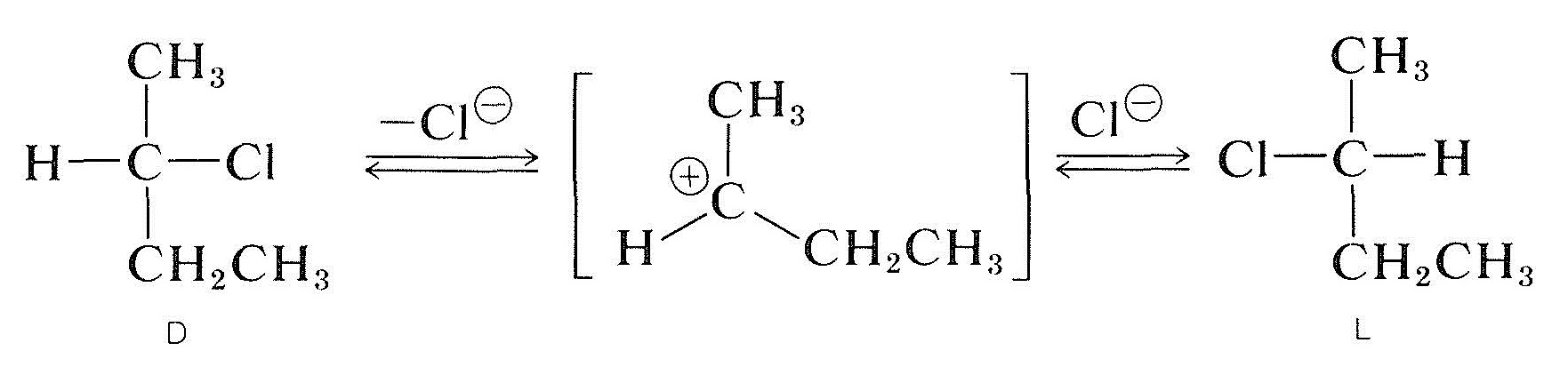
光学活性なハロゲン化物はまた、\(s_\text{N}2\)機構によってラセミ化することもできます。 溶解した塩化リチウムを含む2-プロパノン中の活性2-クロロブタンの溶液はラセミ体となる。 塩化物イオンによるハロゲン化物の塩化物の変位は、置換を受けている原子での配置を反転させる(セクション8-5参照)。 第二の置換は、元の鏡像異性体を再生成する。 最終的には、この前後のプロセスは、\(D\)と\(L\)フォームの等しい数を生成します。:不斉アルコールはしばしば強酸によってラセミ化される。
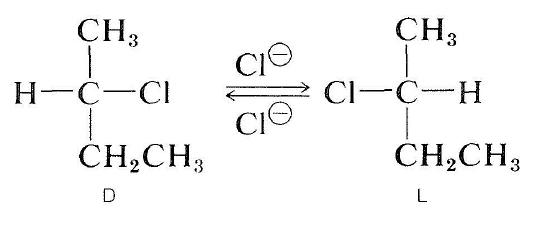
不斉アルコールはしばしば強酸によってラセミ化される。 間違いなく、イオン化が起こり、カルボカチオンと水との再結合は、いずれかの鏡像異性体につながる:
.jpg?revision=1&size=bestfit&width=590&height=243)
ハロゲン化物、アルコール、カルボニル化合物とは対照的に、炭化水素はラセミ化することが非常に困難である可能性がある。 これは、メチルエチルプロピルブチルメタン\(28\)のような四級不斉中心を持つ化合物に特に当てはまります。
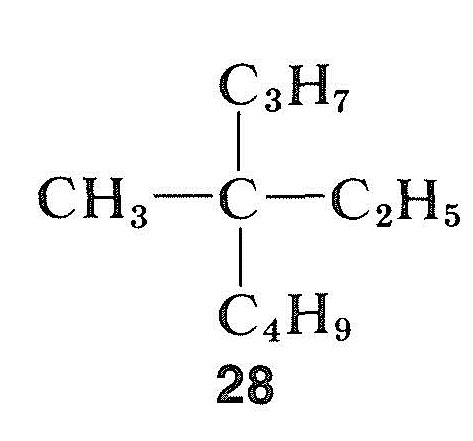
しかし、不斉炭素に水素原子を持つ炭化水素は、カルボカチオンまたはカルバニオンに変換できる場合にラセミ化されることがあります。 カルバニオン型ラセミ化の容易さは、結合した水素の酸性度および形成される中間カルバニオンの立体化学的安定性に依存する。 カルバニオン中間体の配置が反転すると、ラセミ化が起こります(セクション6-4Eも参照)。
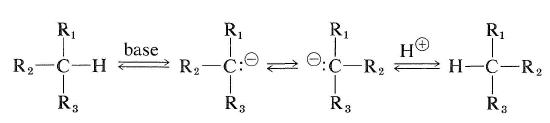
光学活性な炭化水素のラセミ化のカーボケーションタイプは、セクション10-9に記載されている交換反応によって起こることがあります。
投稿者と属性
- John D.RobertとMarjorie C. カゼリオ(1977)有機化学の基本原則、第二版。 W.A.Benjamin,Inc. 、メンロパーク、カリフォルニア州。 ISBN0-8053-8329-8. このコンテンツは、以下の条件の下で著作権で保護されています,”あなたは、個人のための許可を与えられています,教育,研究および非商業的な複製,配”