fenantren
- właściwości chemiczne Fenantrenu,zastosowania,produkcja
- nieliniowe wielopierścieniowe węglowodory aromatyczne
- Struktura molekularna
- właściwości chemiczne
- zastosowania
- preparat
- właściwości chemiczne
- właściwości chemiczne
- Właściwości fizyczne
- zastosowania
- wykorzystuje
- definicja
- metody produkcji
- Synthesis Reference(s)
- Opis ogólny
- powietrze & reakcje wodne
- profil reaktywności
- zagrożenie dla zdrowia
- zagrożenie pożarowe
- profil bezpieczeństwa
- potencjalna ekspozycja
- Rakotwórczość
- źródło
- Los środowiskowy
- Wysyłka
- metody oczyszczania
- Usuwanie odpadów
właściwości chemiczne Fenantrenu,zastosowania,produkcja
nieliniowe wielopierścieniowe węglowodory aromatyczne
fenantren jest najprostszym nieliniowym wielopierścieniowym węglowodorem aromatycznym o strukturze pierścienia trzy benzenowego, będącym izomerem antracenu. W 1872 E. Ostermayer et al zidentyfikował fenantren w frakcji oleju antracenowego w destylacie smoły węglowej, będąc jednym z produktów przetwarzania smoły węglowej. W wysokotemperaturowej smole węglowej zawartość fenantrenu jest wtórna tylko naftalenowi, wynosząca około 4 ~ 6%, głównie skoncentrowana we frakcjach oleju antracenowego. Aktywność chemiczna fenantrenu jest silniejsza niż naftalenu, ale jest słabsza niż antracenu, a reakcje utleniania i dodawania mogą również występować w pozycjach 9 i 10.
fenantren jest bezbarwnym kryształem z połyskiem, a fenantren wytrącony z etanolu jest bezbarwnym kryształem monoklinicznym. Fenantren jest kryształem podobnym do liści o gęstości względnej 1.179 (25/4 ℃) i współczynnik załamania światła 1,6450, temperatura topnienia 101 ° C i temperatura wrzenia 340 °C. może podlegać sublimacji, jest nierozpuszczalny w wodzie, słabo rozpuszczalny w etanolu, rozpuszczalny w eterze, benzenie, kwasie octowym, chloroformie, czterochlorku węgla i dwusiarczku węgla. Roztwór wykazuje niebieską fluorescencję. 1, 4, 5, 8-pozycje są takie same, znane jako α-pozycja; 2, 3, 6, 7-Pozycja są również takie same, znane jako β-pozycja; 9, 10-pozycje są takie same, znane jako ?pozycji. Jego właściwości chemiczne znajdują się między naftalenem a antracenem. Może również mieć reakcję addycyjną w pozycji 9, 10, ale nie tak łatwą jak antracen. Utlenianie występuje również w pozycji 9, 10 z utlenianiem dając fenantrenekwinon. Mogą również wystąpić reakcje podstawienia. Można go również otrzymać poprzez oddzielenie od frakcji oleju antracenowego oleju ze smoły węglowej. Fenantren może być stosowany do produkcji pestycydów i barwników, ale może być również stosowany jako stabilizator wysokiej wydajności & pestycydy o niskiej toksyczności i bezdymne Materiały wybuchowe w proszku.
fenantren może być stosowany do produkcji barwników, leków i żywic po przetwarzaniu konwersji. Produkty utleniania fenantrenekwinon można stosować jako barwniki, fungicydy i inhibitory polimeryzacji; kwas 9, 10-bifenylowy dikarboksylowy stosuje się do produkcji żywicy poliestrowej i alkidowej; kwas 9, 10-dihydro-9-fenatroinowy jest hormonem stymulującym wzrost roślin; Perhydrofenantren wytwarzany przez uwodornienie fenantrenu może być stosowany do produkcji paliwa odrzutowego; jego sulfonowany produkt, kwas fenantrenosulfonowy może być stosowany jako spoiwo i garbnik.
roztwór macierzysty zawierający fenantren podczas produkcji rafinowanego antracenu metodą rozpuszczalnikową, po odzysku rozpuszczalnika i dalszej filtracji krystalizacyjnej, może dać surowy fenantren zawierający 40% fenantrenu.
surowy fenantren, po usunięciu pozostałości rozpuszczalników w kotle do topienia, a następnie rektyfikacji w wieży rektyfikacyjnej z 20 płytami teoretycznymi, frakcje od 335 do 340 °C są wycinane, a następnie chłodzenie, krystalizacja i filtrowanie w celu uzyskania przemysłowego fenantrenu o zawartości fenantrenu większej niż 70%. .
powyższe informacje zostały zebrane przez Tongtonga z Chemicalbook.
Struktura molekularna
struktura molekularna fenantrenu i antracenu są ze sobą podobne, a wszystkie atomy znajdują się w tej samej płaszczyźnie, ale nie w tej samej linii, będąc zamkniętym układem sprzężonym o właściwościach aromatycznych. Pozycje 1, 2, 3, 4, 10 i 5, 6, 7, 8, 9 w cząsteczkach odpowiadają sobie odpowiednio, ale istniały różnice w aktywności w pozycjach 5, wśród których 9 i 10 miały wyższą aktywność z podstawieniem, utlenianiem i dodawaniem występującym w pozycjach 9 i 10: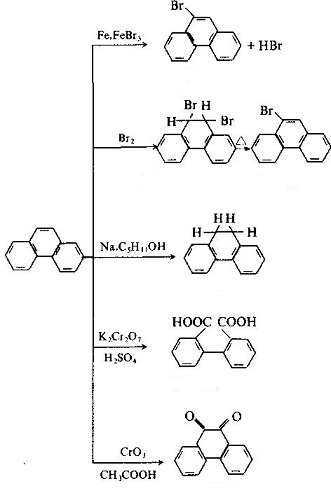
Fenantrenekwinon jest pestycydem stosowanym jako zaprawka do nasion bakteriobójczych, będąc w stanie zapobiegać parchowi pszenicy, twardemu smutowi i czarna plama ze słodkich ziemniaków.
fenantren Przemysłowy pochodzi z destylacji oleju antracenowego pochodzącego z destylatu smoły węglowej. Wiele rodzajów produktów naturalnych (takich jak sterole) zawiera ten system pierścieniowy. Fenantren jest stosowany głównie w produkcji barwników, leków, wysokiej wydajności i niskiej toksyczności pestycydów i może być stosowany jako scyntylatory, bezdymny stabilizator proszku. Wiele pochodnych fenantrenu ma rakotwórcze działanie fizjologiczne. Takie jak: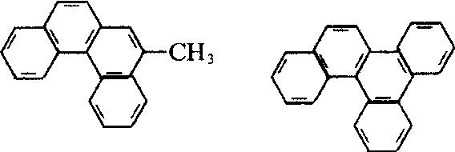
struktura molekularna 2-metylo-3, 4-benzofenantrenu i 1, 2, 3, 4-dibenzofenu
właściwości chemiczne
pojawia się jako białe błyszczące i fluorescencyjne kryształy płatków. Nie jest rozpuszczalny w wodzie, słabo rozpuszczalny w etanolu, rozpuszczalny w eterze, kwasie octowym, benzenie, czterochlorku węgla i dwusiarczku węgla.
zastosowania
może być stosowany do produkcji fenantrenekwinonu, żywicy syntetycznej, pestycydów i konserwantów i tak dalej.
fenantren, poprzez utlenianie, może dać fenantrenekwinon, który ma zastąpić organiczne pestycydy merkurialne ceresin i gallotox. Kwas bifenylowy otrzymany z jego utleniania można wykorzystać do przygotowania żywicy alkidowej. Utlenianie fenantrenu może również dawać bezwodnik, cykloheksanon i fenol. Produkty chlorowania fenantrenu mogą być stosowane do wytwarzania niepalnych izolatorów elektrycznych i impregnatów. Sulfonowany kwas fenantrenosulfonowy może być wykonany ze spoiwa, garbowania i tak dalej. Ale w rzeczywistości większość z tych aplikacji nie została jeszcze opracowana. W przemyśle papierniczym fenantren może być stosowany jako środek przeciwzmarszczkowy do masy celulozowej; może być również stosowany do materiałów wybuchowych nitroglicerynowych i stabilizatora nitrocelulozy oraz do produkcji bomby dymnej; stały tlenek fenantrenu może być wykonany z doskonałych ognioodpornych materiałów izolacyjnych i wypełniaczy. W medycynie fenantren może być stosowany do syntezy alkaloidów-morfiny i kofeiny, morfiny dimetylowej, a także leków o specjalnym fizjologicznym działaniu na wiele narządów rozrodczych. W przemyśle barwników fenantren może być wykonany z 2-aminofenantrenu chinonu, benzantronu, barwnika redukującego siarczki (niebieski BO, Czarny BB i brązowy) i tak dalej. Ponadto przemysł tworzyw sztucznych, syntetyczne garbniki i fenantren, w wysokiej temperaturze i pod wysokim ciśnieniem, mogą ulec uwodornieniu, aby uzyskać hydrofenantren, będący paliwem starszych samolotów odrzutowych.
do oznaczania masy cząsteczkowej i syntezy związków organicznych .
preparat
fenantren jest stosunkowo wysoką zawartością smoły węglowej, stanowiącą 5% smoły węglowej, ustępując jedynie zawartości naftalenu. Olej antracenowy w zakresie frakcji 300-360 ℃ smoły węglowej ma najwyższą zawartość Fenantrenu, a następnie antracenu i karbazolu i tak dalej. Metodą ekstrakcji fenantrenu jest zwykle wysyłanie oleju antracenowego do chłodzenia, krystalizacji, a następnie Filtracja próżniowa lub separacja odśrodkowa do separacji oleju. Stosunkowo duża ilość rozpuszczalnych fenoli w olejach może być odzyskiwana metodą destylacji precyzyjnej. Otrzymany kryształ nazywa się surowym antracenem, który zawiera 25-30% antracenu, 22-25% karbazolu i 30% fenantrenu. Surowy antracen może być poddany ekstrakcji ciężkiego benzenu, chłodzeniu, filtracji z filtratem na parze z rozpuszczalnika przed rekrystalizacją i filtracją. Weź filtrat do destylacji, abyśmy mogli uzyskać przemysłowy fenantren z sulfonowaniem, aby uzyskać drobny fenantren.
właściwości chemiczne
białe kryształy
właściwości chemiczne
fenantren jest białą substancją krystaliczną. Słaby zapach aromatyczny. Wielopierścieniowe węglowodory aromatyczne (WWA) są związkami zawierającymi wiele pierścieni benzenowych i są również nazywane wielopierścieniowymi węglowodorami aromatycznymi.
Właściwości fizyczne
bezbarwne, monokliniczne kryształy o słabym, aromatycznym zapachu
zastosowania
fenantren to wielopierścieniowe węglowodory aromatyczne, zanieczyszczenie środowiska.
wykorzystuje
znakowane wielopierścieniowe węglowodory aromatyczne jako mikropolutanty.
definicja
ChEBI: Policykliczny węglowodór aromatyczny składający się z trzech skondensowanych pierścieni benzenowych, który bierze swoją nazwę od dwóch terminów „fenyl” i ” antracen.”
metody produkcji
fenantren występuje w smole węglowej i może być izolowany z kilku rodzajów ropy naftowej.
Synthesis Reference(s)
Journal of Heterocyclic Chemistry, 30, p. 291, 1993 DOI: 10.1002/jhet. 5570300151
The Journal of Organic Chemistry, 18, P. 801, 1953 DOI: 10.1021/jo50013a004
Tetrahedron Letters, 15, p. 495, 1974
Opis ogólny
bezbarwne kryształy monokliniczne o słabym aromatycznym zapachu. Roztwory wykazują niebieską fluorescencję.
powietrze & reakcje wodne
nierozpuszczalny w wodzie.
profil reaktywności
fenantren może reagować z materiałami utleniającymi .
zagrożenie dla zdrowia
Ostra toksyczność doustna fenantrenu jest low.It jest bardziej toksyczny niż antracen. Doustna wartość LD50 u myszy jest podawana w dawce 700 mg / kg. Może powodować guz w skórze w miejscu aplikacji.Dowody rakotwórczości u zwierząt są jednak niewystarczające.
zagrożenie pożarowe
fenantren jest palny.
profil bezpieczeństwa
zatrucie drogą dożylną. Umiarkowanie toksyczny po spożyciu. Raport z mutacji. Fotouczulacz do skóry człowieka. Wątpliwy rakotwórczy z doświadczalnymi danymi dotyczącymi nowotworów i nowotworów w kontakcie ze skórą. Palne pod wpływem ciepła lub płomienia; może energicznie reagować z materiałami utleniającymi. Aby walczyć z ogniem, użyj wody, piany, CO2, suchej substancji chemicznej. Po podgrzaniu do rozkładu emituje ostry dym i drażniące opary
potencjalna ekspozycja
pył może tworzyć mieszankę wybuchową z powietrzem. Niekompatybilny z utleniaczami (chlorany, azotany, nadtlenki, nadmanganiany, nadchlorany, chlor, brom, fluor itp.); kontakt może spowodować pożar lub wybuch. Przechowywać z dala od materiałów alkalicznych, mocnych zasad, mocnych kwasów, tlenków, epoksydów.
Rakotwórczość
fenantren jest nieskuteczna jako aninitiator. Nie można go zaklasyfikować pod względem rakotwórczości u ludzi—klasa 3 według IARC i klasa D według IRIS, w oparciu o brak danych na temat ludzi i niewystarczające dane z pojedynczego badania gavag u szczurów oraz badań malowania skóry i iniekcji wmice.
źródło
wykryte w wodach gruntowych pod dawną instalacją zgazowania węgla w Seattle, WA przy stężeniu 130 µg/l (ASTR, 1995). Wykryto w 8 olejach napędowych w stężeniach od 0,17-110 mg/l przy średniej wartości 41,43 mg/l (Westerholm i Li, 1994) oraz w destylowanych rozpuszczalnych w wodzie frakcjach nowego i zużytego oleju silnikowego w stężeniach odpowiednio 1,9–2,1 i 2,1–2,2 µg/l (Chen i wsp., 1994). Lee et al. (1992) podano zakresy stężeń od 100 do 300 mg/L i od 15 do 25 µg/l w oleju napędowym i odpowiedniej fazie wodnej (woda destylowana),odpowiednio. Schauer et al. (1999) zgłaszane fenantrenu w oleju napędowym w stężeniu 57µg / G i w spalinach samochodów ciężarowych zasilanych olejem napędowym o średnim obciążeniu przy tempie emisji 93,1 µg/km.Zidentyfikowane w Kuwejcie i południowej Luizjanie ropy naftowej w stężeniach 26 i 70 ppm, odpowiednio (Pancirov i Brown, 1975). Olej napędowy otrzymany ze stacji paliw w Schlieren w Szwajcarii zawierał fenantren w szacunkowym stężeniu 327 mg / L (Schluep et al.,2001).
fenantren wykryto w oparach asfaltu przy średnim stężeniu 57,73 ng/m3 (Wanget al., 2001).
Thomas i Delfino (1991) zrównoważone wolne od zanieczyszczeń wody gruntowe zbierane z Gainesville, FL z poszczególnymi frakcjami trzech poszczególnych produktów ropopochodnych w temperaturze 24-25 °C przez 24 godziny. fazę wodną analizowano pod kątem związków organicznych za pomocą zatwierdzonej przez amerykańską EPA metody badania625. Fenantren wykryto tylko w rozpuszczalnej w wodzie frakcji oleju napędowego przy średnim stężeniu 17 µg/L.
na podstawie analizy laboratoryjnej 7 próbek smoły węglowej stężenia fenantrenu wynosiły od 3100 do 35 000 ppm (EPRI, 1990). Wykryto w 1-yr wieku warstwy smoły węglowej i luzem smoły węglowej w stężeniu anidentical 10,000 mg / kg (Nelson et al., 1996). Wysokotemperaturowa Tarka węglowa zawierała fenantren w średnim stężeniu 2,66% wagowych (McNeil, 1983). Zidentyfikowano również wysokotemperaturowe smoły węglowe w stężeniach od 7500 do 40 300 mg / kg (Arrendale and Rogers, 1981). Lee et al. (1992a) równowaga ośmiu smół węglowych z wodą destylowaną w temperaturze 25 °C. Maksymalne stężenie fenantrenu obserwowane w fazie wodnej wynosi 0,4 mg / L.
dziewięć dostępnych w handlu próbek kreozotu zawierało fenantren w stężeniach od 48 000 do 120 000 mg/kg (Kohler i wsp., 2000).
typowe stężenie fenantrenu w ciężkim oleju pirolitycznym wynosi 2,5% wag. (Chevron Phillips, maj 2003).
Los środowiskowy
biologiczny. Katechol jest głównym metabolitem w bakteryjnej degradacji fenantrenu.Pośrednie produkty uboczne obejmują kwas 1-hydroksy-2-naftoesowy, 1,2-dihydroksynaftalen i kwas salicylowy (Chapman, 1972; Hou, 1982). Doniesiono, że Beijerinckia, w Warunkach aerobiku, rozkłada fenantren do cis-3,4-dihydroksy-3,4-dihydrofenantracenu (Kobayashiand Rittman, 1982).
gleba. Zgłoszone okresy półtrwania fenantrenu w Kidman sandyloam i McLaurin sandyloam są odpowiednio 16 i 35 d (Park et al., 1990). Manilal i Alexander (1991) opisali Half-life of 11 d in a Kendaia soil.
wody powierzchniowe. W zbiorniku wód powierzchniowych o głębokości 5 m obliczone okresy półtrwania dla bezpośredniej fotochemicznej transformacji na szerokości 40 ° N w środku lata w południe wynosiły odpowiednio 59 i 69 d bez podziału osad-woda (Zepp i Schlotzhauer, 1979).
Fotolityczne. Wydajność dwutlenku węgla na poziomie 24,2% uzyskano, gdy fenantren adsorbowany żel onsilica został napromieniowany światłem (λ >290 nm) przez 17 godzin (Freitag et al., 1985). W 2-wkeksperyment, fenantren zastosowany do zawiesin glebowo-wodnych w warunkach tlenowych i beztlenowych dał 14co2 plony 7,2 i 6.3%, odpowiednio (Scheunert et al., 1987). Matsuzawa etal. (2001) badał fotochemiczną degradację pięciu wielopierścieniowych węglowodorów aromatycznych w postaci cząstek stałych odkładających się na ziemi i w różnych składnikach gleby. Degradację fotochemiczną pod wpływem sztucznego światła słonecznego uzyskano za pomocą lampy ksenonowej o mocy 900 W.Światło z tej lampy przepuszczane było przez szklany filtr w celu wyeliminowania światła o krótszych długościach fal (λ2. Ponadto zastosowano symulator słoneczny wyposażony w lampę ksenonową o mocy 300 W, aby zapewnić maksymalną intensywność światła słonecznego obserwowaną w Tokio (szerokość geograficzna 35,5 °N). Okres półtrwania fenantrenu w pyle zawieszonym oleju napędowego z wykorzystaniem źródeł 900 i 300 W wynosił odpowiednio 4,29 i 60,63 h. Następujące okresy półtrwania zostały określone dla fenantrenu adsorbowanego na różnych składnikach gleby przy użyciu aparatury 900 W: 3,04 h dla kwarcu, 2,90 h dla skalenia, 1,15 h dla kaolinitu, 4,97 h dla montmorylonitu, 3,26 h dla żelu krzemionkowego i 1,17 h dla tlenku glinu.
chemiczne/fizyczne. Wodną chlorowanie fenantrenu przy pH 8,8), tlenku fenantrenu-9,10 -, fenantrenu-9,10-dionu i 9,10-dihydrofenantrenodiolu zidentyfikowano jako główne produkty(Oyler i wsp.,1983). Zasugerowano, że chlorowanie fenantrenu w wodzie wodociągowej stanowiło obecność chloro – i dichlorofenantrenów (Shiraishi et al., 1985).
Wysyłka
UN3077 substancje niebezpieczne dla środowiska, stałe, N. O. s., Klasa Zagrożenia: 9; etykiety: 9-Różne materiały niebezpieczne, wymagana nazwa techniczna.
metody oczyszczania
prawdopodobne zanieczyszczenia obejmują antracen, karbazol, fluoren i inne wielopierścieniowe węglowodory. Oczyść go przez destylację z sodu pod próżnią, Gotowanie z bezwodnikiem maleinowym w ksylenie, krystalizację z kwasu octowego, sublimację i topienie strefowe. Był również wielokrotnie rekrystalizowany z EtOH, * benzenu lub eteru pet (b 60-70o), a następnie suszony w próżni nad P2O5 w pistolecie Abderhalden. Feldman, Pantages i Orchin oddzielili większość zanieczyszczeń antracenowych przez refluksowanie fenantrenu (671g) bezwodnikiem maleinowym (194g) w ksylenie (1,25 L) Pod azotem przez 22 godziny, a następnie przefiltrowano. Przesącz ekstrahowano wodnym 10% NaOH, fazę organiczną oddzielono i rozpuszczalnik odparowano. Pozostałość po mieszaniu przez 2 godziny z 7G sodu destylowano w próżni, a następnie dwukrotnie rekrystalizowano z 30% *benzenu w EtOH. Następnie rozpuszczono go w gorącym kwasie octowym (2,2 mL/g) i powoli dodawano do niego wodny roztwór CrO3 (60 g w 72 ml H2O plus 2,2 L kwasu octowego), a następnie powoli dodawano conc H2SO4 (30 ml). Mieszaninę poddano działaniu refluksu przez 15 minut, rozcieńczono równą objętością wody i ochłodzono. Osad odsączono, przemyto wodą, wysuszono i destylowano, a następnie dwukrotnie rekrystalizowano z EtOH. Dalsze oczyszczanie jest możliwe przez chromatografię z roztworu CHCl3 na aktywowanym tlenku glinu, z *benzenem jako eluentem i przez rafinację strefową. Pikrat (1:1) tworzy złotożółte igły z m 146o, a styfnian (1:1) mA m 138-139o (płytki lub igły odpowiednio z EtOH lub EtOH/H2o).
Usuwanie odpadów
skonsultuj się z organami regulacyjnymi ds. środowiska w celu uzyskania wskazówek dotyczących dopuszczalnych praktyk usuwania. Wytwórcy odpadów zawierających to zanieczyszczenie (≥100 kg/mo) muszą przestrzegać przepisów EPA dotyczących przechowywania, transportu, przetwarzania i usuwania odpadów.