7.18: Vinil Halogenetos e teluretos aromáticos Halogenetos
Nucleophilic substituição no teluretos aromáticos halogenetos
daremos uma olhada em alguns detalhes na estrutura de clorobenzeno. Bromobenzeno e iodobenzeno são iguais. A maneira mais simples para desenhar a estrutura de clorobenzeno é:
Para entender clorobenzeno corretamente, você precisa cavar um pouco mais fundo do que isso. Existe uma interação entre os elétrons deslocalizados no anel benzeno e um dos pares solitários no átomo de cloro. Isto se sobrepõe ao sistema de elétrons de anel deslocalizado . . .
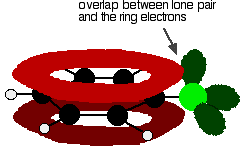
dar uma estrutura como esta:
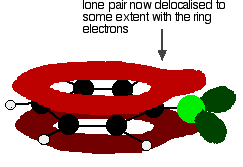
Esta deslocalização não é, de forma completa, mas não deixa de ter um efeito significativo sobre as propriedades do carbono-cloro bond e a polaridade da molécula. A deslocalização introduz alguma ligação extra entre o carbono e o cloro, tornando a ligação mais forte. Isto tem um grande efeito sobre as reações de compostos como o clorobenzeno.
há também algum movimento de elétrons para longe do cloro para o anel. O cloro é bastante eletronegativo e geralmente atrai elétrons na ligação carbono-cloro para si mesmo. Neste caso, isto é compensado em certa medida pelo movimento de elétrons de volta para o anel na deslocalização. A molécula é menos polar do que seria de esperar.halogenetos de aril simples como o clorobenzeno são muito resistentes à substituição nucleofílica. É possível substituir o cloro por-OH, mas apenas em condições industriais muito graves-por exemplo, a 200°C e 200 atmosferas. No laboratório, essas reações não acontecem. Há duas razões para isso-dependendo de qual dos mecanismos acima mencionados você está falando.
- the extra strength of the carbon-halogen bond in aryl halides: The carbon-chlorine bond in chlorobenzene is stronger than you might expect. Há uma interação entre um dos pares solitários no átomo de cloro e os elétrons de anel deslocalizados, e isso fortalece a ligação. Ambos os mecanismos acima envolvem a quebra da ligação carbono-halogéneo em alguma fase. Quanto mais difícil For quebrar, mais lenta será a reação.
- repulsão pelos elétrons do anel: isto só se aplica se o íon hidróxido atacou o clorobenzeno por um mecanismo como o primeiro descrito acima. Nesse mecanismo, o íon hidróxido ataca o carbono ligeiramente positivo ao qual o átomo de halogênio Está ligado.Se o átomo de halogéneo estiver ligado a um anel de benzeno, o íon de hidróxido de entrada será confrontado com os elétrons de anel deslocalizados acima e abaixo desse átomo de carbono. O íon hidróxido negativo será simplesmente repelido. Esse mecanismo em particular é simplesmente um não-arranque!