a Vitamina C: Antioxidante Agente
Redox metabolismo e propriedades antioxidantes da vitamina C
os radicais Livres e antioxidantes desempenham um papel duplo como tóxicos e compostos benéficos, em processos metabólicos e em resposta a estímulos exógenos. São produzidos a partir de atividades metabólicas normais ou de fatores ambientais (poluição, fumaça de cigarro e radiação). Quando uma sobrecarga de radicais livres não pode ser removida, a sua acumulação no corpo gera stress oxidativo . O estresse oxidativo ocorre quando a formação de radicais livres excede a capacidade de proteção contra eles. Este processo leva ao desenvolvimento de doenças crônicas e degenerativas, como câncer, doenças autoimunes, envelhecimento, catarata, artrite reumatóide, doenças cardiovasculares e neurodegenerativas . Um antioxidante é uma molécula que impede a oxidação de outras moléculas. Processo de oxidação é uma reação química que produz radicais livres, levando a reações em cadeia que podem danificar as células. O efeito antioxidante da vitamina C foi bem documentado . A vitamina C é um poderoso antioxidante com capacidade para doar um átomo de hidrogênio e formar um radical relativamente estável sem ascorbilo. Vitamina E, vitamina C e β-caroteno são conhecidos como vitaminas antioxidantes que são sugeridas para diminuir os danos oxidativos e reduzir o risco de certas doenças crônicas. As doenças, como as doenças cardiovasculares, estão associadas a concentrações inadequadas de ácido L-ascórbico, tocoferol e β-caroteno em estudos epidemiológicos. A vitamina C também aumenta a absorção de ferro através da redução de Fe3+ para Fe2+ a partir de fontes de ferro não heme . Na presença de íons redox ativos (ferro, cobre), a vitamina C atua como um prooxidante, contribuindo para a formação de radicais hidroxilo, que podem levar à oxidação de lípidos, DNA ou proteínas . Existem diferentes mecanismos para aliviar o stress oxidativo e reparar macromoléculas danificadas. Os antioxidantes enzimáticos e nãoenzimáticos têm papéis importantes na remoção de radicais livres e espécies reactivas de oxigénio (ROS). As enzimas antioxidantes, catalase (CAT), superóxido dismutase (SOD), glutationa redutase (GR), glutationa peroxidase (GSHpx) e, nas plantas, ascorbato peroxidase (AA-px) e o nonenzymatic antioxidantes, incluindo a glutationa (GSH) e ascorbato (ASC), tem sido mostrado para ser significativamente afetado pelo estresse oxidativo . Os compostos antioxidantes podem impedir a formação descontrolada de radicais livres ou inibir a sua reacção com locais biológicos; além disso, a destruição da maioria dos radicais livres depende da oxidação de antioxidantes endógenos, principalmente por eliminação e redução de moléculas . Pensa-se que a vitamina C é um importante antioxidante solúvel em água, que é relatado para neutralizar ROS e reduzir o estresse oxidativo .a vitamina C é um potente agente redutor e necrófago de radicais livres em sistemas biológicos . Está envolvido na primeira linha de defesa antioxidante, protegendo membranas lipídicas e proteínas de danos oxidativos. Como uma molécula solúvel em água, a vitamina C pode funcionar tanto dentro como fora das células, e pode neutralizar radicais livres e prevenir danos radicais livres. A vitamina C é uma excelente fonte de electrões para os radicais livres que procuram um electrão para recuperar a sua estabilidade. A vitamina C pode doar electrões a radicais livres e atenuar a sua reactividade .
A vitamina C demonstrou ser um necrófago eficaz contra espécies de oxigênio e óxido de nitrogênio, tais como o íon radical superóxido, peróxido de hidrogênio, o radical hidroxilo e oxigênio singlet. Esta propriedade da vitamina C tem processos vitais na proteção dos componentes celulares contra danos induzidos por radicais livres. Além disso, a vitamina C é eficaz na regeneração da forma antioxidante da vitamina E reduzindo os radicais tocoferoxilo. Este processo protege membranas e outros compartimentos da célula de danos induzidos por radicais livres (Figura 2). Ascorbato peroxidase (APX) é uma enzima que reduz o H2O2 à água utilizando ascorbato como dador de electrões. Monodehidroascorbato é um ascorbato oxidado que é regenerado pela redutase da monodehidroascorbato (MDAR). Radicais de monodehidroascorbato rapidamente desmembram-se em ascorbato e dehidroascorbato. Dehydroascorbate is reduced to ascorbate by dehydroascorbate reductase in the presence of GSH, yielding oxidized glutathione (GSSG). It is reduced by glutathione reductase (GR) using nicotinamide adenine dinucleotide phosphate hydrogen (NADPH) as an electron donor. Dehydroascorbate may be reduced nonenzymatically or catalyzed by proteins with dehydroascorbate reductase (DHAR) activity.
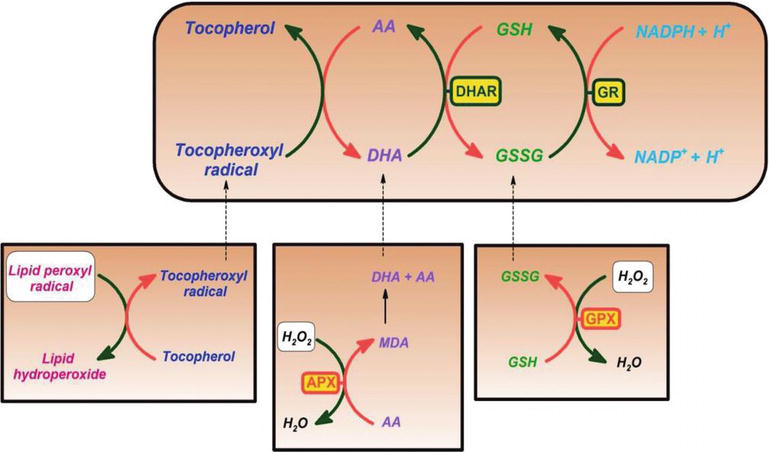
Figure 2.
xmlns:mml=”http://www.w3.org/1998/Math/MathML” xmlns:xlink=”http://www.w3.org/1999/xlink” xmlns:xsi=”http://www.w3.org/2001/XMLSchema-instanceAscorbate and redox cycling antioxidants. AA, ascorbate; DHA, dehydroascorbate; DHAR, semidehydroascorbate reductase; GSH, glutathione; GSSG, semi-glutathione reductase; GR, glutathione reductase; APX, ascorbate peroxidase; and GPX, glutathione peroxidase .
Glutathione-ascorbate cycle operates in the cytosol, mitochondria, plastids, and peroxisomes in plants . Sugere-se que o ciclo glutationa-ascorbato desempenha um papel fundamental na desintoxicação do H2O2, devido às elevadas concentrações de glutationa, ascorbato e NADPH nas células vegetais. Outras enzimas, como ascorbato e glutationa peroxidases, que utilizam tioredoxinas ou glutaredoxinas como substratos redutores, também desempenham papel na remoção de H2O2 nos vegetais (Figura 2).
A vitamina C também forma o radical semidehydroascorbil, um radical de vida relativamente longa, na regeneração da vitamina E da sua forma radical, bem como na eliminação dos radicais. As células vegetais e animais contêm uma enzima da redutase dependente do NADH (EC 1.6.5.4), que reduz o radical à vitamina C utilizando o NADH como agente redutor (Figura 2). Pode decompor-se irreversivelmente em ácido diketoglucónico ou pode ser convertido em ascorbato numa reacção dependente da glutationa .a vitamina C Doa elétrons de alta energia para neutralizar radicais livres, e é oxidada a ácido desidroascórbico. O ácido desidroascórbico pode ser convertido de volta em ácido ascórbico para reutilização ou pode ser metabolizado, liberando mais elétrons. Embora a vitamina C seja absorvida pelo intestino através de um transportador de vitamina C dependente do sódio, a maioria das células transportam a vitamina C numa forma oxidada (ácido desidroascórbico) através do transportador de glucose 1. O ácido desidroascórbico é reduzido para gerar ácido ascórbico no interior da célula, protegendo as mitocôndrias de danos oxidativos induzidos por radicais livres (Figuras 2 e 3). Radicais livres altamente reativos (ex., RO–, RO2–, OH–, NO2) são reduzidos pelo ascorbato, e o radical de ascorbilo recentemente gerado é pouco reativo. O ascorbato também pode retirar espécies não-reactivas do sistema radicular, derivadas do peroxinitrite, tais como o ácido hipocloroso, o ozono e os agentes nitrados. A vitamina C é um catalisador monossacarídeo de oxidação-redução (redox) encontrado em animais e plantas. O efeito antioxidante da vitamina C deve-se à sua capacidade de doar electrões tanto do segundo como do terceiro carbono. Durante a evolução dos primatas, uma das enzimas necessárias para fazer ácido ascórbico foi perdida por mutação, os seres humanos devem obtê-la a partir da dieta ; a maioria dos animais pode sintetizar esta vitamina em seus corpos e não requerê-la em suas dietas . A vitamina C é necessária na conversão do procolagénio em colagénio através da oxidação de resíduos de prolina em hidroxiprolina. Em outras células, é mantido em sua forma reduzida por reação com glutationa . Como mostrado nas Figuras 2 e 3, O ácido ascórbico é um catalisador redox que pode reduzir, e assim neutralizar, ROS como o peróxido de hidrogênio (H2O2) (Figuras 2 e 3).
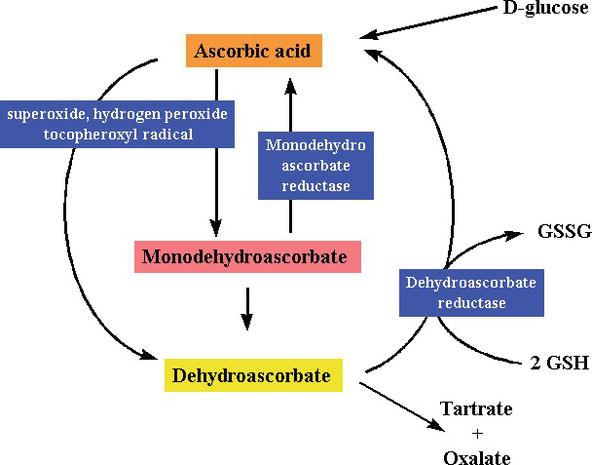
Figure 3.
xmlns:mml=”http://www.w3.org/1998/Math/MathML” xmlns:xlink=”http://www.w3.org/1999/xlink” xmlns:xsi=”http://www.w3.org/2001/XMLSchema-instanceSynthesis and degradation ofl-ascorbic acid in plant tissues .
Ascorbic acid has direct antioxidant effects, and also it is a substrate for the redox enzyme ascorbate peroxidase, that is particularly important in stress resistance in plants. O ácido ascórbico está presente em níveis elevados em todas as partes das plantas, especialmente em cloroplastos que atingem concentrações de 20 mM lá . O radical livre de dehidroascorbato (DHA) e o radical livre de ascorbato (AFR), como produto intermédio, o radical livre de ascorbato (AFR), que são reversíveis, produzem oxidações de um electrão a partir do ascorbato (Figura 4). De acordo com o modelo geralmente assumido de remoção enzimática de ROS, SOD cataliza anião superóxido para H2O2 e oxigênio; então H2O2 é reduzido em água e oxigênio molecular pelo gato. CAT turnover number is very high, but its affinity for H2O2 is relatively low, and consequently a certain amount of H2O2 remains in the cell.
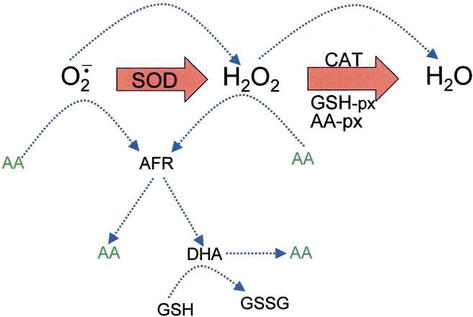
Figure 4.
xmlns:mml=”http://www.w3.org/1998/Math/MathML” xmlns:xlink=”http://www.w3.org/1999/xlink” xmlns:xsi=”http://www.w3.org/2001/XMLSchema-instanceThe role of AA in the detoxification of ROS. Blue dotted lines indicate nonenzymatic reactions.
H2O2 can react with superoxide anion formed in oxidative metabolism generating the highly reactive hydroxyl radical. GSH peroxidases (GSH-px) and AA peroxidases (AA-px) are capable of scavenging H2O2 due to their high affinity for H2O2. The cooperativity of SOD, CAT, and peroxidases ensures low amounts of superoxide anion and H2O2 and limiting the risk of hydroxyl radical formation (Figure 5).

Figure 5.
xmlns:mml=”http://www.w3.org/1998/Math/MathML” xmlns:xlink=”http://www.w3.org/1999/xlink” xmlns:xsi=”http://www.w3.org/2001/XMLSchema-instanceFoyer-Halliwell-Asada cycle .