Cardiologia
defeitos do septo Ventricular
defeitos do septo ventricular isolados (VSD) constituem 25-30% de todas as doenças cardíacas congênitas (DCH) em crianças. O VSD pode estar presente em 50% dos CHDs, como na tetralogia de Fallot, ventrículo direito de saída dupla, truncus arteriosus e outros.aproximadamente 70% de todos os VSDs estão presentes na porção membranosa do septo inter-ventricular, cerca de 20% estão na porção muscular, e os defeitos restantes estão na entrada ou na saída do septo ventricular. O VSD inlet é geralmente uma parte do defeito do septo septal atrioventricular (canal AV). O VSD (supra-cristal) é mais comum (cerca de 20%) na população oriental (ou população da Ásia Oriental).
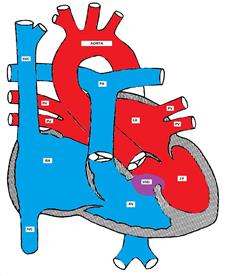
Figura mostrando uma comunicação interventricular
Fisiopatologia
Com um pequeno porte VSD, “restritiva VSD,”a direção e a magnitude do shunt depende do tamanho da CIA e o gradiente de pressão entre o lado esquerdo e os ventrículos direito. A natureza restritiva do VSD mantém o gradiente de pressão entre os dois ventrículos.com um VSD grande, o buraco não é restritivo e a pressão em ambos os ventrículos é quase igual. A direção e magnitude do shunt dependem da diferença relativa entre as resistências pulmonares e vasculares sistêmicas. Na vida fetal, a resistência pulmonar é maior do que a resistência sistémica. À medida que os pulmões se expandem com a primeira respiração, a resistência pulmonar diminui significativamente e o fluxo pulmonar aumenta. A resistência pulmonar continua a diminuir até atingir a razão normal para o adulto de 1:10 em 4 a 8 semanas (ver figura).o shunt prolongado da esquerda para a direita conduz a um aumento gradual da pressão pulmonar e a hipertensão pulmonar eventualmente desenvolve-se. À medida que a diferença de pressão entre os sistemas sistêmico e pulmonar diminui, o fluxo através do shunt também diminui. Se a resistência vascular pulmonar exceder a resistência vascular sistémica, a direcção do shunt reverte e desenvolve-se cianose (síndrome de Eisenmenger). Isto pode desenvolver – se dentro de dois anos em crianças saudáveis e dentro de um ano em pacientes com síndrome de Down.
as apresentações clínicas
As Crianças com uma VSD pequena são geralmente assintomáticas. Um sopro cardíaco holossistólico ou decrescendo descoberto incidentalmente é a apresentação mais comum. O murmúrio é comumente descoberto com 2-4 semanas de idade, à medida que a resistência vascular pulmonar cai e a diferença de pressão entre os dois ventrículos torna-se notável (figura). A intensidade do sopro é inversamente proporcional ao tamanho do VSD devido ao aumento da turbulência e velocidade de fluxo produzida por um defeito menor. Uma emoção pode ser palpável em alguns casos. O defeito pode ser pequeno o suficiente para quase Fechar no final de um descrescendo sistólico murmur.
uma criança com um VSD grande pode ser assintomática nos primeiros dias / semanas de vida até que a resistência vascular pulmonar diminua. À medida que a resistência pulmonar diminui, o shunt da esquerda para a direita aumenta. O ventrículo direito é assim submetido a alta pressão e torna-se hipertrofiado enquanto o átrio esquerdo e o ventrículo esquerdo recebem mais volume e se tornam dilatados. O átrio direito não é geralmente afectado. A insuficiência cardíaca congestiva (ICC) pode desenvolver-se e apresentar-se como taquicardia, taquipneia, dispneia exercional, falta de ar e sudação durante a alimentação. O crescimento da criança também é muitas vezes Atrasado Por Causa da ingestão calórica fraca. Em alguns lactentes, especialmente aqueles com síndrome de Down, A resistência vascular pulmonar pode não diminuir significativamente. Estes lactentes podem não desenvolver ICC, mas apresentam um risco aumentado de desenvolver hipertensão pulmonar. Eles podem precisar de intervenção cirúrgica anterior para prevenir o agravamento da hipertensão pulmonar e o desenvolvimento precoce da síndrome de Eisenmenger.
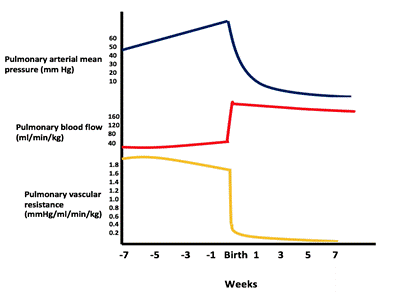
Figura mostrando a queda vascular pulmonar pressão de resistência e o aumento do fluxo sanguíneo pulmonar após o nascimento
Fazer o diagnóstico
- Um holosystolic murmúrio é ouvido na borda esternal esquerda, devido à turbulência através da CIA. A intensidade do sopro é inversamente proporcional à magnitude do shunt; quanto menor o shunt, mais alto o murmur e vice-versa.
- um decrescendo (antigo) murmúrio sistólico pode indicar um VSD pequeno e fechando. Há um fluxo diminuído na última parte da sistole e nenhum murmúrio é ouvido.um sopro apical médio-diastólico (rumble) pode ser ouvido devido ao aumento do fluxo através da válvula mitral (estenose mitral relativa). Isto indica que o VSD é suficientemente grande para causar um fluxo sanguíneo pulmonar excessivo, o que indica clinicamente insuficiência cardíaca congestiva (ICC). Esta ICC não é devida à disfunção da bomba como em adultos, mas devido ao aumento do fluxo sanguíneo pulmonar.um sopro diastólico precoce ouvido na borda superior esquerda do esterno em uma posição sentada poderia ser ouvido em um pequeno membranoso ou um VSD supra-cristal. Isto indica insuficiência aórtica devido ao prolapso de uma das válvulas aórticas aspira ao VSD secundário à sucção criada pelo jato de alta velocidade (efeito Venturi). um P2 Alto com separação estreita do S2 indica aumento da pressão vascular pulmonar e resistência que causaria o encerramento precoce da válvula pulmonar.um sopro diastólico precoce devido a insuficiência pulmonar pode ser ouvido se se desenvolver hipertensão pulmonar.a hipertensão pulmonar diminui o fluxo sanguíneo pulmonar e torna a ICC improvável (lua-de-mel antes do desenvolvimento da síndrome de Eisenmenger).pode ocorrer cardiomegalia e hepatomegalia se estiver presente ICC.as radiografias torácicas podem apresentar cardiomegalia e aumento da vascularidade pulmonar.
- EKG reflete o estado hemodinâmico e pode mostrar RVH, aumento auricular esquerdo e aumento ventricular esquerdo (o eletrocardiograma não é muito sensível em diferenciar LVH da dilatação LV). O átrio direito normalmente não é afectado.
- Ecocardiograma mostra a localização, tipo e tamanho do VSD. Ele também pode estimar o gradiente de pressão através do VSD. Os efeitos hemodinâmicos do VSD em diferentes câmaras podem ser elucidados. Também é importante procurar insuficiência aórtica (especialmente em VSD membranoso e supra-cristal) que pode indicar um dano precoce à válvula aórtica.a cateterização cardíaca raramente é necessária, mas pode medir a pressão/resistência pulmonar e ajudar a determinar a reactividade (e, portanto, operabilidade) da vasculatura pulmonar em caso de hipertensão pulmonar.
História Natural
enquanto mais de metade dos VSD de pequeno e médio tamanho se fecham espontaneamente, apenas cerca de 10% dos VSD de grande tamanho se fecham espontaneamente. O VSD muscular fecha-se pelo crescimento muscular. O VSD membranoso fecha pelo tecido do folheto da válvula tricúspide que forma um aneurisma que gradualmente se torna endotelializado. É pouco provável que os VSDs de entrada e supra-cristal (saída) se fechem espontaneamente. Em pacientes não operados com grande VSD, a síndrome de Eisenmenger pode desenvolver-se dentro de dois anos, mas pode desenvolver-se tão cedo quanto um ano em pacientes com síndrome de Down. Isto pode ser atribuído ao aumento da densidade vascular/alveolar e ao aumento da secreção de endostatina em doentes com síndrome de Down.
Gestão
crianças assintomáticas com VSD de pequeno ou médio tamanho só precisam de cuidados de suporte, com a expectativa de que o VSD irá fechar nos primeiros anos de vida. Se a ICC se desenvolver, o tratamento consiste em diuréticos, agentes redutores da carga, tais como inibidores da ECA e possivelmente digoxina. A insuficiência cardíaca nas rampas esquerda-direita deve-se à sobrecarga de volume na circulação pulmonar. Isto contrasta com os adultos com enfarte do miocárdio em que a insuficiência cardíaca se deve à disfunção da bomba. Em adultos com insuficiência cardíaca, a digoxina é utilizada para melhorar a função da bomba. No entanto, se a digoxina for utilizada no tratamento da ICC devido ao shunt da esquerda para a direita, actua principalmente para que o seu efeito colinérgico diminua a frequência cardíaca. A restrição de fluidos deve ser evitada, pois reduz a ingestão calórica e atrasa o crescimento. a terapêutica com oxigénio também deve ser evitada, uma vez que é um vasodilatador pulmonar e um vasoconstritor Sistémico. Isso pioraria os sintomas do shunt da esquerda para a direita. Os doentes com ICC persistente ou aqueles que estão a desenvolver hipertensão pulmonar requerem o encerramento cirúrgico do VSD. Se um paciente não é um candidato adequado para cirurgia, a bandagem da artéria pulmonar deve ser considerada até que a cirurgia pode ser feita (geralmente dentro do primeiro ano de vida). Recentemente, técnicas de trans-cateter têm sido usadas para fechar VSDs (especialmente VSDs musculares). o canal arterial, formado a partir do sexto arco aórtico embrionário, liga a aorta à artéria pulmonar. Normalmente fecha poucos dias após o nascimento. Uma elevada tensão do oxigénio e uma diminuição das prostaglandinas endógenas são factores importantes na indução do fecho ductal. Pela mesma razão, os inibidores da prostaglandina sintetase, como a indometacina, são eficazes na indução do fecho ductal e são frequentemente utilizados no período neonatal, especialmente em lactentes pré-termo.
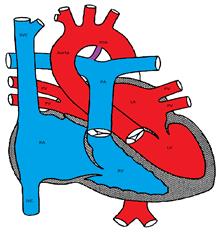
Figura mostrando a persistência do Canal Arterial
Fisiopatologia
Falha de fechamento do canal arterial leva a alterações hemodinâmicas semelhantes aos observados em VSD. A direcção e extensão do shunt no PDA depende do tamanho do PDA e da resistência vascular sistémica e pulmonar relativa.
apresentações clínicas
PDA é mais comum em mulheres, lactentes prematuros, doentes com síndrome de Down e síndrome de rubéola congénita. Os sintomas são semelhantes aos encontrados no VSD e dependem do tamanho do shunt e direção do fluxo. Enquanto um pequeno PDA é geralmente assintomático, um grande PDA com shunt significativo da esquerda para a direita pode levar a CHF e, eventualmente, hipertensão pulmonar.em crianças mais velhas, a PDA produz classicamente um murmúrio contínuo ou” máquina ” devido ao fluxo através do shunt durante todo o ciclo cardíaco. Em recém-nascidos, especialmente aqueles nascidos prematuramente, o murmúrio pode ser ouvido apenas durante a sistole porque a pressão arterial pulmonar mais elevada diminui o fluxo durante o diastol.um sopro apical médio-diastólico pode ser ouvido devido ao aumento do fluxo através da válvula mitral (estenose mitral relativa). Isto geralmente significa um grande PDA e é muitas vezes associado com CHF.a pressão do pulso largo indica um grande desvio da esquerda para a direita devido a uma queda súbita na pressão diastólica.
História Natural e gestão
p > PDA de tamanho pequeno e moderado fecham-se espontaneamente, especialmente em lactentes de idade adulta. A PDA em lactentes prematuros pode necessitar de tratamento com indometacina (nas primeiras 2-4 semanas de vida) ou ligação cirúrgica. O fecho do dispositivo transcateter de PDA é frequentemente utilizado em crianças mais velhas.defeitos atriais septais envolvem várias partes diferentes do septo atrial. O defeito do Secundo do septo é o mais comum e compreende 6-10% de toda a DQC. Está localizado na fossa ovalis, na localização do foramen ovale. O defeito septal primum é considerado uma forma parcial de defeito septal atrioventricular. Os outros tipos “menos comuns” de ASD são o veno sinusal e o un-roofing do seio coronário.
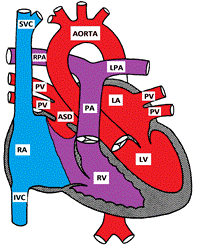
Figura mostrando um Secundum comunicação Interatrial
Fisiopatologia
Desde que a diferença de pressão entre os dois átrios é pequena, sem a turbulência é gerada pelo fluxo através da CIA. Em ASD moderadas a grandes, a direção e magnitude do shunt através da ASD depende da relativa conformidade ventricular direita e esquerda. No início da infância, a conformidade ventricular direita é baixa e o shunt através da DSA é pequeno. À medida que a conformidade do ventrículo direito aumenta, o shunt da esquerda para a direita aumenta. Se a conformidade ventricular direita diminuir, mais tarde na vida, o shunt diminui. O shunt pode eventualmente reverter se o paciente desenvolver hipertensão pulmonar e síndrome de Eisenmenger. Isso geralmente leva algumas décadas para se desenvolver.
a apresentação clínica
ASD é geralmente assintomática e apresenta tipicamente um sopro cardíaco na idade pré-escolar. A ICC raramente se desenvolve em doentes com uma grande DSA. O estiramento Auricular direito pode causar arritmias auriculares. A sobrecarga volumétrica prolongada dos pulmões eventualmente causa hipertensão pulmonar, que pode levar 4 a 5 décadas para se desenvolver.um sopro de ejecção sistólica pode ser ouvido na área pulmonar devido ao aumento do fluxo através da válvula pulmonar (estenose pulmonar relativa).um sopro diastólico médio pode ser ouvido na borda inferior esquerda do esterno devido ao aumento do fluxo através da válvula tricúspide. Este murmúrio raramente é ouvido porque a válvula tricúspide annulus é maior do que a válvula pulmonar annulus. Um sopro de válvula tricúspide indica que o paciente está em ICC devido a um grande desvio da esquerda para a direita.
Gestão
a maioria dos doentes com DSA são assintomáticos e não é necessário qualquer tratamento médico específico. A gestão médica (como no VSD) pode ser necessária se a CHF estiver presente. O fechamento Trans-cateter é o método preferido de fechar o secundum ASDs. O fechamento cirúrgico pode ser necessário em pacientes com uma grande DSA secundarizada que não é passível de fechamento trans-cateter ou outros tipos de DSA, uma vez que é improvável que se fechem espontaneamente.
Atrioventricular de Defeito (AVSD)
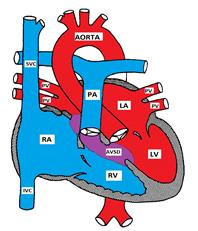
Figura Mostrando um Defeito Septal Atrioventricular
AVSD ocorre em 2% de todos os CHD e é mais prevalente em pacientes com Síndrome de Down. Quarenta por cento das crianças com síndrome de Down têm CHD e 40 % dos defeitos são formas de AVSD
Anatomia
defeito septal Atrioventricular é também conhecido como endocárdicas almofada de defeito (ECD) e canal atrioventricular (AVC). É constituída por uma variedade de defeitos nas almofadas endocárdicas que formam a parte inferior do septo Auricular, parte superior (Entrada) do septo ventricular, e as partes mediais das válvulas AV.
existem 4 tipos possíveis:
a) AVSD parcial (primum ASD) consiste num defeito na parte inferior do septo auricular e é geralmente associado a uma fenda no folheto mitral anterior causando insuficiência mitral. O septo ventricular está normalmente intacto.
B) AVSD completo tem um defeito que se estende da parte inferior do septo auricular para a parte superior (Entrada) do septo ventricular. As válvulas mitral e tricúspide perdem seus pontos de âncora no septo ventricular e estão ligadas umas às outras, formando UMA válvula AV comum que abana o septo ventricular.
c) o AVSD intermediário é semelhante ao AVSD completo, mas tem 2 válvulas AV com um primum ASD e um VSD de entrada grande.
d) O AVSD transitório é semelhante ao AVSD intermediário, mas o VSD é pequeno.a fisiopatologia depende da lesão predominante (Auricular vs ventricular). Há um shunt esquerdo-para-direita no nível Auricular devido ao aumento da conformidade ventricular direita relativa levando ao aumento do atrial direito. O aumento auricular esquerdo ocorre devido à insuficiência mitral secundária à fissura da válvula mitral. Existe um grau variável de hipertensão pulmonar à medida que a vasculatura pulmonar é exposta ao excesso de volume sanguíneo a pressões mais elevadas. A hipertensão pulmonar pode desenvolver-se nos primeiros dois anos em doentes normais e no primeiro ano em doentes com síndrome de Down.
apresentações clínicas
a apresentação clínica do AVSD é variável e depende do tamanho do defeito e do grau do shunt da esquerda para a direita. Os doentes com AVSD completo geralmente apresentam insuficiência cardíaca congestiva nas primeiras semanas de vida, enquanto os doentes com AVSD parcial (primum ASSD) podem ser completamente assintomáticos.os sintomas da ICC incluem falta de alimentação, falta de ar, diaforese durante a alimentação e aumento de peso. Cianose ligeira pode raramente desenvolver-se devido ao shunt da direita para a esquerda devido ao aumento da resistência pulmonar ou devido ao streaming preferencial do sangue venoso da CIV para o átrio esquerdo.os resultados físicos são variáveis e dependem da presença ou ausência de insuficiência cardíaca congestiva. O precórdio pode ser hiper-dinâmico e o apex cardíaco pode ser deslocado inferioramente e para a esquerda.
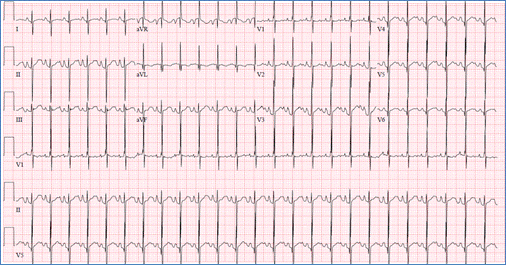
ECG mostrando superior QRS eixo do desvio negativo em avF) e ventricular direita
hipertrofia AVSD
Administração
CHF, se presente, é administrado com diuréticos, inibidores da ECA, e, ocasionalmente, digoxina. Uma fórmula de alta densidade calórica deve ser usada sem restrição de fluidos.quase todos os doentes com AVSD necessitarão de cirurgia. O momento da cirurgia depende do tamanho do paciente, da presença de ICC, da resposta ao tratamento médico e da presença ou ausência de hipertensão pulmonar. Em doentes assintomáticos com AVSD parcial, a cirurgia pode ser adiada até à idade pré-escolar. A cirurgia corretiva é geralmente realizada em doentes sintomáticos com ICC intractável nos primeiros meses de vida. Mesmo em pacientes que respondem ao tratamento médico, a presença de síndrome de Down requer uma cirurgia precoce para prevenir o desenvolvimento da hipertensão pulmonar. Se a cirurgia não puder ser realizada em um paciente sintomático, a bandagem arterial pulmonar pode ajudar a limitar o fluxo sanguíneo pulmonar até que seja possível a reparação cirúrgica.