The Universal Solvent
The Universal Solvent
This is, of course, another key property of water because more substances dissolve in water than any other common liquid. Isto é porque a molécula de água polar aumenta o poder dissolvente.”Dissolução envolve quebrar” sais “em íons componentes. Por exemplo, NaCl (sal comum) se decompõe nos íons Na+ e Cl – por causa da atração por íons (átomos ou grupos de átomos com carga) para moléculas de água é alta.
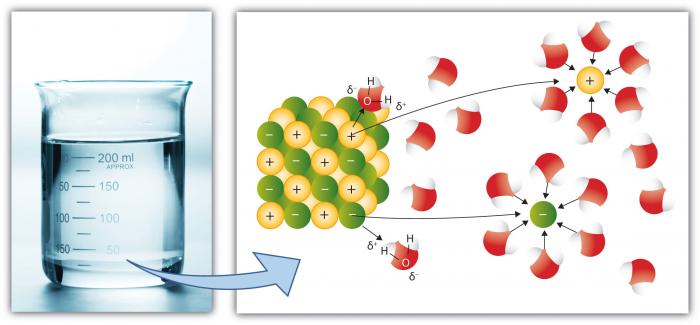
Cations, tais como na (sódio) têm uma carga positiva líquida, enquanto aniões (tais como Cl, Cloreto) têm uma carga negativa líquida. Há muitos elementos e compostos individuais que formam íons. Assim, a água pode conter concentrações consideráveis de várias espécies químicas, dependendo de suas propriedades particulares. Observe como as moléculas de água rodeiam os íons individuais, mantendo-os isolados de outros íons em solução. Isto ocorre até que a capacidade de água para isolar os íons é excedida, em que ponto a solução está “saturada” com esses íons e não pode dissolver mais (o sal começará a precipitar—formar um sólido).