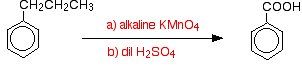alcune altre reazioni di benzene e metilbenzene
La solfonazione di metilbenzene
Il metilbenzene è più reattivo del benzene a causa della tendenza del gruppo metilico a “spingere” gli elettroni verso l’anello. Esattamente come questo aumenta la velocità di reazione è al di là del Regno Unito Un livello-è piuttosto più complicato di un semplice aumento della densità elettronica dell’anello.
L’effetto di questa maggiore reattività è che il metilbenzene reagirà con acido solforico fumante a 0°C e con acido solforico concentrato se vengono riscaldati sotto reflusso per circa 5 minuti.
Oltre all’effetto sulla velocità di reazione, con il metilbenzene devi anche pensare a dove il gruppo acido solfonico finisce sull’anello rispetto al gruppo metilico.
I gruppi metilici hanno la tendenza a”dirigere" nuovi gruppi nelle posizioni 2 e 4 sull’anello (supponendo che il gruppo metilico sia nella posizione 1). Si dice che i gruppi metilici siano 2,4-diretti. L’origine di questo effetto di regia è anche al di là del Regno Unito Un livello.
Quindi ottieni una miscela che consiste principalmente di due isomeri. Si forma solo circa il 5-10% dell’isomero 3.
Le principali reazioni sono:
![]()
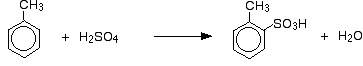
e:
![]()
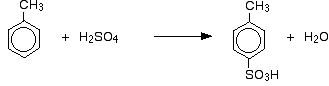
In caso di sulphonation, l’esatta percentuale di isomeri formato dipende dalla temperatura di reazione. All’aumentare della temperatura, si ottengono proporzioni crescenti dell’isomero 4 e meno dell’isomero 2.
Questo perché la solfonazione è reversibile. Il gruppo acido solfonico può cadere di nuovo dall’anello e ricollegarsi da qualche altra parte. Ciò tende a favorire la formazione dell’isomero termodinamicamente più stabile. Questo interscambio avviene più a temperature più elevate.
L’isomero 4 è più stabile perché non c’è ingombro nella molecola come ci sarebbe se il gruppo metilico e il gruppo acido solfonico fossero vicini l’uno all’altro.
Ossidazione della catena laterale in alchilbenzeni
Un alchilbenzene è semplicemente un anello benzenico con un gruppo alchilico collegato ad esso. Il metilbenzene è il più semplice alchilbenzene.
I gruppi alchilici sono solitamente abbastanza resistenti all’ossidazione. Tuttavia, quando sono attaccati ad un anello benzenico, sono facilmente ossidati da una soluzione alcalina di manganato di potassio(VII) (permanganato di potassio).
Il metilbenzene viene riscaldato sotto reflusso con una soluzione di manganato di potassio(VII) reso alcalino con carbonato di sodio. Il colore viola del manganato di potassio (VII) è infine sostituito da un precipitato marrone scuro di ossido di manganese(IV).
La miscela viene infine acidificata con acido solforico diluito.
Nel complesso, il metilbenzene viene ossidato ad acido benzoico.
![]()
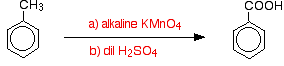
È interessante notare che qualsiasi gruppo alchilico viene ossidato di nuovo al gruppo a-COOH sull’anello in queste condizioni. Quindi, ad esempio, il propilbenzene viene anche ossidato ad acido benzoico.
![]()