Idiopathic intracranial hypertension
Assessment | Biopsychology | Comparative |Cognitive | Developmental | Language | Individual differences |Personality | Philosophy | Social |
Methods | Statistics |Clinical | Educational | Industrial |Professional items |World psychology |
Biological:Behavioural genetics · Evolutionary psychology · Neuroanatomy · Neurochemistry · Neuroendocrinology ·Neuroscience · Psychoneuroimmunology · Physiological Psychology · Psychopharmacology(Index, Outline)
MRI brain.jpg|
| ICD-10 | G932 | |
|---|---|---|
| ICD-9 | 348.2 | |
| 243200 | Boliddb | 1331 | MedlinePlus | 000351 |
| emedicină | neuro/329 OPH/190 neuro/537 | |
| mesh | {{{meshnumber}}} | |
hipertensiune intracraniană idiopatică (IIH), uneori numit de numele mai vechi hipertensiune intracraniană benignă (bih) sau pseudotumor cerebri (PTC), este o tulburare neurologică care se caracterizează prin creșterea presiunii intracraniene (presiune în jurul creier) în absența unei tumori sau a altor boli. Principalele simptome sunt dureri de cap, greață și vărsături, precum și tinitus pulsatil (bâzâit în urechi sincron cu pulsul), vedere dublă și alte simptome vizuale. Dacă nu este tratată, poate duce la umflarea discului optic în ochi, care poate progresa până la pierderea vederii.
IIH este diagnosticat cu o scanare a creierului (pentru a exclude alte cauze) și o puncție lombară; puncția lombară poate oferi, de asemenea, o ușurare temporară și uneori permanentă a simptomelor. Unii răspund la medicamente (cu medicamentul acetazolamidă), dar alții necesită o intervenție chirurgicală pentru ameliorarea presiunii. Afecțiunea poate apărea la toate grupele de vârstă, dar este cea mai frecventă la femeile tinere, în special la cele cu obezitate.
semne și simptome
cel mai frecvent simptom al IIH este cefaleea, care apare în aproape toate cazurile (92-94%). Este caracteristic mai rău dimineața, generalizat în caracter și pulsatil în natură. Poate fi asociat cu greață și vărsături. Durerea de cap poate fi agravată de orice activitate care crește și mai mult presiunea intracraniană, cum ar fi tusea și strănutul. Durerea poate fi, de asemenea, experimentată la nivelul gâtului și umerilor. Mulți au tinitus pulsatil, o senzație whooshing în una sau ambele urechi (64-87%); acest sunet este sincron cu pulsul. Diverse alte simptome, cum ar fi amorțirea extremităților, slăbiciunea generalizată, pierderea mirosului și necoordonarea, sunt raportate mai rar; niciunul nu este specific pentru IIH. La copii, pot fi prezente numeroase semne și simptome nespecifice.
presiunea crescută duce la compresia și tracțiunea nervilor cranieni, un grup de nervi care apar din tulpina creierului și alimentează fața și gâtul. Cel mai frecvent, este implicat nervul abducens (al șaselea nerv). Acest nerv furnizează mușchiul care trage ochiul spre exterior. Prin urmare, cei cu a șasea paralizie nervoasă experimentează o viziune dublă orizontală, care este mai gravă atunci când privim spre partea afectată. Mai rar, nervul oculomotor și nervul trohlear (respectiv a treia și a patra paralizie nervoasă) sunt afectate; ambele joacă un rol în mișcările ochilor. Nervul facial (al șaptelea nerv cranian) este afectat ocazional-rezultatul este slăbiciunea totală sau parțială a mușchilor expresiei faciale pe una sau ambele părți ale feței.
presiunea crescută duce la papilemă, care este umflarea discului optic, locul în care nervul optic intră în globul ocular. Acest lucru se întâmplă practic în toate cazurile de IIH, dar nu toată lumea prezintă simptome din acest motiv. Cei care prezintă simptome raportează de obicei” obscurări vizuale tranzitorii”, episoade de dificultate de a vedea care apar la ambii ochi, dar nu neapărat în același timp. Papiledemul netratat pe termen lung duce la pierderea vederii, inițial la periferie, dar progresiv spre centrul vederii.
examinarea fizică a sistemului nervos este de obicei normală, în afară de prezența papilemului, care se observă la examinarea ochiului cu un dispozitiv mic numit oftalmoscop sau mai detaliat cu o cameră de fundus. Dacă există anomalii ale nervilor cranieni, acestea pot fi observate la examinarea ochilor sub formă de strabism (a treia, a patra sau a șasea paralizie nervoasă) sau ca paralizie a nervului facial. Dacă papilledema a fost de lungă durată, câmpurile vizuale pot fi restrânse și acuitatea vizuală poate fi scăzută. Testarea câmpului vizual prin perimetrie automată (Humphrey) este recomandată, deoarece alte metode de testare pot fi mai puțin precise. Papilledema de lungă durată duce la atrofie optică, în care discul pare palid și pierderea vizuală tinde să fie avansată.
cauze
„idiopatic” înseamnă „de etiologie necunoscută”. Prin urmare, IIH poate fi diagnosticat numai dacă nu există o explicație alternativă pentru simptome. Presiunea intracraniană poate fi crescută datorită medicamentelor, cum ar fi derivații de vitamina A cu doze mari (de exemplu, izotretinoină pentru acnee), antibiotice tetraciclinice pe termen lung (pentru o varietate de afecțiuni ale pielii) și contraceptive hormonale. Există numeroase alte boli, în special afecțiuni rare, care pot duce la hipertensiune intracraniană. Dacă există o cauză de bază, afecțiunea este denumită „hipertensiune intracraniană secundară”. Cauzele frecvente ale hipertensiunii intracraniene secundare includ apneea obstructivă de somn (o tulburare de respirație legată de somn), lupusul eritematos sistemic (SLE), boala renală cronică și boala Behicktet.
mecanism
cauza IIH nu este cunoscută. Regula Monro-Kellie afirmă că presiunea intracraniană (literalmente: presiunea din interiorul craniului) este determinată de cantitatea de țesut cerebral, lichid cefalorahidian (LCR) și sânge din interiorul bolții craniene osoase. Prin urmare, există trei teorii cu privire la motivul pentru care presiunea ar putea fi ridicată în IIH: exces de producție de LCR, volum crescut de sânge sau țesut cerebral sau obstrucție a venelor care scurg sângele din creier.
prima teorie, cea a creșterii producției de lichid cefalorahidian, a fost propusă în descrierile timpurii ale bolii. Cu toate acestea, nu există date experimentale care să susțină un rol pentru acest proces în IIH.a doua teorie susține că fie creșterea fluxului sanguin către creier, fie creșterea țesutului cerebral în sine poate duce la creșterea presiunii. S-au acumulat puține dovezi care să susțină sugestia că fluxul sanguin crescut joacă un rol, dar atât probele de biopsie, cât și diferitele tipuri de scanări ale creierului au arătat un conținut crescut de apă al țesutului cerebral. Rămâne neclar de ce ar putea fi cazul.a treia teorie sugerează că fluxul de sânge din creier poate fi afectat sau congestionat. Doar la o mică proporție de pacienți s-a demonstrat îngustarea subiacentă a sinusurilor sau venelor cerebrale. Congestia sângelui venos poate rezulta dintr-o presiune venoasă în general crescută, care a fost legată de obezitate.
diagnostic
diagnosticul poate fi suspectat pe baza istoricului și examinării. Pentru a confirma diagnosticul, precum și pentru a exclude cauzele alternative, sunt necesare mai multe investigații; pot fi efectuate mai multe investigații dacă istoricul nu este tipic sau pacientul este mai probabil să aibă o problemă alternativă: copii, bărbați, vârstnici sau femei care nu sunt supraponderale.
Investigații
neuroimagistica, de obicei cu tomografie computerizată (CT / CAT) sau imagistică prin rezonanță magnetică (RMN), exclude leziunile de masă. În IIH aceste scanări pot fi normale, deși ventriculele mici sau asemănătoare fantei și „semnul sella gol” (aplatizarea glandei pituitare datorită presiunii crescute) pot fi văzute. O venogramă MR este, de asemenea, efectuată în toate cazurile (sau conform unor experți numai în cazuri atipice) pentru a exclude posibilitatea obstrucției venoase sau a trombozei sinusului venos cerebral.
puncția lombară este efectuată pentru a măsura presiunea de deschidere, precum și pentru a obține lichidul cefalorahidian (LCR) pentru a exclude diagnosticele alternative. Dacă presiunea de deschidere este crescută, LCR poate fi îndepărtat pentru ușurare (a se vedea mai jos). LCR este examinat pentru celule anormale, niveluri de glucoză și proteine; în IIH, toate sunt în limite normale. Ocazional, măsurarea presiunii poate fi normală, în ciuda simptomelor foarte sugestive. Acest lucru poate fi atribuit faptului că presiunea LCR poate fluctua pe parcursul zilei. Dacă suspiciunea rămâne ridicată, poate fi necesar să se efectueze o monitorizare mai lungă a ICP de către un cateter de presiune.
clasificare
criteriile originale pentru IIH au fost descrise de Dandy în 1937.
1Signs & simptome de presiune crescută ICP – CSF >25 cmH2O
2NU există semne de localizare cu excepția paraliziei nervoase abducens
3NORMAL CSF compoziție
4normal la ventricule mici (fante) pe imagistica fără masă intracraniană
au fost modificate de Smith în 1985 pentru a deveni „criteriile dandy modificate”. Smith a inclus utilizarea unor imagini mai avansate: Dandy necesitase ventriculografie, dar Smith a înlocuit-o cu tomografie computerizată. Într-o lucrare din 2001, Digre și Corbett au modificat în continuare criteriile lui Dandy. Ei au adăugat cerința ca pacientul să fie treaz și alert, deoarece coma împiedică evaluarea neurologică adecvată și necesită excluderea trombozei sinusurilor venoase ca cauză principală. În plus, ele adaugă cerința ca nici o altă cauză pentru ICP crescut este găsit.
1simptome ale presiunii intracraniene crescute (cefalee, greață, vărsături, obscurații vizuale tranzitorii sau edem papilar)
2NU există semne de localizare, cu excepția paraliziei nervoase abducens (a șasea)
3pacientul este treaz și alert
4 rezultate normale ale CT/RMN fără dovezi de tromboză
5LP presiunea de deschidere a >25 cmH2O și compoziția biochimică și citologică normală a LCR
6NU există altă explicație pentru presiunea intracraniană crescută
într-o revizuire din 2002, Friedman și Jacobson propune un set alternativ de criterii, derivate din Smith. acestea necesită absența simptomelor care nu au putut fi explicate printr-un diagnostic de IIH, dar nu necesită prezența reală a oricăror simptome (cum ar fi cefaleea) atribuibile IIH. Aceste criterii necesită, de asemenea, ca puncția lombară să fie efectuată cu pacientul întins lateral, deoarece o puncție lombară efectuată în poziție verticală așezată poate duce la măsurători artificiale de presiune ridicată. Friedman și Jacobson, de asemenea, nu insistă asupra venografiei Domnului pentru fiecare pacient; mai degrabă, acest lucru este necesar numai în cazuri atipice (vezi „diagnosticul” de mai sus).
tratamentul
scopul principal în tratamentul IIH este prevenirea pierderii vizuale și a orbirii, precum și controlul simptomelor. IIH este tratată în principal prin reducerea presiunii LCR și, dacă este cazul, prin scăderea în greutate. IIH se poate rezolva după tratamentul inițial, poate intra în remisie spontană (deși poate recidiva într-o etapă ulterioară) sau poate continua cronic.
puncție lombară
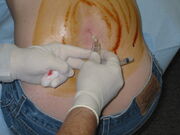
o puncție lombară în desfășurare. O suprafață mare de pe spate a fost spălată cu un dezinfectant pe bază de iod, lăsând o culoare maro. În această imagine, pacientul este așezat în poziție verticală, ceea ce poate face procedura mai ușor de efectuat, dar face ca orice măsurare a presiunii de deschidere să fie nesigură.
primul pas în controlul simptomelor este drenajul lichidului cefalorahidian prin puncție lombară. Dacă este necesar, acest lucru poate fi efectuat în același timp cu un LP „diagnostic”. În unele cazuri, acest lucru este suficient pentru a controla simptomele și nu este necesar un tratament suplimentar.
procedura poate fi repetată dacă este necesar, dar acest lucru este, în general, luat ca un indiciu că pot fi necesare tratamente suplimentare pentru a controla simptomele și a păstra vederea; LPs repetate sunt considerate neplăcute de către pacienți. LP repetate sunt uneori necesare pentru a controla urgent ICP dacă vederea se deteriorează rapid.
medicație
cel mai bine studiat tratament medical este acetazolamida (Diamox), care acționează prin inhibarea enzimei anhidrază carbonică și reduce producția de LCR cu șase până la 57%. Poate provoca simptome de hipokaliemie (niveluri scăzute de potasiu din sânge), care includ slăbiciune musculară și furnicături la nivelul degetelor. Acetazolamida nu poate fi utilizată în timpul sarcinii, deoarece s-a demonstrat că provoacă anomalii embrionare în studiile la animale, iar la om s-a demonstrat că provoacă acidoză metabolică, precum și perturbări ale nivelului de electroliți din sânge la nou-născut. Furosemidul diuretic este uneori utilizat dacă acetazolamida nu este tolerată, dar acest lucru are un efect redus asupra ICP.
diferite analgezice (analgezice) pot fi utilizate în controlul durerii de cap. În plus față de agenții convenționali, cum ar fi paracetamolul, o doză mică de antidepresiv amitriptilină, precum și topiramatul anticonvulsivant au arătat un beneficiu suplimentar pentru ameliorarea durerii.
utilizarea steroizilor pentru a reduce ICP este controversată; ele pot fi utilizate în papilledema severă, dar în caz contrar utilizarea lor este descurajată.
Chirurgie
există două proceduri chirurgicale principale în tratamentul IIH: decompresia tecii nervului optic și fenestrarea și manevrarea. Chirurgia ar fi oferită în mod normal numai dacă terapia medicală este fie nereușită, fie nu este tolerată. Alegerea dintre aceste două proceduri depinde de problema predominantă în IIH. Niciuna dintre proceduri nu este perfectă: ambele pot provoca complicații semnificative și ambele pot eșua în cele din urmă în controlul simptomelor. Nu există studii randomizate controlate care să ghideze decizia cu privire la procedura cea mai bună.
fenestrarea tecii nervului Optic este o operație oftalmologică care implică efectuarea unei incizii în mucoasa țesutului conjunctiv al nervului optic în porțiunea sa din spatele ochiului. Nu este foarte clar cum protejează ochiul de presiunea ridicată, dar poate fi rezultatul fie al devierii CSF în orbită, fie al creării unei zone de țesut cicatricial care scade presiunea. Efectele asupra presiunii intracraniene în sine sunt mai modeste. Mai mult, procedura poate duce la complicații semnificative, inclusiv orbire în 1-2%. Prin urmare, procedura este recomandată în special la cei care au simptome limitate de cefalee, dar papiledem semnificativ sau vedere amenințată sau la cei care au suferit un tratament nereușit cu un șunt sau au o contraindicație pentru chirurgia șuntului.
chirurgia șuntului, efectuată de obicei de neurochirurgi, implică crearea unei conducte prin care CSF poate fi drenat într-o altă cavitate a corpului. Procedura inițială este de obicei un șunt lumboperitoneal (LP), care conectează spațiul subarahnoid din coloana lombară cu cavitatea peritoneală. În general, o supapă de presiune este inclusă în circuit pentru a evita drenajul excesiv atunci când pacientul este erect și, prin urmare, are un ICP relativ ridicat. Manevrarea LP oferă o ușurare pe termen lung în aproximativ jumătate din cazuri; altele necesită revizuirea șuntului, adesea în mai multe ocazii—de obicei din cauza obstrucției șuntului. Dacă șuntul lumboperitoneal necesită revizuiri repetate, poate fi luat în considerare un șunt ventriculoatrial sau ventriculoperitoneal. Aceste șunturi sunt inserate într-unul din ventriculele laterale ale creierului, de obicei prin chirurgie stereotactică, și apoi conectate fie la atriul drept al inimii, fie la cavitatea peritoneală. Având în vedere nevoia redusă de revizuiri în șunturile ventriculare, este posibil ca această procedură să devină tipul de primă linie de tratament al șuntului.
în cazurile de obezitate severă, s-a demonstrat că operația de bypass gastric duce la o îmbunătățire semnificativă a simptomelor.
prognostic
nu se știe ce procent din persoanele cu IIH vor remite spontan și ce procent va dezvolta boli cronice.
IIH nu afectează în mod normal speranța de viață. Complicațiile majore ale IIH apar din papilema netratată sau rezistentă la tratament. În diferite serii de cazuri, riscul pe termen lung al celor viziune fiind afectat în mod semnificativ de IIH este raportat să se afle oriunde între 10 și 25%.
Epidemiologie
incidența IIH este puternic determinată de sex și greutatea corporală. Cifrele la femei sunt la femei între 20 și 45 de ani.
în medie, IIH apare la aproximativ 1 la 100.000 de persoane și poate apărea la copii și adulți. Vârsta medie la diagnostic este de 30 de ani. IIH apare predominant la femei, în special la vârsta de 20-45 de ani, care au de patru până la opt ori mai multe șanse decât bărbații să fie afectați. Excesul de greutate și obezitatea predispun puternic o persoană la IIH: femeile care au mai mult de zece la sută peste greutatea corporală ideală au de treisprezece ori mai multe șanse să dezvolte IIH, iar această cifră crește până la nouăsprezece ori la femeile care au mai mult de douăzeci la sută peste greutatea corporală ideală. La bărbați există și această relație, dar creșterea este de doar cinci ori la cei cu peste 20% peste greutatea corporală ideală.
în ciuda mai multor rapoarte de IIH în familii, nu există o cauză genetică cunoscută pentru IIH. Oamenii din toate etniile pot dezvolta IIH. La copii, nu există nicio diferență de incidență între bărbați și femei.
din bazele de date naționale de admitere a spitalelor se pare că nevoia de intervenție neurochirurgicală pentru IIH a crescut semnificativ în perioada 1988-2002. Acest lucru a fost atribuit cel puțin parțial prevalenței în creștere a obezității, deși o parte din această creștere poate fi explicată prin popularitatea crescută a șuntării peste fenestrarea tecii nervului optic.
istoric
primul raport al IIH a fost realizat de medicul German Heinrich Quincke, care l-a descris în 1893 sub numele de meningită seroasă. Termenul „pseudotumor cerebri” a fost introdus în 1904 de compatriotul său Max Nonne. Numeroase alte cazuri au apărut ulterior în literatură; în multe cazuri, presiunea intracraniană crescută poate să fi rezultat de fapt din Condițiile subiacente. De exemplu, hidrocefalia otitica raportata de neurologul londonez Sir Charles Symonds ar fi putut rezulta din tromboza sinusului venos cauzata de infectia urechii medii. Criteriile de Diagnostic pentru IIH au fost dezvoltate în 1937 de neurochirurgul Baltimore Walter Dandy; Dandy a introdus, de asemenea, o intervenție chirurgicală decompresivă subtemporală în tratamentul afecțiunii.
termenii „benign” și „pseudotumor” derivă din faptul că presiunea intracraniană crescută poate fi asociată cu tumori cerebrale. Acei pacienți la care nu a fost găsită nicio tumoare au fost, prin urmare, diagnosticați cu „pseudotumor cerebri” (o boală care imită o tumoare pe creier). Boala a fost redenumită „hipertensiune intracraniană benignă” în 1955 pentru a o distinge de hipertensiunea intracraniană datorată bolilor care pun viața în pericol (cum ar fi cancerul); cu toate acestea, acest lucru a fost, de asemenea, considerat a fi înșelător, deoarece orice boală care poate orbi pe cineva nu ar trebui considerată benignă și, prin urmare, numele a fost revizuit în 1989 la „hipertensiune intracraniană idiopatică (fără cauză identificabilă)”.
chirurgia șuntului a fost introdusă în 1949; inițial, s-au folosit șunturi ventriculoperitoneale. În 1971, au fost raportate rezultate bune cu manevrarea lumboperitoneală. Rapoartele Negative privind manevrarea în anii 1980 au dus la o scurtă perioadă (1988-1993) în care fenestrarea nervului optic (care fusese descrisă inițial într-o stare fără legătură în 1871) a fost mai populară. De atunci, manevrarea este recomandată predominant, cu excepții ocazionale.
Vezi și
- hipertensiune
- 1.00 1.01 1.02 1.03 1.04 1.05 1.06 1.07 1.08 1.09 1.10 1.11 1.12 1.13 1.14 1.15 1.16 1.17 1.18 1.19 1.20 1.21 1.22 1.23 1.24 1.25 1.26 1.27 Binder DK, Horton JC, Lawton MT, McDermott MW (martie 2004). Hipertensiune intracraniană idiopatică. Neurochirurgie 54 (3): 538-51; discuție 551-2.
- Sismanis A (iulie 1998). Tinitus pulsatil. O experiență de 15 ani. Am J Otol 19 (4): 472-7.
- 3.0 3.1 3.2 3.3 3.4 3.5 3.6 Soler D, Cox T, Bullock P, Calver DM, Robinson RO (ianuarie 1998). Diagnosticul și gestionarea hipertensiunii intracraniene benigne. Arch. Dis. Copil. 78 (1): 89–94.
- 4.0 4.1 4.2 4.3 4.4 4.5 4.6 4.7 4.8 Friedman DI, Jacobson DM (2002). Criterii de Diagnostic pentru hipertensiunea intracraniană idiopatică. Neurologie 59 (10): 1492-1495.
- 5.00 5.01 5.02 5.03 5.04 5.05 5.06 5.07 5.08 5.09 5.10 5.11 5.12 5.13 5.14 5.15 5.16 5.17 5.18 Acheson JF (2006). Idiopathic intracranial hypertension and visual function. Br. Med. Bull. 79-80 (1): 233–44.
- 6.0 6.1 6.2 Dandy WE (October 1937). Intracranial pressure without brain tumor – diagnosis and treatment. Ann. Surg. 106 (4): 492–513.
- Smith JL (1985). Whence pseudotumor cerebri?. J. Clin. Neuroophthalmol. 5 (1): 55–6.
- 8.0 8.1 Digre KB, Corbett JJ (2001). Idiopathic intracranial hypertension (pseudotumor cerebri): A reappraisal. Neurologist 7: 2–67.
- Curry WT, Butler noi, Barker FG (2005). Creșterea rapidă a incidenței procedurilor de manevră a lichidului cefalorahidian pentru hipertensiunea intracraniană idiopatică în Statele Unite, 1988-2002. Neurochirurgie 57 (1): 97-108; discuție 97-108. Quincke HI (1893). Meningită seroasă. Samml. Klin. Vortr. 67: 655.
- Nonne M (1904). Ueber Falle vom Symptomkomplex” Tumor Cerebri ” mit Ausgang in Heilung (Pseudotumor Cerebri). Dtsch. Z. Nervenheilk. 27 (3-4): 169–216.
- 12.0 12.1 12.2 Johnston I (2001). Dezvoltarea istorică a conceptului de pseudotumor. Neurochirurgie. Focalizarea 11 (2): 1.
- Symonds CP (1931). Hidrocefalie otitică. Creier 54 (3705): 55-71.
- Foley J (1955). Forme benigne de hipertensiune intracraniană; hidrocefalie toxică și otită. Creier 78 (1): 1-41. Corbett JJ, Thompson HS (octombrie 1989). Managementul rațional al hipertensiunii intracraniene idiopatice. Arch. Neurol. 46 (10): 1049–51.
- Bandyopadhyay S (2001). Pseudotumor cerebri. Arch. Neurol. 58 (10): 1699–701.
- Idiopathic intracranial hypertension at the Open Directory Project
|
v·d·e
Nervous system disorders, primarily CNS (G04–G47, 323–349) |
||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Inflammation |
|
Both/either
|
||||||||||||||||||||||
| Brain/ encephalopathy |
|
|||||||||||||||||||||||
| Spinal cord/ myelopathy |
Syringomyelia · Syringobulbia · Morvan’s syndrome · Vascular myelopathy (Foix-Alajouanine syndrome) · Spinal cord compression |
|||||||||||||||||||||||
| Both/either |
|
|
||||||||||||||||||||||
| {| class=”navbox collapsible nowraplinks” style=”margin:auto; „ | ||||||||||||||||||||||||
|
··
|
||||||||||||||||||||||||
|
||||||||||||||||||||||||
|}
This page uses Creative Commons Licensed content from Wikipedia (view authors).