Idiopathic intracranial hypertension
Assessment | Biopsychology | Comparative |Cognitive | Developmental | Language | Individual differences |Personality | Philosophy | Social |
Methods | Statistics |Clinical | Educational | Industrial |Professional items |World psychology |
Biological:Behavioural genetics · Evolutionary psychology · Neuroanatomy · Neurochemistry · Neuroendocrinology ·Neuroscience · Psychoneuroimmunology · Physiological Psychology · Psychopharmacology(Index, Outline)
MRI brain.jpg|
| ICD-10 | G932 | |
|---|---|---|
| ICD-9 | 348.2 | |
| OMIM | 243200 | |
| Sjukdomardb | 1331 | |
| MedlinePlus | 000351 | |
| emedicin | neuro/329 oph/190 neuro/537 | |
| mesh | {{{meshnumber}}} | |
idiopatisk intrakraniell hypertension (IIH), som ibland kallas av de äldre namnen godartad intrakraniell hypertoni (bih) eller pseudotumor cerebri (PTC), är en neurologisk störning som kännetecknas av ökat intrakraniellt tryck (tryck runt hjärnan) i frånvaro av en tumör eller andra sjukdomar. De viktigaste symptomen är huvudvärk, illamående och kräkningar, liksom pulserande tinnitus (surrande i öronen synkron med puls), dubbelsyn och andra visuella symtom. Om det inte behandlas kan det leda till svullnad av optisk skiva i ögat, vilket kan utvecklas till synförlust.
IIH diagnostiseras med en hjärnskanning (för att utesluta andra orsaker) och en ländryggspunktur; ländryggspunktur kan också ge tillfällig och ibland permanent lättnad från symtomen. Vissa svarar på medicinering (med läkemedlet acetazolamid), men andra kräver operation för att lindra trycket. Tillståndet kan förekomma i alla åldersgrupper, men är vanligast hos unga kvinnor, särskilt de med fetma.
tecken och symtom
det vanligaste symptomet på IIH är huvudvärk, vilket förekommer i nästan alla (92-94%) fall. Det är karakteristiskt sämre på morgonen, generaliserat i karaktär och bankande i naturen. Det kan vara förknippat med illamående och kräkningar. Huvudvärken kan förvärras av någon aktivitet som ytterligare ökar det intrakraniella trycket, såsom hosta och nysningar. Smärtan kan också upplevas i nacke och axlar. Många har pulserande tinnitus, en whooshing känsla i en eller båda öronen (64-87%); detta ljud är synkront med pulsen. Olika andra symtom, såsom domningar i extremiteterna, generaliserad svaghet, luktförlust och inkoordination, rapporteras mer sällan; ingen är specifik för IIH. Hos barn kan många icke-specifika tecken och symtom vara närvarande.
det ökade trycket leder till kompression och dragkraft i kranialnerven, en grupp nerver som uppstår från hjärnstammen och levererar ansikte och nacke. Oftast är abducensnerven (sjätte nerven) involverad. Denna nerv levererar muskeln som drar ögat utåt. De med sjätte nervpares upplever därför horisontell dubbelsyn som är värre när man tittar mot den drabbade sidan. Mer sällan påverkas den oculomotoriska nerven och trochlearnerven (respektive tredje och fjärde nervpares); båda spelar en roll i ögonrörelser. Ansiktsnerven (sjunde kranialnerven) påverkas ibland-resultatet är total eller partiell svaghet i ansiktsuttryckets muskler på en eller båda sidor av ansiktet.
det ökade trycket leder till papilledema, vilket är svullnad av optisk skiva, den plats där optisk nerv kommer in i ögongloben. Detta sker i praktiskt taget alla fall av IIH, men inte alla upplever symtom från detta. De som upplever symtom rapporterar vanligtvis” övergående visuella obscurations”, episoder av svårigheter att se som förekommer i båda ögonen men inte nödvändigtvis samtidigt. Långvarigt obehandlat papilledema leder till visuell förlust, initialt i periferin men gradvis mot syncentret.
fysisk undersökning av nervsystemet är vanligtvis normalt bortsett från närvaron av papilledema, vilket ses vid undersökning av ögat med en liten enhet som kallas ett oftalmoskop eller mer detaljerat med en funduskamera. Om det finns kranialnervavvikelser kan dessa märkas vid ögonundersökning i form av en squint (tredje, fjärde eller sjätte nervpares) eller som ansiktsnervpares. Om papilledemet har varit långvarigt kan synfält vara trånga och synskärpan kan minskas. Visuell fälttestning med automatiserad (Humphrey) perimetri rekommenderas eftersom andra testmetoder kan vara mindre exakta. Långvarigt papilledema leder till optisk atrofi, där skivan ser blek ut och visuell förlust tenderar att avanceras.
orsaker
” idiopatisk ”betyder”av okänd etiologi”. Därför kan IIH endast diagnostiseras om det inte finns någon alternativ förklaring till symtomen. Intrakraniellt tryck kan ökas på grund av läkemedel som högdos vitamin A-derivat (t.ex. isotretinoin för akne), långvariga tetracyklinantibiotika (för olika hudförhållanden) och hormonella preventivmedel. Det finns många andra sjukdomar, mestadels sällsynta tillstånd, som kan leda till intrakraniell hypertoni. Om det finns en bakomliggande orsak kallas tillståndet ”sekundär intrakraniell hypertoni”. Vanliga orsaker till sekundär intrakraniell hypertoni inkluderar obstruktiv sömnapnea (en sömnrelaterad andningsstörning), systemisk lupus erythematosus (SLE), kronisk njursjukdom och beh Augilets sjukdom.
mekanism
orsaken till IIH är inte känd. Monro-Kellie-regeln säger att det intrakraniella trycket (bokstavligen: tryck inuti skallen) bestäms av mängden hjärnvävnad, cerebrospinalvätska (CSF) och blod inuti det beniga kranialvalvet. Tre teorier finns därför om varför trycket kan höjas i IIH: ett överskott av CSF-produktion, ökad volym blod eller hjärnvävnad eller obstruktion av venerna som dränerar blod från hjärnan.
den första teorin, den för ökad produktion av cerebrospinalvätska, föreslogs i tidiga beskrivningar av sjukdomen. Det finns dock inga experimentella data som stöder en roll för denna process i IIH.
den andra teorin innebär att antingen ökat blodflöde till hjärnan eller ökning av hjärnvävnaden i sig kan leda till det upphöjda trycket. Lite bevis har samlats för att stödja förslaget att ökat blodflöde spelar en roll, men både biopsiprover och olika typer av hjärnskanningar har visat ett ökat vatteninnehåll i hjärnvävnaden. Det är fortfarande oklart varför detta kan vara fallet.
den tredje teorin antyder att blodflödet från hjärnan kan vara nedsatt eller överbelastad. Endast i en liten del av patienterna har underliggande förträngning av cerebrala bihålor eller vener visats. Överbelastning av venöst blod kan bero på ett generellt ökat venöst tryck, vilket har kopplats till fetma.
diagnos
diagnosen kan misstänkas på grundval av historia och undersökning. För att bekräfta diagnosen, såväl som att utesluta alternativa orsaker, krävs flera undersökningar; fler undersökningar kan utföras om historien inte är typisk eller patienten är mer benägna att ha ett alternativt problem: barn, män, äldre eller kvinnor som inte är överviktiga.
undersökningar
Neuroimaging, vanligtvis med datortomografi (CT / CAT) eller magnetisk resonansavbildning (MRI), utesluter massskador. I IIH kan dessa skanningar vara normala, även om små eller slitsliknande ventriklar och ”tomt sella-tecken” (utplattning av hypofysen på grund av ökat tryck) kan ses. Ett MR-venogram utförs också i alla fall (eller enligt vissa experter endast i atypiska fall) för att utesluta möjligheten till venös obstruktion eller cerebral venös sinustrombos.
Lumbar punktering utförs för att mäta öppningstrycket, liksom för att erhålla cerebrospinalvätska (CSF) för att utesluta alternativa diagnoser. Om öppningstrycket ökas kan CSF avlägsnas för lindring (se nedan). CSF undersöks för onormala celler, glukos och proteinnivåer; i IIH är alla inom normala gränser. Ibland kan tryckmätningen vara normal trots mycket suggestiva symtom. Detta kan bero på att CSF-trycket kan fluktuera under dagen. Om misstanken förblir hög kan det vara nödvändigt att utföra mer långvarig övervakning av ICP med en tryckkateter.
klassificering
de ursprungliga kriterierna för IIH beskrevs av Dandy 1937.
1tecken& symtom på ökat ICP-CSF-tryck>25 cmH2O
2inga lokaliserande tecken med undantag för abducens nervpares
3Normal CSF-komposition
4normala till små (slitsade) ventriklar vid avbildning utan intrakraniell massa
de modifierades av Smith 1985 för att bli ”modifierade dandy-kriterier”. Smith inkluderade användningen av mer avancerad bildbehandling: Dandy hade krävt ventrikulografi, men Smith ersatte detta med datortomografi. I en tidning från 2001 ändrade Digre och Corbett dandys kriterier ytterligare. De tillade kravet att patienten är vaken och vaken, eftersom koma utesluter adekvat neurologisk bedömning och kräver uteslutning av venös sinustrombos som en bakomliggande orsak. Dessutom lägger de till kravet att ingen annan orsak till den upphöjda ICP hittas.
1symptom på förhöjt intrakraniellt tryck (huvudvärk, illamående, kräkningar, övergående visuella obscurations eller papilledema)
2inga lokaliserande tecken med undantag av abducens (sjätte) nervpares
3patienten är vaken och alert
4normala CT/MR-fynd utan bevis på trombos
5LP öppningstryck av>25 cmH2O och normal biokemisk och cytologisk sammansättning av CSF
6ingen annan förklaring till det upphöjda intrakraniella trycket
i en 2002-recension, Friedman och Jacobson föreslår en alternativ uppsättning kriterier, härledda från Smiths. dessa kräver frånvaro av symtom som inte kunde förklaras av en diagnos av IIH, men kräver inte den faktiska förekomsten av några symtom (som huvudvärk) som kan hänföras till IIH. Dessa kriterier kräver också att lumbalpunktion utförs med patienten liggande i sidled, som en lumbalpunktion utförs i upprätt sittande ställning kan leda till artificiellt högtrycksmätningar. Friedman och Jacobson insisterar inte heller på Mr venografi för varje patient; snarare krävs detta endast i atypiska fall (se ”diagnos” ovan).
behandling
det primära målet vid behandling av IIH är förebyggande av synförlust och blindhet samt symptomkontroll. IIH behandlas huvudsakligen genom minskning av CSF-tryck och, i förekommande fall, viktminskning. IIH kan lösa efter initial behandling, kan gå in i spontan remission (även om det fortfarande kan återfalla i ett senare skede) eller kan fortsätta kroniskt.
lumbalpunktion
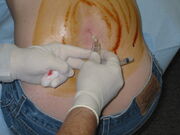
en lumbalpunktion pågår. Ett stort område på baksidan har tvättats med ett jodbaserat desinfektionsmedel som lämnar brun färgning. I denna bild sitter patienten upprätt, vilket kan göra proceduren lättare att utföra men gör varje mätning av öppningstrycket opålitligt.
det första steget i symptomkontroll är dränering av cerebrospinalvätska genom ländryggspunktur. Vid behov kan detta utföras samtidigt som en” diagnostisk ” LP. I vissa fall är detta tillräckligt för att kontrollera symtomen, och ingen ytterligare behandling behövs.
proceduren kan upprepas vid behov, men detta tas i allmänhet som en ledtråd att ytterligare behandlingar kan krävas för att kontrollera symtomen och bevara synen; upprepade lp betraktas som obehagliga av patienter. Upprepade lp behövs ibland för att snabbt kontrollera ICP om synen försämras snabbt.
medicinering
den bäst studerade medicinska behandlingen är acetazolamid (Diamox), som verkar genom att hämma enzymet kolsyraanhydras och det minskar CSF-produktionen med sex till 57 procent. Det kan orsaka symtom på hypokalemi (låga kaliumnivåer i blodet), som inkluderar muskelsvaghet och stickningar i fingrarna. Acetazolamid kan inte användas under graviditet, eftersom det har visat sig orsaka embryonala abnormiteter i djurstudier, och hos människor har visat sig orsaka metabolisk acidos samt störningar i blodelektrolytnivåerna hos nyfödda. Den diuretiska furosemiden används ibland om acetazolamid inte tolereras, men detta har liten effekt på ICP.
olika analgetika (smärtstillande medel) kan användas för att kontrollera huvudvärk. Förutom konventionella medel såsom paracetamol har en låg dos av antidepressiva amitriptylin såväl som antikonvulsiva topiramat visat några ytterligare fördelar för smärtlindring.
användningen av steroider för att minska ICP är kontroversiell; de kan användas vid svår papilledema, men annars är deras användning avskräckt.
kirurgi
två huvudsakliga kirurgiska ingrepp finns vid behandling av IIH: optisk nervmanteldekompression och fenestration och shunting. Kirurgi skulle normalt endast erbjudas om medicinsk behandling antingen misslyckas eller inte tolereras. Valet mellan dessa två procedurer beror på det övervägande problemet i IIH. Varken proceduren är perfekt: båda kan orsaka betydande komplikationer, och båda kan så småningom misslyckas med att kontrollera symtomen. Det finns inga randomiserade kontrollerade studier för att styra beslutet om vilket förfarande som är bäst.
optisk nervhölje fenestration är en oftalmologisk operation som innebär att man gör ett snitt i bindvävsfodret i synnerven i sin del bakom ögat. Det är inte helt klart hur det skyddar ögat från det upphöjda trycket, men det kan vara resultatet av antingen avledning av CSF i banan eller skapandet av ett område av ärrvävnad som sänker trycket. Effekterna på det intrakraniella trycket i sig är mer blygsamma. Dessutom kan förfarandet leda till betydande komplikationer, inklusive blindhet i 1-2%. Förfarandet rekommenderas därför främst hos dem som har begränsade huvudvärkssymtom men signifikant papilledema eller hotad syn, eller hos dem som har genomgått misslyckad behandling med en shunt eller har kontraindikation för shuntoperation.
Shuntkirurgi, som vanligtvis utförs av neurokirurger, innefattar skapandet av en ledning genom vilken CSF kan dräneras i en annan kroppshålighet. Det initiala förfarandet är vanligtvis en lumboperitoneal (LP) shunt, som förbinder det subaraknoida utrymmet i ländryggen med bukhålan. I allmänhet ingår en tryckventil i kretsen för att undvika överdriven dränering när patienten är upprätt och därför har en relativt hög ICP. LP shunting ger långvarig lättnad i ungefär hälften av fallen; andra kräver revision av shunten, ofta vid mer än ett tillfälle—vanligtvis på grund av shuntobstruktion. Om lumboperitoneal shunt behöver upprepade revideringar kan en ventrikuloatriell eller ventrikuloperitoneal shunt övervägas. Dessa shuntar sätts in i en av hjärnans laterala ventriklar, vanligtvis genom stereotaktisk kirurgi, och ansluts sedan antingen till hjärtans högra atrium eller bukhålan. Med tanke på det minskade behovet av revisioner i ventrikulära shuntar är det möjligt att denna procedur blir den första linjens typ av shuntbehandling.
i fall av svår fetma har gastrisk bypassoperation visat sig leda till en markant förbättring av symtomen.
prognos
det är inte känt vilken procentandel av personer med IIH som kommer att avgå spontant och vilken procentandel som kommer att utveckla kronisk sjukdom.
IIH påverkar normalt inte livslängden. De viktigaste komplikationerna från IIH uppstår från obehandlat eller behandlingsresistent papilledema. I olika fallserier rapporteras den långsiktiga risken för att visionen påverkas avsevärt av IIH ligga någonstans mellan 10 och 25%.
epidemiologi
förekomsten av IIH bestäms starkt av kön och kroppsvikt. Siffrorna hos kvinnor är hos kvinnor mellan 20 och 45 år.
i genomsnitt förekommer IIH hos cirka 1 per 100 000 personer och kan förekomma hos barn och vuxna. Medianåldern vid diagnos är 30. IIH förekommer främst hos kvinnor, särskilt i åldrarna 20-45, som är fyra till åtta gånger mer benägna än män att drabbas. Övervikt och fetma predisponerar starkt en person att IIH: kvinnor som är mer än tio procent över sin idealvikt är tretton gånger mer benägna att utveckla IIH, och denna siffra går upp till nitton gånger hos kvinnor som är mer än tjugo procent över sin idealvikt. Hos män finns detta förhållande också, men ökningen är bara femfaldig hos de över 20% över deras ideala kroppsvikt.
trots flera rapporter om IIH i familjer finns det ingen känd genetisk orsak till IIH. Människor från alla etniciteter kan utveckla IIH. Hos barn är det ingen skillnad i förekomst mellan män och kvinnor.
från National hospital admission databases verkar det som om behovet av neurokirurgisk intervention för IIH har ökat markant under perioden mellan 1988 och 2002. Detta har tillskrivits åtminstone delvis till den ökande förekomsten av fetma, även om en del av denna ökning kan förklaras av den ökade populariteten för växling över synnerven mantel fenestration.
historia
den första rapporten från IIH var av den tyska läkaren Heinrich Quincke, som beskrev den 1893 under namnet serös meningit. Termen ”pseudotumor cerebri” introducerades 1904 av hans landsmän Max Nonne. Många andra fall dök upp i litteraturen senare; i många fall kan det upphöjda intrakraniella trycket faktiskt ha resulterat från underliggande tillstånd. Till exempel kan den otitiska hydrocephalus som rapporterats av Londons neurolog Sir Charles Symonds ha resulterat i venös sinustrombos orsakad av mellanörsinfektion. Diagnostiska kriterier för IIH utvecklades 1937 av Baltimore neurokirurg Walter Dandy; Dandy introducerade också subtemporal dekompressiv kirurgi vid behandling av tillståndet.
termerna” godartade ”och” pseudotumor ” härrör från det faktum att ökat intrakraniellt tryck kan associeras med hjärntumörer. De patienter hos vilka ingen tumör hittades diagnostiserades därför med ”pseudotumor cerebri” (en sjukdom som efterliknar en hjärntumör). Sjukdomen döptes om till ”godartad intrakraniell hypertoni” 1955 för att skilja den från intrakraniell hypertoni på grund av livshotande sjukdomar (som cancer); detta ansågs emellertid också vara vilseledande eftersom någon sjukdom som kan blinda någon inte bör betraktas som godartad, och namnet reviderades därför 1989 till ”idiopatisk (utan identifierbar orsak) intrakraniell hypertoni”.
Shuntkirurgi introducerades 1949; initialt användes ventrikuloperitoneala shuntar. 1971 rapporterades goda resultat med lumboperitoneal shunting. Negativa rapporter om shunting på 1980-talet ledde till en kort period (1988-1993) under vilken optisk nervfenestration (som ursprungligen beskrivits i ett orelaterat tillstånd 1871) var mer populär. Sedan dess rekommenderas shunting övervägande, med tillfälliga undantag.
Se även
- hypertoni
- 1.00 1.01 1.02 1.03 1.04 1.05 1.06 1.07 1.08 1.09 1.10 1.11 1.12 1.13 1.14 1.15 1.16 1.17 1.18 1.19 1.20 1.21 1.22 1.23 1.24 1.25 1.26 1.27 Binder DK, Horton JC, Lawton MT, McDermott MW (mars 2004). Idiopatisk intrakraniell hypertoni. Neurokirurgi 54 (3): 538-51; diskussion 551-2.
- Sismanis A (juli 1998). Pulserande tinnitus. 15 års erfarenhet. Am J Otol 19 (4): 472-7.
- 3,0 3,1 3,2 3,3 3,4 3,5 3,6 Soler D, Cox T, Bullock P, Calver DM, Robinson RO (januari 1998). Diagnos och hantering av godartad intrakraniell hypertoni. Båge. Dis. Barn. 78 (1): 89–94.
- 4.0 4.1 4.2 4.3 4.4 4.5 4.6 4.7 4.8 Friedman DI, Jacobson DM (2002) (på engelska). Diagnostiska kriterier för idiopatisk intrakraniell hypertoni. Neurologi 59 (10): 1492-1495.
- 5,00 5,01 5,02 5.03 5.04 5.05 5.06 5.07 5.08 5.09 5.10 5.11 5.12 5.13 5.14 5.15 5.16 5.17 5.18 Acheson JF (2006). Idiopathic intracranial hypertension and visual function. Br. Med. Bull. 79-80 (1): 233–44.
- 6.0 6.1 6.2 Dandy WE (October 1937). Intracranial pressure without brain tumor – diagnosis and treatment. Ann. Surg. 106 (4): 492–513.
- Smith JL (1985). Whence pseudotumor cerebri?. J. Clin. Neuroophthalmol. 5 (1): 55–6.
- 8.0 8.1 Digre KB, Corbett JJ (2001). Idiopathic intracranial hypertension (pseudotumor cerebri): A reappraisal. Neurologist 7: 2–67.
- Curry WT, Butler vi, Barker FG (2005). Snabbt stigande förekomst av cerebrospinalvätska shunting förfaranden för idiopatisk intrakraniell hypertension i USA, 1988-2002. Neurokirurgi 57 (1): 97-108; diskussion 97-108.
- Quincke hej (1893). Meningit serosa. Samml. Klin. Vortr. 67: 655.
- Nonne M (1904). Ueber Falle vom Symptomkomplex ”tumör Cerebri” mit Ausgang i Heilung (Pseudotumor Cerebri). Dtsch. Z. Nervenheilk. 27 (3-4): 169–216.
- 12,0 12,1 12,2 Johnston I (2001). Den historiska utvecklingen av pseudotumorkonceptet. Neurosurg. Fokus 11 (2): 1.
- Symonds CP (1931). Otitisk hydrocephalus. Hjärna 54 (3705): 55-71.
- Foley J (1955). Godartade former av intrakraniell hypertoni; giftig och otitisk hydrocephalus. Hjärna 78 (1): 1-41.
- Corbett JJ, Thompson HS (oktober 1989). Den rationella hanteringen av idiopatisk intrakraniell hypertoni. Båge. Neurol. 46 (10): 1049–51.
- Bandyopadhyay S (2001). Pseudotumor cerebri. Båge. Neurol. 58 (10): 1699–701.
- Idiopathic intracranial hypertension at the Open Directory Project
|
v·d·e
Nervous system disorders, primarily CNS (G04–G47, 323–349) |
||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Inflammation |
|
Both/either
|
||||||||||||||||||||||
| Brain/ encephalopathy |
|
|||||||||||||||||||||||
| Spinal cord/ myelopathy |
Syringomyelia · Syringobulbia · Morvan’s syndrome · Vascular myelopathy (Foix-Alajouanine syndrome) · Spinal cord compression |
|||||||||||||||||||||||
| Both/either |
|
|
||||||||||||||||||||||
| {| class=”navbox collapsible nowraplinks” style=”margin:auto; ” | ||||||||||||||||||||||||
|
··
|
||||||||||||||||||||||||
|
||||||||||||||||||||||||
|}
This page uses Creative Commons Licensed content from Wikipedia (view authors).