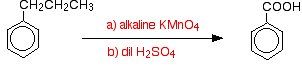algunas reacciones más de benceno y metilbenceno
La sulfonación de metilbenceno
El metilbenceno es más reactivo que el benceno debido a la tendencia del grupo metilo a «empujar» electrones hacia el anillo. La forma exacta en que esto aumenta la velocidad de reacción está más allá del nivel A del Reino Unido: es bastante más complicado que solo un aumento en la densidad electrónica del anillo.
El efecto de esta mayor reactividad es que el metilbenceno reaccionará con ácido sulfúrico fumante a 0°C, y con ácido sulfúrico concentrado si se calientan bajo reflujo durante aproximadamente 5 minutos.
Además del efecto en la velocidad de reacción, con el metilbenceno también hay que pensar en dónde termina el grupo ácido sulfónico en el anillo en relación con el grupo metilo.
Los grupos metilo tienen una tendencia a «dirigir& citar nuevos grupos en las posiciones 2 y 4 en el anillo (suponiendo que el grupo metilo esté en la posición 1). Se dice que los grupos metilo son 2,4 directores. El origen de este efecto directo también está más allá del nivel A del Reino Unido.
Para obtener una mezcla que consta principalmente de dos isómeros. Solo se forma alrededor del 5-10% del isómero 3.
Las principales reacciones son:
![]()
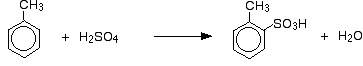
:
![]()
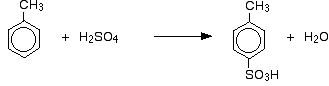
En el caso de sulfonación no, la proporción exacta de los isómeros formados depende de la temperatura de la reacción. A medida que aumenta la temperatura, se obtienen proporciones crecientes del isómero 4 y menos del isómero 2.
Esto se debe a que la sulfonación es reversible. El grupo ácido sulfónico puede caerse del anillo de nuevo y volver a unirse en otro lugar. Esto tiende a favorecer la formación del isómero termodinámicamente más estable. Este intercambio ocurre más a temperaturas más altas.
El isómero 4 es más estable porque no hay desorden en la molécula como lo habría si el grupo metilo y el grupo ácido sulfónico estuvieran al lado el uno del otro.
Oxidación de cadena lateral en alquilbencenos
Un alquilbenceno es simplemente un anillo de benceno con un grupo alquilo unido a él. El metilbenceno es el alquilbenceno más simple.
Los grupos alquilos suelen ser bastante resistentes a la oxidación. Sin embargo, cuando se unen a un anillo de benceno, se oxidan fácilmente por una solución alcalina de manganato de potasio(VII) (permanganato de potasio).
El metilbenceno se calienta bajo reflujo con una solución de manganato de potasio(VII) alcalino con carbonato de sodio. El color púrpura del manganato de potasio(VII) es eventualmente reemplazado por un precipitado marrón oscuro de óxido de manganeso(IV).
La mezcla se acidifica finalmente con ácido sulfúrico diluido.
en General, el metilbenceno se oxida a ácido benzoico.
![]()
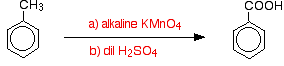
Curiosamente, cualquier grupo alquilo se oxida de nuevo a un grupo-COOH en el anillo bajo estas condiciones. Así, por ejemplo, el propilbenceno también se oxida a ácido benzoico.
![]()