Idiopathic intracranial hypertension
Assessment | Biopsychology | Comparative |Cognitive | Developmental | Language | Individual differences |Personality | Philosophy | Social |
Methods | Statistics |Clinical | Educational | Industrial |Professional items |World psychology |
Biological:Behavioural genetics · Evolutionary psychology · Neuroanatomy · Neurochemistry · Neuroendocrinology ·Neuroscience · Psychoneuroimmunology · Physiological Psychology · Psychopharmacology(Index, Outline)
MRI brain.jpg|
| ICD-10 | G932 | |
|---|---|---|
| ICD-9 | 348.2 | |
| OMIM | 243200 | |
| DiseasesDB | 1331 | |
| MedlinePlus | 000351 | |
| eMedicine | neuro/329 oph/190 neuro/537 | |
| MeSH | {{{MeshNumber}}} | |
Hipertensión intracraneal idiopática (IIH), a veces llamada por los nombres más antiguos intracraneal benigno la hipertensión (BIH) o pseudotumor cerebral (PTC), es un trastorno neurológico que se caracteriza por un aumento de la presión intracraneal (presión alrededor de la cerebro) en ausencia de un tumor u otras enfermedades. Los síntomas principales son dolor de cabeza, náuseas y vómitos, así como tinnitus pulsátil (zumbido en los oídos sincronizado con el pulso), visión doble y otros síntomas visuales. Si no se trata, puede provocar hinchazón del disco óptico en el ojo, que puede progresar a pérdida de la visión.
IIH se diagnostica con un escáner cerebral (para descartar otras causas) y una punción lumbar; la punción lumbar también puede proporcionar un alivio temporal y, a veces, permanente de los síntomas. Algunos responden a los medicamentos (con el medicamento acetazolamida), pero otros requieren cirugía para aliviar la presión. La afección puede ocurrir en todos los grupos de edad, pero es más común en mujeres jóvenes, especialmente en aquellas con obesidad.
Signos y síntomas
El síntoma más común de IIH es el dolor de cabeza, que ocurre en casi todos los casos (92-94%). Es característicamente peor por la mañana, de carácter generalizado y de naturaleza palpitante. Puede estar asociado con náuseas y vómitos. El dolor de cabeza puede empeorar con cualquier actividad que aumente aún más la presión intracraneal, como toser y estornudar. El dolor también se puede experimentar en el cuello y los hombros. Muchos tienen tinnitus pulsátil, una sensación de zumbido en uno o ambos oídos (64-87%); este sonido es sincrónico con el pulso. Varios otros síntomas, como entumecimiento de las extremidades, debilidad generalizada, pérdida del olfato e incoherencia, se reportan más raramente; ninguno es específico para IIH. En los niños, pueden estar presentes numerosos signos y síntomas inespecíficos.
El aumento de la presión conduce a la compresión y tracción de los nervios craneales, un grupo de nervios que surgen del tronco encefálico y que irrigan la cara y el cuello. Con mayor frecuencia, el nervio abducente (sexto nervio) está involucrado. Este nervio suministra el músculo que tira del ojo hacia afuera. Por lo tanto, las personas con parálisis del sexto nervio experimentan visión doble horizontal que es peor cuando miran hacia el lado afectado. Más raramente, el nervio oculomotor y el nervio troclear (parálisis del tercer y cuarto nervio, respectivamente) se ven afectados; ambos desempeñan un papel en los movimientos oculares. El nervio facial (séptimo nervio craneal) se ve afectado ocasionalmente the el resultado es debilidad total o parcial de los músculos de la expresión facial en uno o ambos lados de la cara.
El aumento de la presión provoca papiledema, que es la hinchazón del disco óptico, el punto donde el nervio óptico entra en el globo ocular. Esto ocurre en prácticamente todos los casos de IIH, pero no todos experimentan síntomas de esto. Aquellos que experimentan síntomas generalmente reportan «oscurecimientos visuales transitorios», episodios de dificultad para ver que ocurren en ambos ojos, pero no necesariamente al mismo tiempo. El edema papilar no tratado a largo plazo conduce a la pérdida visual, inicialmente en la periferia, pero progresivamente hacia el centro de la visión.
El examen físico del sistema nervioso suele ser normal, aparte de la presencia de papiledema, que se observa al examinar el ojo con un pequeño dispositivo llamado oftalmoscopio o con más detalle con una cámara de fondo de ojo. Si hay anomalías en los nervios craneales, se pueden notar en el examen ocular en forma de bizqueo (parálisis del tercer, cuarto o sexto nervio) o como parálisis del nervio facial. Si el papiledema ha sido de larga data, los campos visuales pueden estar constreñidos y la agudeza visual puede disminuir. Se recomienda realizar pruebas de campo visual mediante perimetría automatizada (Humphrey), ya que otros métodos de prueba pueden ser menos precisos. El papiledema de larga duración conduce a atrofia óptica, en la que el disco se ve pálido y la pérdida visual tiende a ser avanzada.
Causas
«Idiopática» significa «de etiología desconocida». Por lo tanto, la HII solo se puede diagnosticar si no hay una explicación alternativa para los síntomas. La presión intracraneal puede aumentar debido a medicamentos como derivados de alta dosis de vitamina A (por ejemplo, isotretinoína para el acné), antibióticos de tetraciclina a largo plazo (para una variedad de afecciones de la piel) y anticonceptivos hormonales. Hay muchas otras enfermedades, en su mayoría afecciones raras, que pueden conducir a hipertensión intracraneal. Si hay una causa subyacente, la afección se denomina «hipertensión intracraneal secundaria». Las causas comunes de hipertensión intracraneal secundaria incluyen apnea obstructiva del sueño (un trastorno respiratorio relacionado con el sueño), lupus eritematoso sistémico (LES), enfermedad renal crónica y enfermedad de Behçet.
Mecanismo
Se desconoce la causa de la IIH. La regla de Monro-Kellie establece que la presión intracraneal (literalmente: presión dentro del cráneo) está determinada por la cantidad de tejido cerebral, líquido cefalorraquídeo (LCR) y sangre dentro de la bóveda craneal ósea. Por lo tanto, existen tres teorías sobre por qué la presión podría aumentarse en IIH: exceso de producción de LCR, aumento del volumen de sangre o tejido cerebral u obstrucción de las venas que drenan sangre del cerebro.
La primera teoría, la del aumento de la producción de líquido cefalorraquídeo, fue propuesta en las descripciones tempranas de la enfermedad. Sin embargo, no hay datos experimentales que apoyen un rol para este proceso en IIH.
La segunda teoría postula que el aumento del flujo sanguíneo al cerebro o el aumento en el tejido cerebral en sí puede resultar en el aumento de la presión. Se ha acumulado poca evidencia para apoyar la sugerencia de que el aumento del flujo sanguíneo juega un papel, pero tanto las muestras de biopsia como varios tipos de escáneres cerebrales han mostrado un mayor contenido de agua en el tejido cerebral. No está claro por qué podría ser así.
La tercera teoría sugiere que el flujo sanguíneo del cerebro puede estar deteriorado o congestionado. Solo en una pequeña proporción de pacientes se ha demostrado un estrechamiento subyacente de los senos o venas cerebrales. La congestión de la sangre venosa puede ser el resultado de un aumento general de la presión venosa, que se ha relacionado con la obesidad.
Diagnóstico
El diagnóstico puede sospecharse sobre la base de la historia clínica y el examen. Para confirmar el diagnóstico, además de excluir causas alternativas, se requieren varias investigaciones; se pueden realizar más investigaciones si la historia clínica no es típica o si el paciente tiene más probabilidades de tener un problema alternativo: niños, hombres, ancianos o mujeres que no tienen sobrepeso.
Investigaciones
La neuroimagen, generalmente con tomografía computarizada (TC / TAC) o imágenes por resonancia magnética (RM), descarta lesiones masivas. En IIH estas exploraciones pueden ser normales, aunque se pueden ver ventrículos pequeños o con forma de hendidura y «signo de sella vacío» (aplanamiento de la glándula pituitaria debido al aumento de la presión). También se realiza una venografía por RMN en todos los casos (o, según algunos expertos, solo en casos atípicos) para excluir la posibilidad de obstrucción venosa o trombosis del seno venoso cerebral.
La punción lumbar se realiza para medir la presión de apertura, así como para obtener líquido cefalorraquídeo (LCR) para excluir diagnósticos alternativos. Si se aumenta la presión de apertura, se puede extraer el líquido cefalorraquídeo para aliviarlo (ver más abajo). El LCR se examina en busca de células anormales, niveles de glucosa y proteínas; en IIH, todos están dentro de los límites normales. Ocasionalmente, la medición de la presión puede ser normal a pesar de los síntomas muy sugestivos. Esto puede atribuirse al hecho de que la presión del líquido cefalorraquídeo puede fluctuar a lo largo del día. Si la sospecha sigue siendo alta, puede ser necesario realizar una monitorización a más largo plazo de la PIC mediante un catéter de presión.
Clasificación
Los criterios originales para IIH fueron descritos por Dandy en 1937.
1 Signos & síntomas de aumento de la presión del ICP – CSF >25 cmH2O
2no signos de localización con la excepción de parálisis del nervio abducente
3Normal Composición del LCR
4 Ventrículos normales a pequeños (hendiduras) en imágenes sin masa intracraneal
Fueron modificados por Smith en 1985 para convertirse en los «criterios Dandy modificados». Smith incluyó el uso de imágenes más avanzadas: Dandy había requerido ventriculografía, pero Smith la reemplazó con tomografía computarizada. En un artículo de 2001, Digre y Corbett modificaron aún más los criterios de Dandy. Agregaron el requisito de que el paciente esté despierto y alerta, ya que el coma impide una evaluación neurológica adecuada y requiere la exclusión de la trombosis del seno venoso como causa subyacente. Además, añaden el requisito de que no se encuentre ninguna otra causa para el PCI planteado.
1 Síntomas de aumento de la presión intracraneal (dolor de cabeza, náuseas, vómitos, oscurecimientos visuales transitorios o edema papilar)
2 Sin signos de localización con excepción de parálisis abducente (sexto nervio)
3 El paciente está despierto y alerta
4 Hallazgos normales de TC/RM sin evidencia de trombosis
Presión de apertura de 5 LP de>25 cmH2O y composición bioquímica y citológica normal del LCR
6No hay otra explicación para el aumento de la presión intracraneal
En una revisión de 2002, Friedman y Jacobson propone un conjunto de criterios alternativos, derivados del de Smith, que requieren la ausencia de síntomas que no puedan explicarse por un diagnóstico de IIH, pero no requieren la presencia real de ningún síntoma (como dolor de cabeza) atribuible a IIH. Estos criterios también requieren que la punción lumbar se realice con el paciente acostado de lado, ya que una punción lumbar realizada en posición sentada erguida puede conducir a mediciones de presión artificialmente alta. Friedman y Jacobson tampoco insisten en la venografía por RMN para todos los pacientes; más bien, esto solo se requiere en casos atípicos (consulte «diagnóstico» más arriba).
Tratamiento
El objetivo principal en el tratamiento de la HII es la prevención de la pérdida visual y la ceguera, así como el control de los síntomas. La AIH se trata principalmente mediante la reducción de la presión del líquido cefalorraquídeo y, en su caso, la pérdida de peso. La IIH puede resolverse después del tratamiento inicial, puede entrar en remisión espontánea (aunque todavía puede recaer en una etapa posterior) o puede continuar de forma crónica.
punción Lumbar
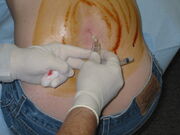
Una punción lumbar en el progreso. Se ha lavado un área grande en la parte posterior con un desinfectante a base de yodo que deja una coloración marrón. En esta imagen, el paciente está sentado en posición vertical, lo que puede hacer que el procedimiento sea más fácil de realizar, pero hace que cualquier medición de la presión de apertura no sea confiable.
El primer paso en el control de los síntomas es el drenaje del líquido cefalorraquídeo por punción lumbar. Si es necesario, esto se puede realizar al mismo tiempo que un LP» diagnóstico». En algunos casos, esto es suficiente para controlar los síntomas, y no se necesita tratamiento adicional.
El procedimiento se puede repetir si es necesario, pero esto generalmente se toma como una señal de que se pueden requerir tratamientos adicionales para controlar los síntomas y preservar la visión; los pacientes consideran que los LPs repetidos son desagradables. A veces se necesitan LPs repetidos para controlar la PIC con urgencia si la visión se deteriora rápidamente.
Medicación
El tratamiento médico mejor estudiado es la acetazolamida (Diamox), que actúa inhibiendo la enzima anhidrasa carbónica y reduce la producción de LCR entre un seis y un 57 por ciento. Puede causar los síntomas de hipopotasemia (niveles bajos de potasio en sangre), que incluyen debilidad muscular y hormigueo en los dedos. La acetazolamida no se puede usar en el embarazo, ya que ha demostrado causar anomalías embrionarias en estudios en animales, y en humanos ha demostrado causar acidosis metabólica, así como alteraciones en los niveles de electrolitos en sangre en el recién nacido. El diurético furosemida a veces se usa si la acetazolamida no se tolera, pero esto tiene poco efecto en la PIC.
Se pueden usar varios analgésicos (analgésicos) para controlar el dolor de cabeza. Además de los agentes convencionales como el paracetamol, una dosis baja del antidepresivo amitriptilina, así como del anticonvulsivo topiramato, han mostrado algún beneficio adicional para aliviar el dolor.
El uso de esteroides para reducir la PIC es controvertido; pueden usarse en papiledema grave, pero de lo contrario se desaconseja su uso.
Cirugía
Existen dos procedimientos quirúrgicos principales en el tratamiento de la HII: descompresión de la vaina del nervio óptico y fenestración y derivación. La cirugía normalmente solo se ofrecería si la terapia médica no tiene éxito o no se tolera. La elección entre estos dos procedimientos depende del problema predominante en IIH. Ninguno de los dos procedimientos es perfecto: ambos pueden causar complicaciones significativas y, con el tiempo, ambos pueden fallar en el control de los síntomas. No hay ensayos controlados aleatorios que guíen la decisión sobre qué procedimiento es el mejor.
La fenestración de la vaina del nervio óptico es una operación oftalmológica que consiste en hacer una incisión en el revestimiento de tejido conectivo del nervio óptico en su porción detrás del ojo. No está del todo claro cómo protege el ojo de la presión elevada, pero puede ser el resultado de la desviación del LCR hacia la órbita o la creación de un área de tejido cicatricial que reduce la presión. Los efectos sobre la presión intracraneal en sí son más modestos. Además, el procedimiento puede llevar a complicaciones significativas, incluida la ceguera en un 1-2%. Por lo tanto, el procedimiento se recomienda principalmente en aquellos que tienen síntomas limitados de dolor de cabeza, pero un edema papilar significativo o una visión amenazada, o en aquellos que se han sometido a un tratamiento fallido con una derivación o tienen una contraindicación para la cirugía de derivación.
La cirugía de derivación, generalmente realizada por neurocirujanos, implica la creación de un conducto por el cual el LCR puede drenarse a otra cavidad corporal. El procedimiento inicial suele ser una derivación lumboperitoneal (LP), que conecta el espacio subaracnoideo en la columna lumbar con la cavidad peritoneal. Generalmente, se incluye una válvula de presión en el circuito para evitar un drenaje excesivo cuando el paciente está erecto y, por lo tanto, tiene una PIC relativamente alta. La derivación de LP proporciona alivio a largo plazo en aproximadamente la mitad de los casos; otros requieren revisión de la derivación, a menudo en más de una ocasión, generalmente debido a la obstrucción de la derivación. Si la derivación lumboperitoneal necesita revisiones repetidas, se puede considerar una derivación ventriculoauricular o ventriculoperitoneal. Estas derivaciones se insertan en uno de los ventrículos laterales del cerebro, generalmente mediante cirugía estereotáctica, y luego se conectan a la aurícula derecha del corazón o a la cavidad peritoneal, respectivamente. Dada la menor necesidad de revisiones en las derivaciones ventriculares, es posible que este procedimiento se convierta en el tipo de tratamiento de primera línea de derivación.
En los casos de obesidad grave, se ha demostrado que la cirugía de bypass gástrico conduce a una marcada mejoría de los síntomas.
Pronóstico
No se sabe qué porcentaje de personas con IIH remitirán espontáneamente y qué porcentaje desarrollará enfermedad crónica.
IIH normalmente no afecta a la esperanza de vida. Las principales complicaciones de IIH surgen del papiledema no tratado o resistente al tratamiento. En varias series de casos, el riesgo a largo plazo de que la visión de uno se vea significativamente afectada por IIH se encuentra entre el 10 y el 25%.
Epidemiología
La incidencia de IIH está fuertemente determinada por el sexo y el peso corporal. Las cifras de mujeres corresponden a mujeres de entre 20 y 45 años de edad.
En promedio, el IIH ocurre en aproximadamente 1 por cada 100,000 personas, y puede ocurrir en niños y adultos. La edad media en el momento del diagnóstico es de 30 años. La HII ocurre predominantemente en mujeres, especialmente en las edades de 20 a 45 años, que tienen de cuatro a ocho veces más probabilidades de verse afectadas que los hombres. El sobrepeso y la obesidad predisponen fuertemente a una persona a IIH: las mujeres que superan en más de un diez por ciento su peso corporal ideal tienen trece veces más probabilidades de desarrollar IIH, y esta cifra aumenta hasta diecinueve veces en las mujeres que superan en más de un veinte por ciento su peso corporal ideal. En los hombres, esta relación también existe, pero el aumento es solo de cinco veces en aquellos que superan el 20% de su peso corporal ideal.
A pesar de varios informes de IIH en familias, no hay una causa genética conocida para IIH. Personas de todas las etnias pueden desarrollar IIH. En los niños, no hay diferencia en la incidencia entre hombres y mujeres.
De las bases de datos nacionales de admisión hospitalaria se desprende que la necesidad de intervención neuroquirúrgica para IIH ha aumentado notablemente en el período comprendido entre 1988 y 2002. Esto se ha atribuido al menos en parte a la creciente prevalencia de obesidad, aunque parte de este aumento puede explicarse por la creciente popularidad de la derivación sobre la fenestración de la vaina del nervio óptico.
Historia
El primer reporte de IIH fue por el médico alemán Heinrich Quincke, quien lo describió en 1893 bajo el nombre de meningitis serosa. El término «pseudotumor cerebri» fue introducido en 1904 por su compatriota Max Nonne. Muchos otros casos aparecieron posteriormente en la literatura; en muchos casos, el aumento de la presión intracraneal puede haber sido el resultado de condiciones subyacentes. Por ejemplo, la hidrocefalia otitica reportada por el neurólogo de Londres Sir Charles Symonds puede haber sido el resultado de una trombosis del seno venoso causada por una infección del oído medio. Los criterios de diagnóstico para IIH fueron desarrollados en 1937 por el neurocirujano de Baltimore Walter Dandy; Dandy también introdujo la cirugía descompresiva subtemporal en el tratamiento de la afección.
Los términos «benigno » y» seudotumor » se derivan del hecho de que el aumento de la presión intracraneal puede estar relacionado con tumores cerebrales. Por lo tanto, a aquellos pacientes en los que no se encontró ningún tumor se les diagnosticó «pseudotumor cerebral» (una enfermedad que imita un tumor cerebral). La enfermedad pasó a llamarse «hipertensión intracraneal benigna» en 1955 para distinguirla de la hipertensión intracraneal debido a enfermedades potencialmente mortales (como el cáncer); sin embargo, esto también se consideró engañoso porque cualquier enfermedad que pueda cegar a alguien no debe considerarse benigna, por lo que el nombre se revisó en 1989 a «hipertensión intracraneal idiopática (sin causa identificable)».
La cirugía de derivación se introdujo en 1949; inicialmente, se utilizaron derivaciones ventriculoperitoneales. En 1971, se reportaron buenos resultados con la derivación lumboperitoneal. Los informes negativos sobre la derivación en la década de 1980 llevaron a un breve período (1988-1993) durante el cual la fenestración del nervio óptico (que inicialmente se había descrito en una condición no relacionada en 1871) fue más popular. Desde entonces, se recomienda la derivación predominantemente, con excepciones ocasionales.
Véase también
- Hipertensión
- 1.00 1.01 1.02 1.03 1.04 1.05 1.06 1.07 1.08 1.09 1.10 1.11 1.12 1.13 1.14 1.15 1.16 1.17 1.18 1.19 1.20 1.21 1.22 1.23 1.24 1.25 1.26 1.27 Binder DK, Horton JC, Lawton MT, McDermott MW (marzo de 2004). Hipertensión intracraneal idiopática. Neurocirugía 54 (3): 538-51; discusión 551-2.
- Sismanis A (julio de 1998). Tinnitus pulsátil. Una experiencia de 15 años. Am J Otol 19 (4): 472-7.
- 3,0 3,1 3,2 3,3 3,4 3,5 3,6 Soler D, Cox T, Bullock P, Calver DM, Robinson RO (enero de 1998). Diagnóstico y manejo de la hipertensión intracraneal benigna. Arco. Dis. Niño. 78 (1): 89–94.
- 4.0 4.1 4.2 4.3 4.4 4.5 4.6 4.7 4.8 Friedman DI, Jacobson DM (2002). Criterios diagnósticos para hipertensión intracraneal idiopática. Neurology 59 (10): 1492-1495.
- 5.00 5.01 5.02 5.03 5.04 5.05 5.06 5.07 5.08 5.09 5.10 5.11 5.12 5.13 5.14 5.15 5.16 5.17 5.18 Acheson JF (2006). Idiopathic intracranial hypertension and visual function. Br. Med. Bull. 79-80 (1): 233–44.
- 6.0 6.1 6.2 Dandy WE (October 1937). Intracranial pressure without brain tumor – diagnosis and treatment. Ann. Surg. 106 (4): 492–513.
- Smith JL (1985). Whence pseudotumor cerebri?. J. Clin. Neuroophthalmol. 5 (1): 55–6.
- 8.0 8.1 Digre KB, Corbett JJ (2001). Idiopathic intracranial hypertension (pseudotumor cerebri): A reappraisal. Neurologist 7: 2–67.
- Curry WT, Butler WE, Barker FG (2005). Aumento rápido de la incidencia de procedimientos de derivación del líquido cefalorraquídeo para la hipertensión intracraneal idiopática en los Estados Unidos, 1988-2002. Neurocirugía 57 (1): 97-108; discusión 97-108. Quincke HI (1893). Meningitis serosa. Samml. Klin. Vortr. 67: 655.
- Nonne M (1904). Ueber Falle vom Symptomkomplex «Tumor Cerebral» mit Ausgang in Heilung (Pseudotumor Cerebral). Dtsch. Z. Nervenheilk. 27 (3-4): 169–216.
- 12.0 12.1 12.2 Johnston I (2001). The historical development of the pseudotumor concept (en inglés). Neurocirugía. Enfoque 11 (2): 1.
- Symonds CP (1931). Otitic hidrocefalia. Brain 54 (3705): 55-71. Foley J (1955). Formas benignas de hipertensión intracraneal; tóxicos y otitic hidrocefalia. Brain 78 (1): 1-41. Corbett JJ, Thompson HS (octubre de 1989). El manejo racional de la hipertensión intracraneal idiopática. Arco. Neurol. 46 (10): 1049–51. Bandyopadhyay S (2001). Pseudotumor cerebral. Arco. Neurol. 58 (10): 1699–701.
- Idiopathic intracranial hypertension at the Open Directory Project
|
v·d·e
Nervous system disorders, primarily CNS (G04–G47, 323–349) |
||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Inflammation |
|
Both/either
|
||||||||||||||||||||||
| Brain/ encephalopathy |
|
|||||||||||||||||||||||
| Spinal cord/ myelopathy |
Syringomyelia · Syringobulbia · Morvan’s syndrome · Vascular myelopathy (Foix-Alajouanine syndrome) · Spinal cord compression |
|||||||||||||||||||||||
| Both/either |
|
|
||||||||||||||||||||||
| {| class=»navbox collapsible nowraplinks» style=»margin:auto; « | ||||||||||||||||||||||||
|
··
|
||||||||||||||||||||||||
|
||||||||||||||||||||||||
|}
This page uses Creative Commons Licensed content from Wikipedia (view authors).