Zespół niespokojnych nóg: częste, słabo zdiagnozowane zaburzenie
US Pharm . 2009;34(1):24-29.
Zespół Niespokojnych Nóg (RLS) jest częstym zaburzeniem czuciowo-ruchowym ośrodkowego układu nerwowego. Charakteryzuje się nieodpartą chęcią lub potrzebą poruszania kończynami, która występuje w wyniku niewygodnych odczuć kończyn. Chociaż RLS zwykle zaczyna się w nogach, może rozprzestrzeniać się na inne części ciała, takie jak ramiona lub tułów. Osoby cierpiące na RLS często opisują zaburzenie jako uczucie, jak woda płynąca wewnątrz nóg, „robaki w kościach” lub elektryczność w nogach. Objawy te mogą występować przez cały dzień, ale zwykle nasilają się w okresach bezczynności i wieczorem. Osoby z RLS zwykle muszą poruszać kończynami w celu całkowitego lub częściowego złagodzenia niewygodnych doznań. W nocy RLS często wiąże się z okresowymi ruchami kończyn (PLMs), które mogą powodować problemy ze snem, a także utrudniać wykonywanie siedzących czynności, takich jak siedzenie wygodnie w samochodzie lub w samolocie przez dłuższy czas.
przyczyna RLS pozostaje niejasna, ale badania sugerują, że upośledzona aktywność dopaminy w mózgu z powodu niewydolności żelaza może wywoływać RLS u osób z predyspozycjami genetycznymi. RLS mogą być klasyfikowane jako pierwotne lub wtórne ze względu na inne schorzenie, takie jak schyłkowa choroba nerek (ESRD) lub ciąży. Agoniści dopaminy, tacy jak ropirynol i pramipeksol, są w leczeniu pierwszego rzutu RLS z objawami dobowymi. Dostępne są alternatywne terapie w przypadkach opornych na leczenie lub utrzymujących się objawów. Ten artykuł bada częstość występowania, etiologia, i diagnoza RLS, jak również dostępnych metod leczenia.
częstość występowania
badania epidemiologiczne donoszą, że 7,2% do 11% ogólnej populacji w Europie i Ameryce Północnej cierpi na jakąś formę RLS.1,2 w samych Stanach Zjednoczonych uważa się, że RLS wpływa na ponad 10 milionów dorosłych i szacunkowo 1,5 miliona dzieci i młodzieży, przy podobnym wskaźniku między chłopcami i dziewczętami.1,3 kobiety są około dwukrotnie bardziej podatne na RLS niż mężczyźni (9% vs. 5,4%).1,2 RLS jest bardziej powszechne u osób starszych, ale po 79 roku życia jego częstość ma tendencję do zmniejszania.1 klinicznie istotne przypadki RLS występują u 2, 7% do 3% populacji.1,2 pomimo wysokiej częstości występowania, zespół ten pozostaje słabo zdiagnozowany i niepokojący dla wielu pacjentów.
etiologia
etiologia RLS nie jest w pełni poznana. Badania wykazały, że nie jest to strukturalny problem neurodegeneracyjny, ale raczej dotyczy układu dopaminowego, zastoju żelaza homeo lub genetyki. Poniższa dyskusja podsumowuje bieżące przemyślenia na temat każdej z tych trzech potencjalnych przyczyn.
układ dopaminowy: próby wykazania, że układ dopaminowy jest nieprawidłowy u osób z RLS nie przyniosły ostatecznych wyników. Wyniki badań neuroobrazowania sugerują raczej dysfunkcję dopaminy niż niewydolność.Udział dopaminy w RLS jest potwierdzony odpowiedzią kliniczną na agonistów dopaminy w leczeniu pierwotnych RLS.Dokładny mechanizm działania agonistów dopaminy w łagodzeniu objawów RLS nie jest znany.
homeostaza żelaza: badanie autopsji wykazało zmniejszenie zapasów żelaza w substantia nigra u pacjentów z RLS.Tak więc, jedną z możliwych przyczyn RLS może być niezdolność mózgu do utrzymania prawidłowego poziomu żelaza. Żelazo jest również kofaktorem w produkcji dopaminy. W innym badaniu wykazano możliwy związek między zaburzoną homeostazą żelaza a zaburzeniami czynności dopaminy.8 dalsze badania są potrzebne do określenia roli żelaza w RLS.
genetyka: doświadczenie kliniczne wykazało silne połączenie rodzinne w RLS. Do tej pory zgłoszono kilka loci, ale gen chorobotwórczy nie został jeszcze zidentyfikowany.9,10 ogólnie przyjmuje się, że RLS następuje autosomalny dominujący tryb dziedziczenia, który wymaga tylko jednego dotkniętego rodzica, aby przekazać cechę potomstwu. Potrzebne są dalsze badania genetyczne, aby rzucić światło na genotyp osób cierpiących na RLS.
diagnoza
diagnoza RLS opiera się w całości na wywiadach z pacjentem i historii objawów. Kryteria diagnostyczne zostały ustanowione w 1995 r. przez międzynarodową grupę badawczą ds. zespołu niespokojnych nóg (IRLSSG)i zmienione w 2003 r. 11, 12. Wszystkie cztery podstawowe kryteria muszą być obecne w celu ustalenia diagnozy RLS. Wspomagające cechy kliniczne pomagają w diagnostyce bardziej skomplikowanych przypadków. Powiązane cechy są obecne w większości przypadków RLS i może dalej prowadzić lekarzy w diagnostyce.

pierwotny RLS
pierwotny RLS został zidentyfikowany jako mający bardziej podstępny początek objawów niż wtórny RLS. Występuje częściej u osób poniżej 40 roku życia. Pacjenci ci są również bardziej narażeni na innych członków rodziny z zaburzeniem. Krytycznym krokiem w leczeniu pacjentów z pierwotnym RLS jest ustalenie częstości i nasilenia ich objawów. Jeden algorytm leczenia dzieli pierwotny RLS na trzy kategorie w zależności od ciężkości objawu13:
przerywany RLS wymaga sporadycznego leczenia objawów, ale nie jest wystarczająco ciężki, aby wymagać codziennej terapii lekami. Osoby z przerywanym RLS mają łagodniejsze objawy i są łatwiejsze w leczeniu. Leczenie bezlekowe jest zwykle preferowanym podejściem pierwszego rzutu.
Codzienny RLS charakteryzuje się uporczywymi objawami, które muszą być zarządzane za pomocą codziennej terapii lekami. Leczenie farmakologiczne jest leczeniem z wyboru.
oporny na leczenie RLS jest dziennym RLS, który nie reaguje na leczenie co najmniej jednym lekiem pierwszego rzutu w zwykłej dawce. Należy spełnić co najmniej jedno z następujących kryteriów: niezdolność do uzyskania odpowiedniej odpowiedzi na leczenie; niezadowalająca odpowiedź w czasie pomimo zwiększenia dawki preferowanego środka; nie do zniesienia działania niepożądane; i nasilenie objawów pomimo dodatkowych dawek leku.
wtórny RLS
wtórny RLS jest związany z bardziej nagłym początkiem i zwykle występuje w połączeniu z lub w wyniku innego stanu, takiego jak niedobór żelaza, ESRD lub ciąża. Objawy wtórnego RLS nie są odróżnialne od objawów pierwotnego RLS, ale leczenie celuje w stan podstawowy.
leczenie pierwotnego RLS
leczenie niefarmakologiczne
w łagodnym RLS należy najpierw wypróbować metody niefarmakologiczne. We wszystkich innych przypadkach terapia bezlekowa może być stosowana oprócz terapii lekowej w celu złagodzenia objawów czuciowo-ruchowych i zaburzeń snu. Leczenie nonfarmakologiczne obejmuje rozwijanie dobrych nawyków snu, takich jak regularny harmonogram snu; zapewnienie cichego, ciemnego otoczenia w sypialni; i unikanie wyzwalaczy RLS (telewizja, kofeina, nikotyna, alkohol) w pobliżu snu.13 zaleca się łagodne do umiarkowanych czynności umysłowych (gry wideo, łamigłówki) i fizycznych (prace domowe, ćwiczenia) w okresach, w których pacjenci są najbardziej podatni na objawy, takie jak wieczorem oraz w okresach bezczynności lub odpoczynku. Siedzący tryb życia, takie jak loty samolotem, długie przejażdżki samochodem i filmy, są zalecane rano, gdy objawy RLS mają tendencję do ustępowania w intensywności.
farmakologiczne leczenie
farmakologiczne leczenie RLS jest objawowe. Nie leczy choroby, ale zarządza jej niepokojącymi przejawami. Leki farmakologiczne stosowane w leczeniu RLS to lewodopa (L-dopa), agoniści dopaminy, gabapentyna, opioidy i benzodiazepiny.
l-Dopa: L-Dopa jest prekursorem dopaminy. Jest on formułowany razem z inhibitorem dekarboksylazy karbidopą (Sinemet), który zapobiega rozpadowi L-dopa w osoczu obwodowym. Karbidopa pomaga zmniejszyć ilość L-dopa potrzebną o 75%. Gdy L-dopa przekroczy barierę krew-mózg, przekształca się w dopaminę. W przypadku choroby Parkinsona leczenie karbidopą/L-dopa rozpoczyna się zwykle od dawki 25 mg / 100 mg trzy razy na dobę; w przypadku przerywanego RLS, połączenie L-dopa i karbidopy stosowano w mniejszych dawkach w razie potrzeby ze względu na jego natychmiastowe działanie i brak konieczności miareczkowania.13 preparaty L-dopa o przedłużonym uwalnianiu z dłuższymi okresami półtrwania zostały zbadane pod kątem alternatywnego stosowania u pacjentów, którzy często są budzeni przez objawy w nocy z powodu krótkiego działania formy o natychmiastowym uwalnianiu.14 obecnie na rynku amerykańskim nie ma produktów l-dopa z pojedynczym podmiotem.
u pacjentów z RLS, l-dopa wywołuje typowe dopaminergiczne działania niepożądane, takie jak nudności, wymioty, senność, zawroty głowy, niedociśnienie i ból głowy. Najbardziej szkodliwy efekt uboczny, augmentacja, zapobiega jego stosowaniu w codziennym RLS.Augmentacja polega na pogorszeniu objawów RLS wcześniej w ciągu dnia po wieczornej dawce leku, zwiększeniu nasilenia objawów i rozprzestrzenianiu się objawów na inne części ciała, takie jak ramiona lub tułów.
agoniści dopaminy: agoniści dopaminy są terapią pierwszego rzutu w dobowym RLS.Ze względu na korzystniejsze profile działań niepożądanych, preferowane są agoniści Nonergot, tacy jak ropinirol i pramipeksol, niż agoniści sporyszu, tacy jak pergolid i kabergolina. Pergolid i kabergolina, które okazały się zwiększać ryzyko niedomykalności zastawki serca, obecnie nie są dostępne w USA z powodu tego szkodliwego działania niepożądanego.
Ropinirol (Requip) był pierwszym lekiem zatwierdzonym przez FDA (w 2005 r.) do leczenia umiarkowanego do ciężkiego pierwotnego RLS. Jest to pełny wewnętrzny agonista nonergoliny dla podtypów receptora dopaminy D2 i D3. Trzy duże badania kliniczne wykazały skuteczność i tolerancję ropinirolu w leczeniu RLS.5,17,18 we wszystkich trzech badaniach pacjentów randomizowano do grupy otrzymującej ropinirol lub placebo według elastycznego schematu dostosowywania dawki od 0,25 mg do 4 mg/dobę, jako tolerowane, przyjmowane raz na dobę na jedną do trzech godzin przed snem. Wyniki oceniano za pomocą międzynarodowej skali oceny RLS (IRLS)-pierwszorzędowego pomiaru wyników-oraz skali CGI-I (Clinical Global Impressions-Improvement scale). IRLS składa się z sekcji 10, które oceniają nasilenie objawów czuciowych i motorycznych, zaburzenia snu, wpływ na czynności codziennego życia i nastrój związany z RLS. W oparciu o IRLS, wszystkie trzy badania wykazały, że ropinirol skutecznie zmniejszał podstawowe objawy RLS – takie jak nasilenie i częstotliwość objawów, a także problemy ze snem-i skutecznie zwiększał ogólne samopoczucie. Najczęściej zgłaszanymi działaniami niepożądanymi były nudności i ból głowy, typowe dla agonistów dopaminy. W badaniach tych nie oceniano oficjalnie nasilenia i nie udokumentowano doniesień o nasileniu choroby.
pramipeksol (Mirapex), zatwierdzony przez FDA w 2006 r.do leczenia umiarkowanej do ciężkiej dziennej RLS, jest kolejnym pełnym agonistą receptora D2 i D3 nonergoliny. Skuteczność pramipeksolu oceniano w kilku badaniach klinicznych.6,19,20 wszyscy pacjenci otrzymywali pramipeksol (0,125 mg-0,75 mg) w razie potrzeby i tolerowany lub placebo raz na dobę na dwie do trzech godzin przed snem. We wszystkich badaniach dwa miary wyników stosowane do oceny skuteczności to IRLS i CGI-I. Poprawę zaobserwowano zarówno w subiektywnych, jak i obiektywnych miarach RLS. Często zgłaszanymi działaniami niepożądanymi były nudności, ból głowy i zmęczenie. Zwiększenie dawki nie zostało formalnie ocenione, chociaż niektóre udokumentowane doniesienia o zwiększeniu dawki pramipeksolu pojawiły się w badaniach retrospektywnych.21,22
Inne metody leczenia: Gabapentyna, benzodiazepiny i opioidy są pomocnymi środkami drugiego rzutu, które są odpowiednią alternatywną terapią dla przypadków RLS obejmujących specyficzne objawy, takie jak ciągłe zaburzenia snu lub bolesne odczucia kończyn.
większość badań dotyczących RLS dotyczy gabapentyny przeciwdrgawkowej (Neurontin), która okazała się przydatna w przypadku RLS i neuropatii obwodowej.23,24 Gabapentyna, strukturalny Analog kwasu gamma-aminomasłowego, działa poprzez zmniejszenie subiektywnych objawów RLS.Ze względu na to, że gabapentyna może powodować senność, może być stosowana jako środek wspomagający RLS, który wiąże się z uporczywymi problemami ze snem.Konieczne są dodatkowe badania w celu oceny długotrwałego działania przewlekłej monoterapii gabapentyną.
istnieje stosunkowo niewiele opublikowanych badań na temat stosowania benzodiazepin do RLS. W badaniach klinicznych badano jedynie klonazepam i alprazolam. Ze względu na ich właściwości uspokajające, te dwa środki były używane głównie do wywoływania snu. Małe badanie klonazepamu wykazało, że lek był skuteczny w nocnym RLS ze względu na jego zdolność do wywoływania i utrzymywania snu; jednak nie zmniejszał PLMs podczas snu.25 większa częstość występowania senności w ciągu dnia i zaburzeń poznawczych była podobno związana z dłuższym działaniem leku. Ogólnie rzecz biorąc, benzodiazepiny są uważane za opcję drugiego rzutu dla RLS, która wiąże się ze znaczną bezsennością.
sposób działania opioidowych leków przeciwbólowych w RLS jest nieznany. Jedno retrospektywne badanie kliniczne z udziałem pacjentów otrzymujących długotrwałą monoterapię opioidami (oksykodon, propoksyfen, kodeinę lub metadon) w pierwotnym RLS wykazało, że opioidy były bardzo skuteczne w łagodzeniu objawów motorycznych i zaburzeń snu i praktycznie nie powodowały tolerancji ani uzależnienia fizycznego (występujące tylko u jednego z 36 pacjentów w monoterapii).Autorzy zalecili dobór opioidu na podstawie nasilenia dolegliwości pacjenta. Inne badanie sugerowało, że tramadol (Ultram) ma mniejszy potencjał nadużywania i mniej skutków ubocznych niż inne opioidy i że powinien być opioidem z wyboru w leczeniu RLS.W ciężkich, opornych przypadkach zaleca się stosowanie metadonu doustnego ze względu na długi okres półtrwania.
leczenie wtórnego RLS
u niektórych pacjentów rozwija się RLS w wyniku innego stanu. Do 26% kobiet w ciąży ma wpływ na objawy RLS, zwłaszcza w trzecim trymestrze ciąży.Wysoka częstość występowania RLS występuje u osób ze schyłkową niewydolnością nerek oraz u osób z niedoborem żelaza.31,32 leczenie wtórnego RLS koncentruje się na identyfikacji i leczeniu przyczyny. W ciąży leczenie jest wstrzymane, ponieważ kobiety doświadczają całkowitego odwrócenia objawów po porodzie. Przeszczep nerki–ale nie dializa — jest leczniczy dla RLS w ESRD. Jeśli zapasy żelaza są małe, można podać dożylnie żelazo.Lekarze powinni oceniać pacjentów pod kątem innych substancji, które mogą nasilać objawy RLS, takich jak metoklopromid, wszystkie neuroleptyki, wiele leków przeciwdepresyjnych i przeciwhistaminowych. W miarę możliwości należy przerwać stosowanie tych leków.
rola farmaceuty w RLS
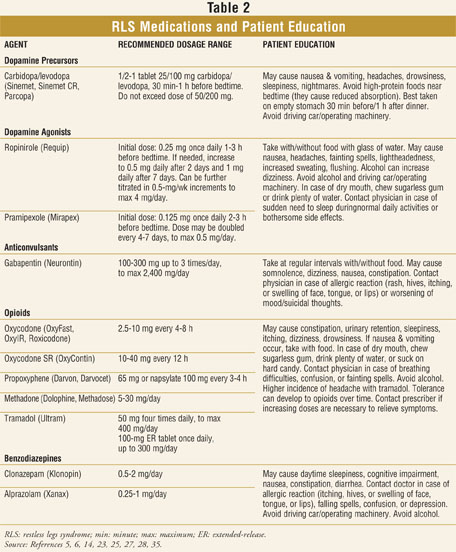
farmaceuci powinni mieć wiedzę i umieć rozpoznać typowe objawy RLS, takie jak nieprzyjemne odczucia w łydkach, udach, stopach, a nawet ramionach. Te odczucia są często opisywane przez pacjentów jako” pełzanie”,” pełzanie”,” mrowienie”,” roztrzęsione”,” głęboko osadzone „lub” pieczenie.”Chociaż opis RLS może się znacznie różnić u pacjentów, wspólnym elementem jest pragnienie lub potrzeba poruszania kończynami, które pogarszają się wieczorami i powodują trudności w zasypianiu lub pozostaniu we śnie. Osoby dotknięte RLS mogą również skarżyć się na zmęczenie, nastrój depresyjny lub brak koncentracji.Farmaceuci mogą rozważyć zalecenie, aby pacjenci z objawami RLS porozmawiali z lekarzem pierwszego kontaktu w sprawie skierowania do neurologa lub odpowiedniego specjalisty ds. snu na podstawie oceny i zaleceń lekarza. Ważne jest również, aby farmaceuci byli zaznajomieni z najczęstszymi lekami na RLS i oferowali odpowiednie doradztwo w zakresie ich właściwego stosowania i możliwych działań niepożądanych (tabela 2).
istnieją różne zasoby online, które mogą dostarczyć dodatkowych informacji o RLS. Fundacja RLS (www.rls.org) jest najlepszym ogólnym źródłem informacji RLS. Strona zawiera listę grup wsparcia, czat, aktualne recenzje zabiegów RLS i porady ekspertów. Inne zasoby online są we MOVE (www.wemove.org) i mówić o śnie (www.talkaboutsleep.com).
1. Allen RP, Walters AS, Montplaisir J, et al. Zespół niespokojnych nóg częstość występowania i wpływ: badanie populacji ogólnej REST. Arch Intern Med. 2005;165:1286-1292.
2. Hening w, Walters AS, Allen RP, et al. Wpływ, diagnostyka i leczenie zespołu niespokojnych nóg (RLS) w populacji podstawowej opieki zdrowotnej: badanie Rest (RLS epidemiology, symptoms, and treatment) primary care. Sleep Med. 2004;5:237-246.
3. Picchietti D, Allen RP, Walters AS, et al. Zespół niespokojnych nóg: występowanie i wpływ u dzieci i młodzieży-badanie pediatryczne. Pediatria. 2007;120:253-266.
4. Wetter TC, Eisensehr i, Trenkwalder C. Functional neuroimaging studies in restless legs syndrome. Sleep Med. 2004;5:401-406.
5. Trenkwalder C, Garcia-Borreguero D, Montagna P, et al. Ropinirol w leczeniu zespołu niespokojnych nóg: wyniki badania TREAT RLS 1, trwającego 12 tygodni, randomizowanego, kontrolowanego placebo badania w 10 krajach europejskich. J Neurol Neurochirurg Psychiatria. 2004;75:92-97.
6. Winkelman JW, Sethi KD, Kushida CA, et al. Skuteczność i bezpieczeństwo pramipeksolu w zespole niespokojnych nóg. Neurologia. 2006;67:1034-1039.
7. Connor JR, Boyer PJ, Menzies SL i inni. Badania neuropatologiczne sugerują zaburzenia nabywania żelaza w mózgu w zespole niespokojnych nóg. Neurologia. 2003;61:304-309.
8. Wang X, Wiesinger J, Beard J, et al. Ekspresja Thy1 w mózgu jest wpływ żelaza i zmniejsza się w zespole niespokojnych nóg. J Neurol Sci. 2004;220:59-66.
9. Mathias RA, Hening w, Washburn M, et al. Analiza segregacji zespołu niespokojnych nóg: możliwe dowody na duży gen w badaniu rodzinnym z zastosowaniem ślepej diagnozy. Hum Hered.
10. Desautels a, Turecki G, Xiong L, et al. Analiza mutacyjna neurotensyny w rodzinnym zespole niespokojnych nóg. Mov Disord. 2004;19:90-94.
11. Walters AS. W kierunku lepszej definicji zespołu niespokojnych nóg. International Restless Legs Syndrome Study Group. Mov Disord. 1995;10:634-642.
12. Allen RP, Picchietti D, Henning WA, et al. Zespół niespokojnych nóg: kryteria diagnostyczne, szczególne względy i epidemiologia. Relacja z warsztatów diagnostyki i epidemiologii zespołu niespokojnych nóg w Narodowym Instytucie Zdrowia. Sleep Med. 2003;4:101-119.
13. Silber MH, Ehrenberg BL, Allen RP, et al. Algorytm leczenia zespołu niespokojnych nóg. Mayo Clin Proc. 2004;79:916-922.
14. Trenkwalder C, Collado Seidel V, Kazenwadel J, et al. Jednoroczne leczenie lewodopą o standardowym i o przedłużonym uwalnianiu: odpowiednie długotrwałe leczenie zespołu niespokojnych nóg? Mov Disord.
15. Allen RP, Earley CJ. Nasilenie zespołu niespokojnych nóg karbidopą / lewodopą. Śpij.
16. Schade R, Andersohn F, Suissa s, et al. Agonistów dopaminy i ryzyko niedomykalności zastawki serca. N Engl J Med. 2007;356:29-38.
17. Walters AS, Ondo WG, Dreykluft T, et al. Ropinirol jest skuteczny w leczeniu zespołu niespokojnych nóg. Leczenie RLS 2: 12-tygodniowe, podwójnie zaślepione, randomizowane, kontrolowane placebo badanie w grupach równoległych. Mov Disord. 2004;19:1414-1423.
18. Bogan RK, Fry JM, Schmidt MH, et al. Ropinirol w leczeniu pacjentów z zespołem niespokojnych nóg: randomizowane, podwójnie zaślepione, kontrolowane placebo badanie kliniczne z siedzibą w USA. Mayo Clin Proc.
19. Oertel WH, Stiasny-Kolster K, Bergtholdt B, et al. Skuteczność pramipeksolu w leczeniu zespołu niespokojnych nóg: sześciotygodniowe, wieloośrodkowe, randomizowane badanie z podwójnie ślepą próbą (badanie effect – RLS). Mov Disord.
20. Trenkwalder C, Stiasny-Kolster K, Kupsch A, et al. Kontrolowane odstawienie pramipeksolu po 6 miesiącach leczenia otwartego u pacjentów z zespołem niespokojnych nóg. Mov Disord.
21. Ferini-Strambi L. Zespół Niespokojnych Nóg Sleep Med.
22. Winkelman JW, Johnston L. Augmentation and tolerance with long-term pramipexole treatment of restless legs syndrome (RLS). Sleep Med. 2004;5:9-14.
23. Happe S, Klösch G, Saletu B, Zeitlhofer J. leczenie idiopatycznego zespołu niespokojnych nóg (RLS) gabapentyną. Neurologia. 2001;57:1717-1719.
24. Garcia-Borreguero D, Larrosa O, de la Llave y, et al. Leczenie zespołu niespokojnych nóg za pomocą gabapentyny: podwójnie ślepe badanie krzyżowe. Neurologia. 2002;59:1573-1579.
25. Saletu M, Anderer P, Saletu-Zyhlarz G, et al. Zespół niespokojnych nóg (RLS) i okresowe zaburzenia ruchu kończyn (PLMD): ostre, kontrolowane placebo badania laboratoryjne dotyczące snu z użyciem klonazepamu. EUR Neuropsychofarmakol. 2001;11:153-161.
26. Schenck CH, Mahowald MW. Długotrwałe, nocne leczenie benzodiazepinami szkodliwych parasomni i innych zaburzeń zakłóconego snu nocnego u 170 osób dorosłych. Am J Med.
27. Walters AS, Winkelmann J, Trenkwalder C, et al. Długotrwała obserwacja pacjentów z zespołem niespokojnych nóg leczonych opioidami. Mov Disord. 2001;16:1105-1109.
28. Lauerma H, Markkula J. leczenie zespołu niespokojnych nóg tramadolem: badanie otwarte. J Clin Psychiatry. 1999;60:241-244.
29. Ondo WG. Metadon na oporny zespół niespokojnych nóg. Mov Disord. 2005;20:345-348.
30. Manconi M, Govoni V, De Vito A, et al. Zespół niespokojnych nóg a ciąża. Neurologia.
31. Gigli GL, Adorati m, Dolso P, et al. Zespół niespokojnych nóg w schyłkowej fazie choroby nerek. Sleep Med. 2004;5:309-315.
32. Sun ER, Chen CA, Ho G, et al. Żelazo i zespół niespokojnych nóg. Śpij. 1998;21:371-377.
33. Earley CJ, Heckler D, Allen RP. Powtarzane dożylne dawki żelaza zapewniają skuteczne uzupełniające leczenie zespołu niespokojnych nóg. Sleep Med. 2005;6:301-305.
34. Kushida C, Martin M, Nikam P, et al. Obciążenie zespołem niespokojnych nóg dla jakości życia związanej ze zdrowiem. Qual Life Res. 2007;16: 617-624.
35. Fakty & porównania. Fakty & porównanie 4.0 .www.factsandcomparisons.com. dostęp 31 sierpnia 2008. 2006;62:157-164. 2003;18:1184-1189. 1996;19:205-213. 2006;81:17-27. 2007;22:213-219. 2006;21:1404-1410. 2002; 3 (suppl): S23-S25. 1996;100:333-337. 2004;63:1065-1069.