etiketti: MEGACE es – megestroliasetaattisuspensio
Kliininen farmakologia
megestroliasetaattipitoisuuksien arvioimiseen plasmassa on useita analyysimenetelmiä, kuten kaasukromatografia-mass fragmentography (GC-MF), korkeapaine nestekromatografia (HPLC) ja radioimmunoanalyysi (Ria). GC-MF-ja HPLC-menetelmät ovat spesifisiä megestroliasetaatin ja saanto-ekvivalenttien pitoisuuksien osalta. Ria-menetelmä reagoi megestroliasetaattimetaboliittien kanssa, joten se on epäspesifinen ja osoittaa suurempia pitoisuuksia kuin GC-MF-ja HPLC-menetelmät. Plasmapitoisuudet riippuvat paitsi käytetystä menetelmästä, myös lääkkeen suoliston ja maksan inaktivaatiosta, johon voivat vaikuttaa tekijät, kuten suoliston motiliteetti, suolistobakteerit, annetut antibiootit, kehon paino, ruokavalio ja maksan toiminta.
vaikutusmekanismi
useat tutkijat ovat raportoineet megestroliasetaatin ruokahalua lisäävästä ominaisuudesta ja sen mahdollisesta käytöstä kakeksiassa. Tarkkaa mekanismia, jolla megestroliasetaatti vaikuttaa anoreksiaan ja kakeksiaan, ei tällä hetkellä tunneta.
farmakokineettiset ominaisuudet:
Megestroliasetaatin pitoisuus plasmassa annettaessa 625 mg (125 mg/mL) Megace® es-oraalisuspensiota vastaa ruokintaolosuhteissa 800 mg (40 mg / mL) megestroliasetaatti-oraalisuspensiota (KS.alla oleva kuva).
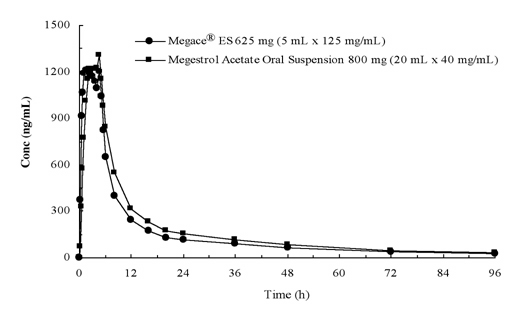
Megace® ES-annosten suhteellisuuden selvittämiseksi tehtiin farmakokineettisiä tutkimuksia eri annosalueilla, kun niitä annettiin paastossa ja ruokittuna. Megestrolin farmakokinetiikka oli lineaarinen annosvälillä 150-675 mg Megace® es-annoksen jälkeen riippumatta ateriatilasta. Rasvaisen aterian yhteydessä Cmax suureni 48% ja AUC 36% verrattuna 625 mg: n Megace® es-annoksen paastoannokseen (Taulukko 1). Runsasrasvainen ateria nosti kuitenkin megestrolin AUC-arvon 2-kertaiseksi ja Cmax-arvon 7-kertaiseksi verrattuna niihin, jotka olivat paastotilassa 800 mg: n annoksen jälkeen alkuperäisessä lääkemuodossa. Annon jälkeen turvallisuudessa ei ollut eroa ruokintatilassa, joten Megace® ES voitiin ottaa aterioista riippumatta.
|
*megestrol acetate oral suspension |
||||||||||||||||
| Table 1 – Pharmacokinetic Studies Conducted with Megace® ES | ||||||||||||||||
| Amount Dosed | 150 mg | 250 mg | 375 mg | 450 mg | 575 mg | 625 mg | 675 mg | 800 mg* | ||||||||
| Dose | 5 mL | 5 mL | 5 mL | 5 mL | 5 mL | 5 mL | 5 mL | 20 mL | ||||||||
| Fast | Fed | Fast | Fed | Fast | Fed | Fast | Fed | Fast | Fed | Fast | Fed | Fast | Fed | Fast | Fed | |
| Cmax (ng/mL) | 412 | 379 | 647 | 588 | 810 | 958 | 955 | 1079 | – | 1421 | 1133 | 1618 | 1044 | 1616 | 187 | 1364 |
| AUC0-∞ (ng∙h/mL) | 3058 | 3889 | 5194 | 6328 | 7238 | 12193 | 9483 | 11800 | – | 14743 | 12095 | 16268 | 11879 | 17029 | 8942 | 18625 |
| Tmax (h) | 1.74 | 3.80 | 1.58 | 3.38 | 1.56 | 3.42 | 1.74 | 3.16 | – | 3.75 | 1.72 | 2.91 | 1.96 | 2.76 | 5.89 | 3.85 |
Megestroliasetaatin vakaan tilan farmakokinetiikkaa plasmassa arvioitiin 10 aikuisella, kakektisella miespotilaalla, joilla oli hankittu immuunivajavuusoireyhtymä (AIDS) ja tahaton painon lasku yli 10% lähtötilanteesta. Potilaat saivat megestroliasetaatti-oraalisuspensiota suun kautta kerta-annoksena 800 mg/vrk 21 päivän ajan. Päivänä 21 saatuja plasmapitoisuustietoja arvioitiin 48 tunnin ajan viimeisen annoksen jälkeen.
Megestroliasetaatin keskimääräinen (±1SD) huippupitoisuus plasmassa (Cmax) oli 753 (±539) ng / mL. Pitoisuus-aikakäyrän alle jäävän alueen keskiarvo (AUC) oli 10476 (±7788) ng x h/mL. Tmax-arvon mediaani oli viisi tuntia. Seitsemän potilasta kymmenestä lihoi kolmessa viikossa.
lisäksi 24 aikuiselle, oireettomalle HIV-seropositiiviselle mieskoehenkilölle annettiin kerran vuorokaudessa 750 mg megestroliasetaatti-oraalisuspensiota. Hoitoa annettiin 14 vuorokautta. Keskimääräiset Cmax-arvot olivat 490 (±238) ng/mL ja AUC-arvot 6779 (±3048) H x ng/mL. Tmax-arvon mediaani oli kolme tuntia. Keskimääräinen Cmax-arvo oli 202 (±101) ng/mL. Keskimääräinen % vaihteluarvosta oli 107 (±40).
metabolia
virtsasta tunnistetut Megestroliasetaattimetaboliitit muodostivat 5-8% annetusta annoksesta. Hengitysteihin erittyminen merkittynä hiilidioksidina ja rasvan varastoitumisena on saattanut selittää ainakin osan radioaktiivisuudesta, jota ei esiinny virtsassa ja ulosteessa.
eliminaatio
lääkkeen pääasiallinen eliminoitumistie ihmisillä on virtsa. Kun radioaktiivisesti merkittyä megestroliasetaattia annettiin ihmisille 4-90 mg: n annoksina, virtsaan erittyminen oli 10 päivän kuluessa 56, 5-78, 4% (keskiarvo 66, 4%) ja ulosteeseen erittyminen 7, 7-30, 3% (keskiarvo 19, 8%). Kokonaisradioaktiivisuus vaihteli 83, 1%: n ja 94, 7%: n välillä (keskiarvo 86, 2%).
erityisryhmät
megestroliasetaatin farmakokinetiikkaa ei ole tutkittu missään erityisryhmässä.
ELÄINFARMAKOLOGIA ja / tai toksikologia
Pitkäaikainen Megace ® es (megestroliasetaatti)-hoito saattaa lisätä hengitystieinfektioiden riskiä. Rotilla tehdyssä kaksi vuotta kestäneessä kroonisessa toksisuus-/karsinogeenisuustutkimuksessa havaittiin, että hengitystieinfektiot, lymfosyyttien väheneminen ja neutrofiilien lisääntyminen lisääntyivät.
kliinisten tutkimusten kuvaus
megestroliasetaatti-oraalisuspensio annoksella 800 mg/20 mL vastaa 625 mg / 5 mL Megace ® ES-valmistetta. Megestroliasetaatti – Oraalisuspension kliinistä tehoa arvioitiin kahdessa kliinisessä tutkimuksessa. Yksi oli satunnaistettu lumekontrolloitu monikeskustutkimus, jossa megestroliasetaattia (ma) verrattiin 100 mg: n, 400 mg: n ja 800 mg: n vuorokausiannoksilla lumelääkkeeseen AIDS-potilailla, joilla oli anoreksia/kakeksia ja merkittävää painon laskua. Tutkimukseen osallistuneista 270 potilaasta 195 täytti kaikki tutkimukseen osallistumiseen / poissulkemiseen liittyvät kriteerit, heille oli tehty vähintään kaksi ylimääräistä painomittausta lähtötilanteen jälkeen 12 viikon aikana tai yksi painomittaus lähtötilanteen jälkeen, mutta he keskeyttivät hoidon epäonnistumisen vuoksi. Niiden potilaiden prosentuaalinen osuus, joiden paino nousi enimmillään viisi kiloa 12 tutkimusviikon aikana, oli tilastollisesti merkitsevästi suurempi MA-hoitoa saaneissa 800 mg: n (64%) ja 400 mg: n (57%) ryhmissä kuin lumelääkeryhmässä (24%). Keskimääräinen paino nousi lähtötilanteesta viimeiseen arviointiin 12 tutkimusviikon aikana 800 mg MA-hoitoa saaneessa ryhmässä 7: llä.8 kiloa, 400 mg MA-ryhmä 4,2 kiloa, 100 mg MA-ryhmä 1,9 kiloa ja laski lumelääkeryhmässä 1,6 kiloa. Painon keskimääräiset muutokset 4, 8 ja 12 viikon kohdalla potilailla, joiden teho voitiin arvioida kahdessa kliinisessä tutkimuksessa, on esitetty graafisesti. Biosähköisellä impedanssianalyysillä mitatut muutokset kehonkoostumuksessa 12 tutkimusviikon aikana osoittivat, että ma-hoitoa saaneiden ryhmien paino nousi ilman vettä (KS.taulukko kliinisistä tutkimuksista). Lisäksi turvotus kehittyi tai paheni vain 3 potilaalla.
suuremmilla MA-hoitoa saaneiden potilaiden prosentuaalisilla osuuksilla 800 mg: n ryhmässä (89%), 400 mg: n ryhmässä (68%) ja 100 mg: n ryhmässä (72%) kuin lumelääkeryhmässä (50%) havaittiin ruokahalun paranevan 12 tutkimusviikon aikana. 800 mg MA-hoitoa saaneiden ryhmän ja plaseboryhmän välillä havaittiin tilastollisesti merkitsevä ero kalorisaannin muutoksessa lähtötilanteesta aikaan, jolloin paino muuttui maksimaalisesti. Potilaita pyydettiin arvioimaan painon muutosta, ruokahalua, ulkonäköä ja yleistä käsitystä hyvinvoinnista 9 kysymyksen kyselyssä. Maksimaalisessa painomuutoksessa vain 800 mg MA-hoitoa saanut ryhmä sai vastauksia, jotka olivat tilastollisesti merkitsevästi suotuisampia kaikkiin kysymyksiin verrattuna lumelääkettä saaneeseen ryhmään. Tutkimuksessa havaittiin annosvaste, jonka myönteiset vasteet korreloivat suurempaan annokseen kaikissa kysymyksissä.
toinen tutkimus oli satunnaistettu, kaksoissokkoutettu lumekontrolloitu monikeskustutkimus, jossa verrattiin megestroliasetaattia 800 mg/vrk lumelääkkeeseen AIDS-potilailla, joilla oli anoreksia / kakeksia ja merkittävää painon laskua. Tutkimukseen osallistuneista 100 potilaasta 65 täytti kaikki tutkimukseen osallistumiseen / poissulkemiseen liittyvät kriteerit, heille oli tehty vähintään kaksi ylimääräistä painomittausta lähtötilanteen jälkeen 12 viikon aikana tai yksi painomittaus lähtötilanteen jälkeen, mutta he keskeyttivät hoidon epäonnistumisen vuoksi. 800 mg MA-hoitoa saaneiden potilaiden keskimääräinen painon muutos oli tilastollisesti merkitsevästi suurempi kuin lumeryhmän potilaiden. Lähtötilanteesta tutkimusviikolle 12 keskimääräinen paino nousi MA-hoitoa saaneessa ryhmässä 11, 2 kiloa ja laski 2, 1 kiloa lumelääkeryhmässä. Biosähköisellä impedanssianalyysillä mitatut muutokset kehonkoostumuksessa osoittivat muun kuin veden painon nousua MA-käsitellyllä ryhmällä (KS.kliinisten tutkimusten taulukko). Ma-hoitoa saaneessa ryhmässä ei todettu turvotusta. Ruokahalu parani 12 tutkimusviikon aikana viimeisessä arvioinnissa suuremmalla prosentilla MA-hoitoa saaneista potilaista (67%) kuin lumelääkettä saaneista potilaista (38%); tämä ero oli tilastollisesti merkitsevä. Hoitoryhmien välillä ei ollut tilastollisesti merkitseviä eroja keskimääräisessä kalorien muutoksessa tai päivittäisessä kalorien saannissa aikaan maksimaaliseen painon muutokseen. Samassa 9 kysymyksen tutkimuksessa, johon viitattiin ensimmäisessä tutkimuksessa, potilaiden arviot painon muutoksesta, ruokahalusta, ulkonäöstä ja yleisestä käsityksestä hyvinvoinnista osoittivat keskimääräisten pisteiden lisääntyneen MA-hoitoa saaneilla potilailla lumelääkeryhmään verrattuna.
molemmissa tutkimuksissa potilaat sietivät lääkettä hyvin, eikä hoitoryhmien välillä havaittu tilastollisesti merkitseviä eroja laboratorioarvojen poikkeavuuksissa, uusissa opportunistisissa infektioissa, lymfosyyttien määrissä, T4-määrissä, T8-määrissä tai ihoreaktiotesteissä (KS.kontraindikaatiot kohta).
| Megestrol Acetate Oral Suspension Clinical Efficacy Trials | |||||||
| Trial 1 | Trial 2 | ||||||
| Study Accrual Dates | Study Accrual Dates | ||||||
| 11/88 to 12/90 | 5/89 to 4/91 | ||||||
| Megestrol Acetate, mg/day | 0 | 100 | 400 | 800 | 0 | 800 | |
| Entered Patients | 38 | 82 | 75 | 75 | 48 | 52 | |
| Evaluable Patients | 28 | 61 | 53 | 53 | 29 | 36 | |
| Mean Change in Weight (lb.) | |||||||
| Baseline to 12 Weeks | 0.0 | 2.9 | 9.3 | 10.7 | -2.1 | 11.2 | |
| % Patients ≥ 5 Pound Gain | |||||||
| At Last Evaluation in 12 weeks | 21 | 44 | 57 | 64 | 28 | 47 | |
| Mean Changes in Body Composition: | |||||||
| Fat Body Mass (lb.) | 0.0 | 2.2 | 2.9 | 5.5 | 1.5 | 5.7 | |
| Lean Body Mass (lb.) | -1.7 | -0.3 | 1.5 | 2.5 | -1.6 | -0.6 | |
| Water (liters) | -1.3 | -0.3 | 0.0 | 0.0 | -0.1 | -0.1 | |
| % Patients With Improved Appetite: | |||||||
| At Time of Maximum Weight Change | 50 | 72 | 72 | 93 | 48 | 69 | |
| At Last Evaluation in 12 Weeks | 50 | 72 | 68 | 89 | 38 | 67 | |
| Mean Change in Daily Caloric Intake: | |||||||
| Baseline to Time of Maximum Weight Change | -107 | 326 | 308 | 646 | 30 | 464 | |
| *Based on bioelectrical impedance analysis determinations at last evaluation in 12 weeks |
Presented below are the results of mean weight changes for patients evaluable for efficacy in trials 1 and 2.