16.2: viruksen elinkaaret
lysogeeninen reitti
parempi vaihtoehto joillekin bakteeriviruksille on nimeltään lysogeeninen reitti. Bakteriofagi, jolla on tämä vaihtoehto, sekä lyyttinen reitti, tunnetaan lauhkeana faagina. Tällä reitillä virus menee lepotilaan integroimalla isäntägenomiin ja pysymällä transkriptioiden mukaisesti lepäävänä, kunnes ympäristöolosuhteet muuttuvat ja heijastavat todennäköisyyttä, että useampi isäntäsolu infektoituu (Kuva \(\PageIndex{4}\)).
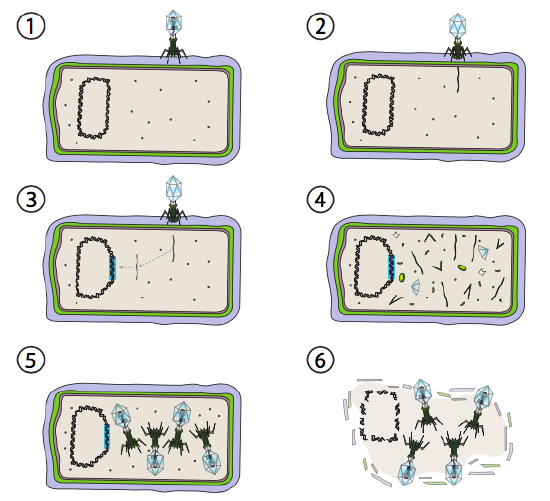
Lambda (λ) on esimerkki lauhkeasta bakteriofagista. Infektion ja genomiruiskutuksen alkuvaiheet ovat samat kuin Lyytisen syklin, mutta lysogeniaa edistävissä olosuhteissa viruksen genomi integroidaan isäntägenomiin vaiheessa 3. Λ integroinnissa E. coli, tämä tapahtuu vastavuoroisella rekombinaatiolla 15-emäsparin sekvenssissä, joka tunnetaan att λ-kohtana, ja sitä helpottaa Int-geenituote. Niin kauan kuin ympäristöolosuhteet eivät ole suotuisat bakteerien lisääntymiselle (ja siten rajallinen määrä mahdollisia isäntäsoluja), viruksen perimä pysyy enimmäkseen piilossa ja toimimattomana. Ainoa merkittävä poikkeus on λ-repressoria koodaava geeni, joka estää seuraavan vaiheen ja pitää viruksen lepotilassa.
seuraava vaihe on λ: n faagi-DNA: n irrottaminen isäntäkromosomista ja sitä seuraava viruksen DNA: n replikaatio ja transkriptio (Kuva \(\PageIndex{4}\), Vaihe 4). Sitten, kuten ennenkin, viimeiset vaiheet ovat virionien kokoaminen ja kasautuminen, ja lopulta solurakenteen hajoaminen ja viruspartikkelien vapautuminen.
jotta viruksen genomit voidaan pakata kapsidien ahtaaseen tilaan, niiden on oltava erittäin taloudellisia. Esimerkiksi HIV: n genomissa (Kuva \(\PageIndex{6}\)) on useita geenejä, jotka menevät päällekkäin.
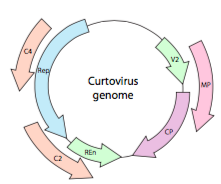
tai curtovirusten tapauksessa ssDNA – kasvivirukset (esim.juurikkaiden kihara top-virus), genomissa ei ole ainoastaan Ylireagoivia geenejä, vaan se on jopa kaksisuuntainen (Kuva \(\PageIndex{7}\)), joka koodaa geenituotteita molemmissa DNA-säikeissä sen jälkeen, kun ssDNA on muuntunut dsDNA: ksi.
mitä geenejä viruksista löytyy talouden tarpeen vuoksi? Yksi tutkituimmista viruksen genomeista, bakteriofagi λ, sisältää geenejä, jotka koodaavat viittä transkriptiokontrolliproteiinia (mitkä niistä ilmaistaan riippuu siitä, onko faagi lysogeenisessä vai lyyttisessä tilassa), sitoutuvaa proteiinia, joka ohjaa transkriptioaktivaattorin hajoamista, 17 kapsidiproteiinia, eksisionaasia, joka ohjaa faagigenomin irrottamista ja lisäämistä isäntägenomiin, integraatioproteiinia, joka lisää faagigenomin isännän genomiin, ja 3 geeniä, jotka osallistuvat isäntäsolun lyysiin.
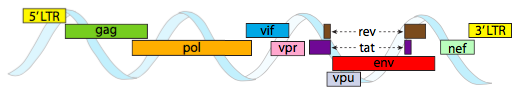
yllä kuvattu HI-viruksen perimä on paljon λ: ta pienempi, noin 9 kilobaasia verrattuna 48 kb: hen, mutta jälleen teemana on käyttää soluproteiineja mahdollisuuksien mukaan ja koodata viruksen geenejä tarvittaessa. Niinpä gag koodaa kapsidiproteiineja, pol koodaa käänteiskopioijaentsyymiä, integraasia ja HIV-proteaasia (joka pilkkoo gag-ja pol-geenituotteet funktionaalisiin proteiineihinsa), vif toimii yhteistä isäntäsolun antiviraalista entsyymiä vastaan, vpr säätelee ydinenergian tuontia, tat lisää voimakkaasti HIV-geenien transkriptiota, rev vie virus-RNA: ta tumasta, VPU: ta tarvitaan isännän hiukkasten orastamiseen, env koodaa viruksen kirjekuoren glykoproteiineja ja nef edistää infektoituneiden solujen selviytymistä. LTR-alueet ovat erittäin voimakkaita promoottoreita näiden geenien voimakkaaseen ilmentymiseen.
vaikka sitä ei kutsuta lysogeniaksi, jotkut eläinvirukset voivat käyttäytyä samalla tavalla. Näkyvin esimerkki ovat Baltimoren Vi – luokan virukset-yleisesti retrovirukset, joista yksi on HIV. Retroviruksen reitti eukaryoottisen isäntäsolun läpi on kuvattu alla (g. 5).
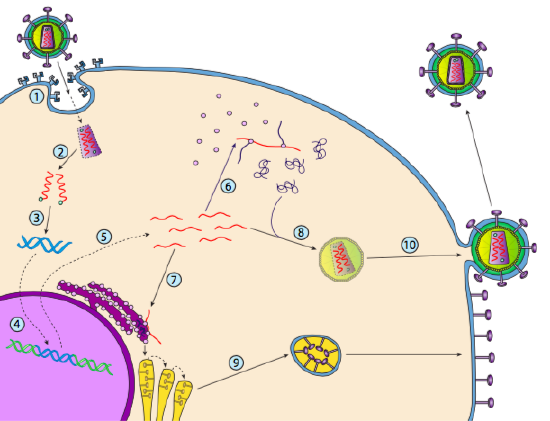
HIV: llä on kirjekuori, jossa on isäntäsolun tunnistamia transmembraaniproteiineja, jotka sitovat viruksen solun pintaan ja aloittavat reseptorivälitteisen endosytoosin (1). Endosytoosin jälkeen virionin kalvokuori ja vesikulaarisen kalvosulake vapauttavat kapsidin ja sen sisällön (2). Kun kapsidi hajoaa sytoplasmassa, viruksen RNA: n kaksi juostetta vapautuvat yhdessä erityisen polymeraasin kanssa: käänteiskopioijaentsyymin, joka lukee RNA-mallin ja syntetisoi DNA: ta. Käänteiskopioijaentsyymi käyttää uutta DNA: ta myös täydentävän DNA – juosteen syntetisoimiseen niin, että se lopulta tuottaa viruksen perimästä kaksijuosteisen DNA-version (3). Tämä viruksen dsDNA kulkeutuu tumaan, jossa se integroituu isäntägeeniin toisen virusproteiinin, integraasin
(4), avulla. Viruksen DNA: ta kutsutaan provirukseksi. Provirus voi olla lepotilassa, mutta jos se aktivoituu, se transkriboidaan ja tuloksena oleva virus-RNA kuljetetaan ulos tumasta (5). Osa viruksen RNA: sta koodaa entsyymejä, kuten käänteiskopioijaentsyymejä ja integraasia eli kapsidiproteiineja, jotka kaikki valmistetaan sytoplasmassa (6), mutta osa koodaa kalvoon sitoutuneita glykoproteiineja, jotka translokoituvat ER: ään (7) ja lopulta prosessoituvat Golgin läpi ja liitetään plasmakalvoon (9). Kun virioni on koottu (8), se sitoutuu viruksen transmembraaniproteiineihin nukleoimalla eksosyyttisen ”vesikkelin” (10), joka on virioni, jossa on viruksen kuori.
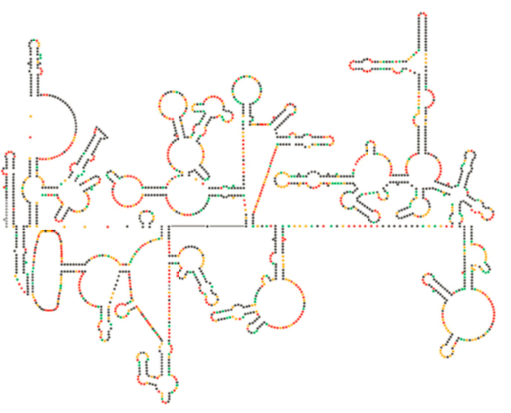
HIV-genomin tuore rakenteellinen tutkimus viittaa siihen, että itse HIV-RNA: n rakenteella saattaa olla merkittävä rooli sen etenemisessä isäntäsolujen sisällä. Kuvassa \(\PageIndex{8}\), teoksesta Watts et al, Nature 460:711-716, 2009, esitetään genomin ennustettu sekundaarirakenne. Kirjoittajat ehdottavat, että RNA-rakenne voi itse asiassa olla vuorovaikutuksessa ribosomaalisen venymän kanssa virusproteiinien taittumisen hillitsemiseksi. He myös postuloivat tämän väitteen laajentamisen koskemaan tärkeää geneettistä informaatiota, joka on koodattu ei vain nukleotidisekvenssiin, vaan minkä tahansa RNA-viruksen sekundaarirakenteeseen ja tertiäärirakenteeseen.
tarkasteltaessa viruksia tämän integratiivisen luvun muun osan suhteen on pidettävä mielessä kaksi ensisijaista ajatusta. Ensinnäkin viruksen eloonjääminen perustuu numeroihin: sen täytyy tehdä valtavia määriä sen komponentteja luodakseen mahdollisimman laajan verkon uusille isäntäsoluille. Tätä varten viruksen promoottorit ovat yleensä paljon vahvempia kuin isäntäsolun promoottorit, jotka samanaikaisesti ajavat enemmän viruksen geeniekspressiota ja estävät isäntägeeniekspression (omistamalla soluresursseja viruksen tuotantoon). Toiseksi nopeiden sukupolviaikojen vuoksi viruksen mutaatio – ja evoluutionopeus on paljon nopeampi kuin normaalit eukaryoottiset genomit. Lisäksi, jos virus käyttää omaa polymeraasiaan (kuten käänteiskopioijaentsyymiä tai RNA-replikaasia), mutaationopeus nousee entisestään, koska viruspolymeraasien virhetarkistus ei onnistu.