16.2: Virale Livssykluser
Den Lysogene Vei
et bedre alternativ for noen bakterielle virus kalles lysogene vei. Bakteriofagen som har dette alternativet, samt en lytisk vei, er kjent som temperert fag. I denne veien går viruset inn i dvalen ved å integrere seg i vertsgenomet, og gjenværende transkripsjonelt hvilende til miljøforholdene endres og reflekterer en sannsynlighet For at flere vertsceller infiserer (Figur \(\PageIndex{4}\)).
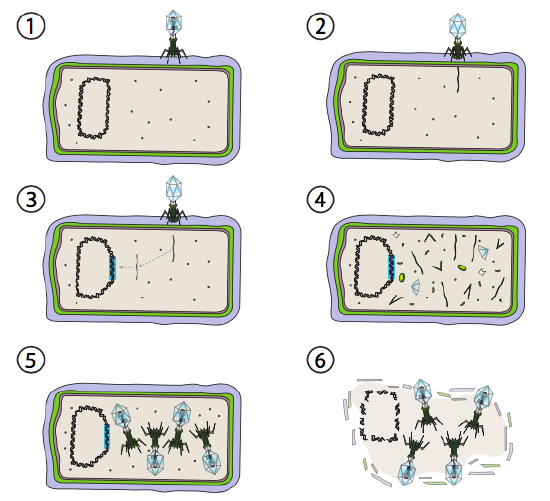
Lambda (λ) er et eksempel på en temperert bakteriofag. De første stadiene av infeksjon og genominjeksjon er de samme som den lytiske syklusen, men under forhold som oppfordrer lysogeni, er det virale genomet integrert i vertsgenomet i trinn 3. I λ integrering I E. coli, dette skjer ved gjensidig rekombinasjon ved en 15-baseparsekvens kjent som att λ-området og forenkles av int-genproduktet. Så lenge miljøforholdene ikke bidrar til bakteriell reproduksjon (og dermed begrenset antall mulige vertsceller), forblir det virale genomet for det meste skjult og inaktivt. Det eneste signifikante unntaket er et gen som koder for en λ repressor som forhindrer neste trinn og holder viruset sovende.
Det neste trinnet er eksisjonering av λ fag DNA FRA verten kromosom, og påfølgende replikasjon og transkripsjon av viral DNA (Figur \(\PageIndex{4}\), Trinn 4). Så, som før, er de siste trinnene montering og akkumulering av virioner, og eventuell nedbrytning av cellulær struktur og frigjøring av viruspartikler.
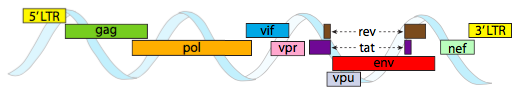
for å pakke inn i de stramme plassbegrensningene som gis av kapsidene, må virale genomer være svært økonomiske. FOR EKSEMPEL HAR HIV-genomet (Figur \(\PageIndex{6}\)) flere gener som overlapper.
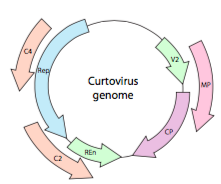
Eller, i tilfelle av curtoviruses, ssDNA plante virus (f.eks bete krøllete topp virus), genomet ikke bare har over – Rep lapping gener, er det enda toveis (Figur \(\PageIndex{7}\)) koding genprodukter i BEGGE tråder AV DNA etter at ssDNA er konvertert til dsDNA.
Gitt behovet for økonomi, hvilke gener finnes i virus? Et av de mest studerte virale genomene, bakteriofag λ, inneholder gener som koder for fem transkripsjonelle kontrollproteiner (hvilke uttrykkes avhenger av om fag er i lysogen eller lytisk modus), et bindende protein som styrer nedbrytning av en transkripsjonell aktivator, 17 kapsidproteiner, en excisionase som styrer eksisjon og innføring av faggenomet i vertsgenomet, et integrasjonsprotein som setter faggenomet inn i vertsens, og 3 gener som deltar i lysis av vertscellen.
HIV-genomet som er avbildet ovenfor, er mye mindre enn λ, rundt 9 kilobaser sammenlignet med 48 kb, men igjen er temaet å bruke cellulære proteiner når det er mulig, og kode virale gener om nødvendig. Så koder gag kapsidproteiner, pol koder for revers transkriptase, integrase og HIV-protease( som spalter gag-og pol-genproduktene i deres funksjonelle proteiner), vif virker mot et felles hostcelle antiviralt enzym, vpr regulerer kjerneimport, tat øker sterkt transkripsjon AV HIV-gener, reveksport viralt RNA fra kjernen, vpu er nødvendig for spirende partikler fra verten, env koder for virale konvoluttglykoproteiner, og nef fremmer overlevelse av infiserte celler. LTR-regionene er svært sterke promotorer for å drive høyt uttrykk for disse genene.
selv om det ikke er referert til som lysogeni, kan noen dyrevirus oppføre seg på samme måte. Det mest fremtredende eksempelet Er Baltimore Klasse VI virus-kjent som retrovirus, hvorav DEN ene ER HIV. Banen til et retrovirus gjennom en eukaryotisk vertscelle er avbildet nedenfor ( g. 5).
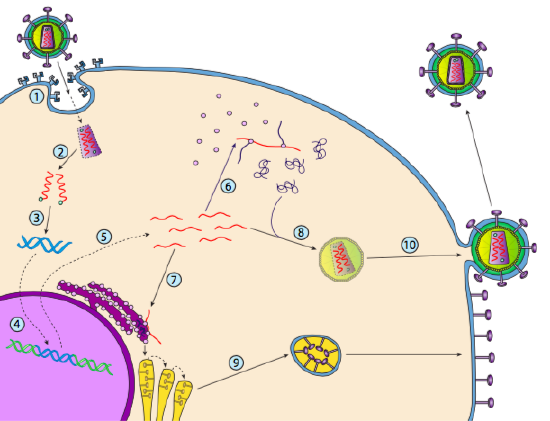
HIV HAR en konvolutt som er besatt med transmembrane proteiner som gjenkjennes av vertscellen, binder viruset til celleoverflaten og initierer reseptormediert endocytose (1). Etter endocytosen smelter membranhylsen til virionen og den vesikulære membranen for å frigjøre kapsidet og dets innhold (2). Etter at kapsidet dissosierer i cytoplasma, frigjøres de to strengene av viralt RNA sammen med en spesiell polymerase: revers transkriptase, som leser EN RNA-mal og syntetiserer DNA. Omvendt transkriptase bruker også det nye DNA til å syntetisere en komplementær DNA-streng slik at den til slutt produserer en dobbeltstrenget DNA-versjon av virusgenomet (3). Denne virale dsDNA transporteres inn i kjernen hvor den integreres i vertsgenomet ved hjelp av et annet virusprotein, integrase
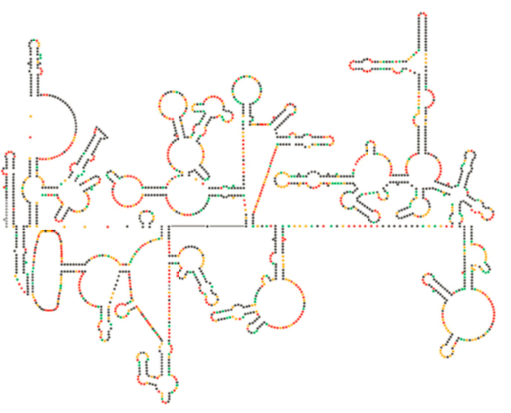
(4). Det integrerte virale DNA kalles et provirus. Proviruset kan ligge sovende, men hvis det er aktivert, blir det transkribert og det resulterende virale RNA transporteres ut av kjernen (5). Noen av virale RNA koder enzymer som revers transkriptase og integrase, eller kapsidproteiner, som alle er laget i cytoplasma (6), men noen koder membranbundne glykoproteiner, som translokeres til ER (7) og til slutt behandles Gjennom Golgi og inkorporeres i plasmamembranen (9). Når virionen er samlet (8), binder den seg til de virale transmembrane proteinene, og nukleerer en eksocytisk «vesikkel» (10) som er virionen komplett med viral konvolutt.Nylig strukturell undersøkelse AV HIV-genomet antyder at strukturen AV HIV-RNA selv kan spille en betydelig rolle i sin forplantning inne i vertsceller. Figur \(\PageIndex{8}\), Fra Watts et al, Nature 460:711-716, 2009, viser en spådd sekundær struktur av genomet. Forfatterne antyder at RNA-strukturen faktisk kan interagere med ribosomal forlengelse for å kontrollere foldingen av virusproteiner. De postulerer også utvidelsen av dette argumentet for å inkludere viktig genetisk informasjon kodet ikke bare i nukleotidsekvensen, men den sekundære strukturen og tertiære strukturen til ETHVERT RNA-virus.
når man vurderer virus med hensyn til resten av dette integrerende kapitlet, er det to overordnede ideer å huske på. For det første er viral overlevelse basert på tall: det må gjøre store antall komponenter for å kaste så bredt et nett for nye vertsceller som mulig. For å gjøre dette, er virale promotorer vanligvis mye sterkere enn vertscellepromotorer, samtidig som de driver mer viral genuttrykk mens de forhindrer verts genuttrykk (ved å dedikere cellulære ressurser til virusproduksjon). For det andre, på grunn av raske generasjonstider, er frekvensen av viral mutasjon og evolusjon langt raskere enn normale eukaryotiske genomer. I tillegg, hvis viruset bruker sin egen polymerase (som revers transkriptase eller RNA replikase), øker mutasjonsraten enda mer fordi det ikke er feilkontroll av virale polymeraser.