16.2: cicluri de viață virale
calea Lizogenă
o opțiune mai bună pentru unele virusuri bacteriene se numește calea lizogenă. Bacteriofagul care are această opțiune, precum și o cale litică, sunt cunoscute sub numele de fag temperat. În această cale, virusul intră în repaus prin integrarea în genomul gazdă și rămâne în repaus transcripțional până când condițiile de mediu se schimbă și reflectă probabilitatea ca mai multe celule gazdă să se infecteze (figura \(\PageIndex{4}\)).
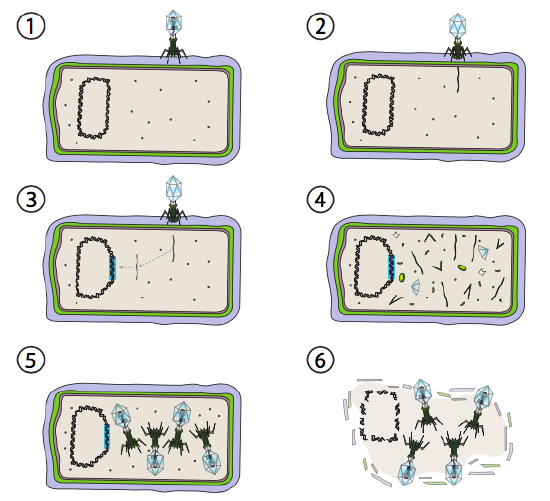
Lambda (XV) este un exemplu de bacteriofag temperat. Etapele inițiale ale infecției și injecției genomului sunt aceleași cu ciclul litic, dar în condiții care încurajează lizogenia, genomul viral este integrat în genomul gazdă în pasul 3. În integrarea în E. coli, acest lucru are loc prin recombinare reciprocă la o secvență de perechi de 15 Baze cunoscută sub numele de situsul att XV și este facilitată de produsul genei int. Atâta timp cât condițiile de mediu nu sunt favorabile reproducerii bacteriene (și astfel un număr limitat de celule gazdă posibile), genomul viral rămâne în mare parte ascuns și inactiv. Singura excepție semnificativă este o genă care codifică un represor cu un număr de centimetrii, care împiedică următorul pas și menține virusul în stare latentă.
următorul pas este excizia ADN-ului fagului de la cromozomul gazdă și replicarea și transcrierea ulterioară a ADN-ului viral (figura \(\PageIndex{4}\), Pasul 4). Apoi, ca și înainte, etapele finale sunt asamblarea și acumularea de virioni și eventuala descompunere a structurii celulare și eliberarea particulelor virale.
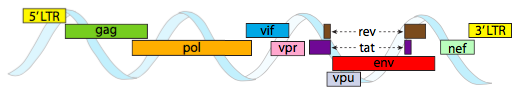
pentru ambalarea în constrângerile de spațiu strânse oferite de capside, genomii virali trebuie să fie extrem de economici. De exemplu, genomul HIV (figura \(\PageIndex{6}\)) are mai multe gene care se suprapun.
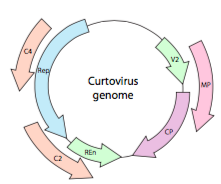
sau, în cazul curtovirusurilor, a virusurilor vegetale ssDNA (de exemplu, virusul de vârf al sfeclei), genomul nu numai că are gene suprapuse, ci este chiar bidirecțional (figura \(\PageIndex{7}\)) codifică produsele genetice în ambele fire de ADN după ce ssDNA a fost convertit în dsDNA.
având în vedere nevoia de Economie, ce gene se găsesc în viruși? Unul dintre cele mai studiate genomi virali, bacteriofagul, conține gene care codifică cinci proteine de control transcripțional (care sunt exprimate depinde de faptul dacă fagul este într-un mod lizogen sau litic), o proteină de legare care controlează degradarea unui activator transcripțional, 17 proteine capsidice, o excizionază care controlează excizia și inserarea genomului fagului în genomul gazdă, o proteină de integrare care introduce genomul fagului în gazdă și 3 gene care participă la liza celulei gazdă.
genomul HIV descris mai sus este mult mai mic decât cel de la hectolitru, la aproximativ 9 kilobaze comparativ cu 48 kb, dar din nou, Tema este utilizarea proteinelor celulare atunci când este posibil și codificarea genelor virale, dacă este necesar. Deci, gag codifică proteinele capsidei, pol codifică transcriptaza inversă, integraza și proteaza HIV (care scindează produsele genei gag și pol în proteinele lor funcționale), Vif acționează împotriva unei enzime antivirale comune a celulei gazdă, VPR reglează importul nuclear, tat crește puternic transcrierea genelor HIV, rev exportă ARN viral din nucleu, vpu este necesar pentru înmugurirea particulelor din gazdă, env codifică glicoproteinele învelișului viral, iar nef promovează supraviețuirea celulelor infectate. Regiunile LTR sunt promotori foarte puternici pentru a stimula exprimarea ridicată a acestor gene.
deși nu este denumită lizogenie, unele virusuri animale se pot comporta în mod similar. Cel mai proeminent exemplu este Baltimore clasa VI viruși – cunoscut sub numele de retrovirusuri, dintre care unul este HIV. Calea unui retrovirus printr-o celulă gazdă eucariotă este descrisă mai jos ( g. 5).
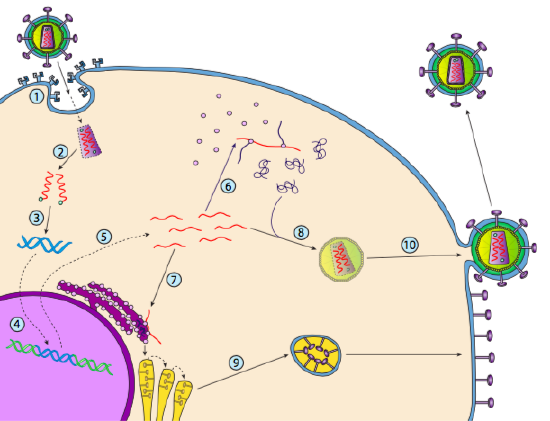
HIV are un înveliș, care este împânzit cu proteine transmembranare care sunt recunoscute de celula gazdă, legând virusul de suprafața celulei și inițiind endocitoza mediată de receptor (1). După endocitoză, învelișul membranei virionului și membrana veziculară fuzionează pentru a elibera capsida și conținutul acesteia (2). După ce capsida se disociază în citoplasmă, cele două fire de ARN viral sunt eliberate împreună cu o polimerază specială: transcriptaza inversă, care citește un șablon de ARN și sintetizează ADN-ul. Transcriptaza inversă folosește, de asemenea, acel nou ADN pentru a sintetiza o catenă ADN complementară, astfel încât să producă în cele din urmă o versiune ADN dublu catenară a genomului viral (3). Acest dsDNA viral este transportat în nucleu unde se integrează în genomul gazdă folosind o altă proteină virală, integraza
(4). ADN-ul viral integrat se numește provirus. Provirusul poate rămâne latent, dar dacă este activat, atunci este transcris și ARN-ul viral rezultat este transportat din nucleu (5). Unele dintre ARN-ul viral codifică enzime precum revers transcriptază și integrază sau proteine capsidice, toate acestea fiind făcute în citoplasmă (6), dar unele codifică glicoproteine legate de membrană, care sunt translocate în ER (7) și în cele din urmă procesate prin Golgi și încorporate în membrana plasmatică (9). Odată ce virionul a fost asamblat (8), se leagă de proteinele transmembranare virale, nucleând o „veziculă” exocitară (10) care este virionul complet cu înveliș viral.
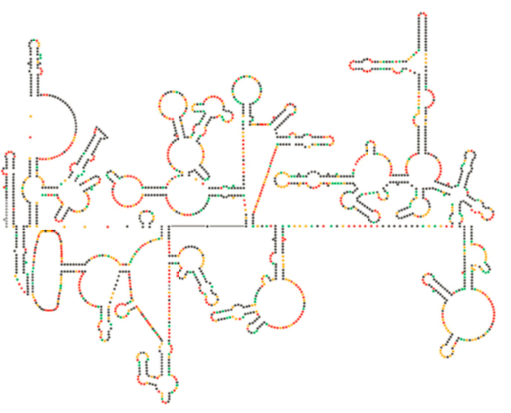
examinarea structurală recentă a genomului HIV sugerează că structura ARN HIV în sine poate juca un rol semnificativ în propagarea sa în interiorul celulelor gazdă. Figura \(\PageIndex{8}\), Din Watts și colab., Nature 460:711-716, 2009, arată o structură secundară prezisă a genomului. Autorii sugerează că structura ARN poate interacționa cu alungirea ribozomală pentru a controla plierea proteinelor virale. De asemenea, postulează extinderea acestui argument pentru a include informații genetice importante codificate nu doar în secvența nucleotidică, ci structura secundară și structura terțiară a oricărui virus ARN.
în luarea în considerare a virușilor în ceea ce privește restul acestui capitol integrativ, există două idei imperative de reținut. În primul rând, supraviețuirea virală se bazează pe numere: trebuie să facă un număr imens de componente pentru a arunca o plasă cât mai largă pentru noi celule gazdă. Pentru a face acest lucru, promotorii virali sunt de obicei mult mai puternici decât promotorii celulelor gazdă, conducând simultan mai multă expresie a genelor virale, prevenind în același timp expresia genelor gazdă (prin dedicarea resurselor celulare producției de virusuri). În al doilea rând, din cauza timpilor de generare rapidă, rata mutației și evoluției virale este mult mai rapidă decât genomul eucariot normal. În plus, dacă virusul folosește propria polimerază (cum ar fi transcriptaza inversă sau REPLICAZA ARN), rata mutației crește și mai mult, deoarece nu există nicio verificare a erorilor de către polimerazele virale.