16.2: virális életciklusok
A lizogén út
néhány bakteriális vírus számára jobb megoldást lizogén útnak hívnak. Azok a bakteriofágok, amelyek rendelkeznek ezzel a lehetőséggel, valamint egy litikus út, mérsékelt fágként ismertek. Ezen az úton a vírus nyugalmi állapotba kerül azáltal, hogy integrálódik a gazdaszervezet genomjába, és transzkripciós nyugalomban marad, amíg a környezeti feltételek megváltoznak, és tükrözik annak valószínűségét, hogy több gazdasejt megfertőződik (\(\pageindex{4}\) ábra).
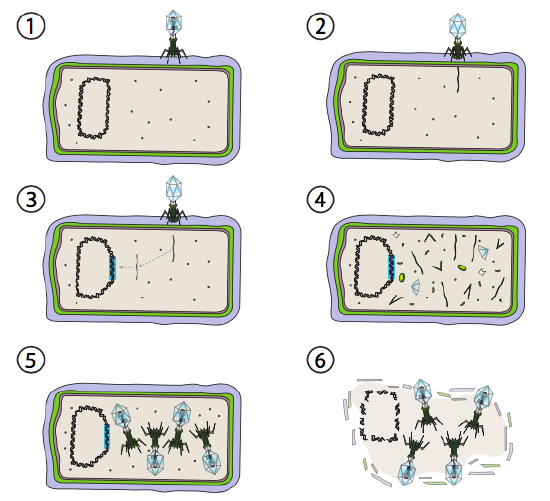
a Lambda (ons) egy mérsékelt bakteriofág példája. A fertőzés és a genominjekció kezdeti szakaszai megegyeznek a litikus ciklussal, de olyan körülmények között, amelyek ösztönzik a lizogenitást, a vírusgenomot a 3.lépésben integrálják a gazdaszervezet genomjába. Az e-be történő integrálás során. coli, ez akkor fordul elő a reciprok rekombináció egy 15-bázis pár szekvencia ismert, mint az ATT helyen, és megkönnyíti az Int gén termék. Mindaddig, amíg a környezeti feltételek nem kedveznek a baktériumok szaporodásának (és így korlátozott számú lehetséges gazdasejt), a vírusgenom többnyire rejtett és inaktív marad. Az egyetlen jelentős kivétel egy olyan gén, amely a következő lépést megakadályozza, és nyugvó állapotban tartja a vírust.
Ez a következő lépés a gazda kromoszómából a DNS-fágok kimetszése, majd ezt követően a vírus DNS replikációja és transzkripciója (\(\Pageindex{4}\) ábra, 4.lépés). Ezután, mint korábban, az utolsó lépések a virionok összeszerelése és felhalmozódása, valamint a sejtszerkezet esetleges lebontása és a vírusrészecskék felszabadulása.
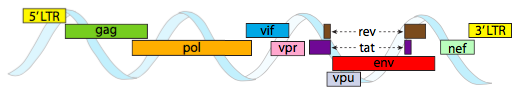
annak érdekében, hogy a kapszidok által biztosított szűk helykorlátokba csomagolják, a vírusgenomoknak rendkívül gazdaságosnak kell lenniük. Például a HIV Genom (\(\pageindex{6}\) ábra) több génnel rendelkezik, amelyek átfedik egymást.
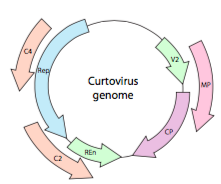
vagy a curtovírusok esetében ssdns növényi vírusok (pl. beet curly top vírus), a genom nem csak túl Rep átfedő génekkel rendelkezik, hanem kétirányú is (ábra \(\PageIndex{7}\)) géntermékeket kódol a DNS mindkét szálában, miután az ssdns – t dsDNS-vé alakították át.
tekintettel a gazdaságosság szükségességére, milyen gének találhatók a vírusokban? Az egyik legtöbbet tanulmányozott vírusgenom, a bakteriofág, öt transzkripciós kontrollfehérjét kódoló géneket tartalmaz (melyek expresszálódnak attól függően, hogy a fág lizogén vagy litikus módban van-e), egy kötő fehérjét, amely szabályozza a transzkripciós aktivátor lebomlását, 17 kapszidfehérjét, egy excisionázt, amely szabályozza a fággenom kivágását és beillesztését a gazdaszervezetbe, egy integrációs fehérjét, amely beilleszti a fággenomot a gazdaszervezetbe, és 3 gént vesz részt a gazdasejt lízisében.
a fent ábrázolt HIV Genom sokkal kisebb, mint az 6, körülbelül 9 kilobázissal, szemben a 48 kb-val, de ismét a téma az, hogy lehetőség szerint celluláris fehérjéket használjunk, és szükség esetén vírusgéneket kódoljunk. Tehát a gag kódolja a kapszid fehérjéket, a pol kódolja a reverz transzkriptázt, az integrázt és a HIV proteázt (amely a gag és a pol géntermékeket funkcionális fehérjéikbe hasítja), a vif egy közös gazdasejt antivirális enzim ellen hat, a VPR szabályozza a nukleáris importot, a tat erősen növeli a HIV gének transzkripcióját, a Rev exportálja a vírus RNS-t a magból, a VPU szükséges a gazdaszervezet részecskéinek bimbózásához, az env kódolja a vírusburok glikoproteinjeit, és a NEF elősegíti a fertőzött sejtek túlélését. Az LTR régiók nagyon erős promóterek ezen gének magas expressziójának elősegítésére.
bár nem nevezik lizogénnek, egyes állati vírusok hasonlóan viselkedhetnek. Osztályú vírusok-közismert nevén retrovírusok, amelyek közül az egyik a HIV. Az alábbiakban bemutatjuk a retrovírus útját egy eukarióta gazdasejten keresztül (5. g).
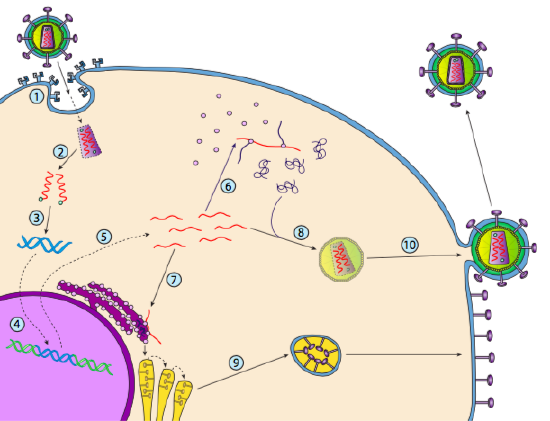
a HIV-nek van egy borítéka, amely transzmembrán fehérjékkel van ellátva, amelyeket a gazdasejt felismer, a vírust a sejtfelszínhez köti és receptor által közvetített endocitózist indít (1). Az endocitózis után a virion membrán burkolata és a vezikuláris membrán összeolvad, hogy felszabadítsa a kapszidot és annak tartalmát (2). Miután a kapszid disszociál a citoplazmában, a vírus RNS két szálát felszabadítják egy speciális polimerázzal együtt: reverz transzkriptáz, amely egy RNS-sablont olvas és szintetizálja a DNS-t. A reverz transzkriptáz ezt az új DNS – t egy komplementer DNS-szál szintetizálására is felhasználja, így végül a vírusgenom kettős szálú DNS-változatát állítja elő (3). Ezt a vírusos dsDNS-t a magba szállítják, ahol egy másik vírusfehérje, az integráz
(4) segítségével integrálódik a gazdaszervezet genomjába. Az integrált vírus DNS-t provírusnak nevezik. A provírus szunnyadhat, de ha aktiválódik, akkor átíródik, és a kapott vírus RNS-t kiszállítják a magból (5). A vírus RNS egy része olyan enzimeket kódol, mint a reverz transzkriptáz és integráz, vagy kapszid fehérjék, amelyek mindegyike a citoplazmában készül (6), de néhány membránhoz kötött glikoproteineket kódol, amelyek transzlokálódnak az ER-be (7), majd végül feldolgozzák a Golgi-n keresztül, és beépülnek a plazmamembránba (9). Miután a virion összeállt (8), kötődik a vírus transzmembrán fehérjéihez, egy exocita “vezikulumot” (10) nukleálva, amely a virion teljes vírusos borítékkal.
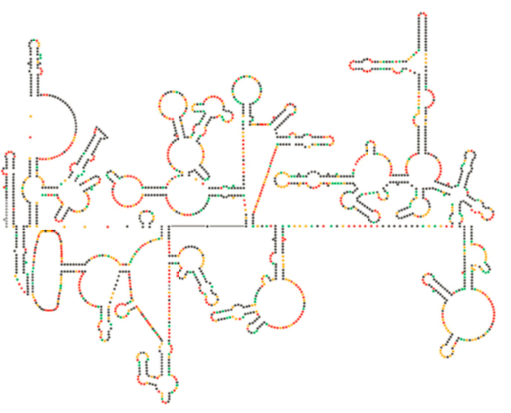
a HIV Genom legújabb szerkezeti vizsgálata azt sugallja, hogy maga a HIV RNS szerkezete jelentős szerepet játszhat a gazdasejteken belüli szaporodásában. Ábra \(\PageIndex{8}\), Watts et al, Nature 460:711-716, 2009, a genom előre jelzett másodlagos szerkezetét mutatja. A szerzők azt sugallják, hogy az RNS szerkezete valójában kölcsönhatásba léphet a riboszomális megnyúlással a vírusfehérjék hajtogatásának szabályozására. Azt is feltételezik, hogy ennek az érvnek a kiterjesztése magában foglalja a fontos genetikai információkat, amelyek nemcsak a nukleotidszekvenciában vannak kódolva, hanem bármely RNS vírus másodlagos és harmadlagos struktúrájában.
a vírusok ezen integratív fejezet többi részének figyelembevételével két legfontosabb ötletet kell szem előtt tartani. Először is, a vírus túlélése számokon alapul: hatalmas számú komponenst kell készítenie ahhoz, hogy a lehető legszélesebb hálót öntse az új gazdasejtek számára. Ehhez a víruspromoterek általában sokkal erősebbek, mint a gazdasejt-promoterek, egyidejűleg több vírusgén expressziót vezetnek, miközben megakadályozzák a gazdagén expresszióját (a sejtes erőforrások vírustermelésnek szentelésével). Másodszor, a gyors generációs idő miatt a vírus mutációjának és evolúciójának sebessége sokkal gyorsabb, mint a normál eukarióta genomoké. Ezenkívül, ha a vírus saját polimerázt (például reverz transzkriptázt vagy RNS replikázt) használ, akkor a mutációs sebesség még tovább növekszik, mivel a víruspolimerázok nem ellenőrzik a hibákat.